您还不是认证园区!
赶快前去认证园区吧!
▎药明康德内容团队编辑
12月14日,中国国家药监局药品审评中心(CDE)官网公示,百吉生物申报的1类新药BRG01注射液获得临床试验默示许可,拟开发适应症为经标准治疗后失败且无有效治疗手段的末线复发/转移性EBV阳性鼻咽癌。根据百吉生物公开资料,BRG01注射液是一款通过基因修饰技术将靶向EB病毒(EBV)抗原的受体表达于T细胞表面而制备成的自体T细胞免疫治疗产品。
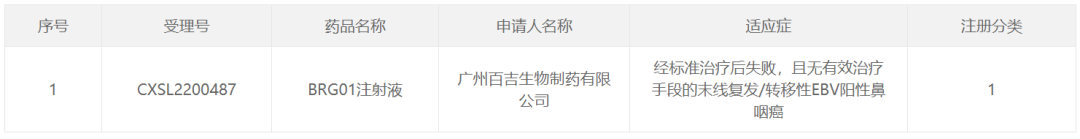 截图来源:CDE官网
截图来源:CDE官网

公开资料显示,百吉生物专注于研发创新型免疫细胞疗法,在治疗鼻咽癌、胃癌、消化道类肿瘤、淋巴瘤和淋巴细胞增生性疾病等多种实体瘤和血液瘤领域拥有全球独家授权和自主研发产品。
百吉生物董事长张琼女士表示,BRG01注射液申报IND获得临床试验默示许可是该公司又一具有里程碑意义的进展。百吉生物目前已有多条管线进入研究者发起的临床试验,并将于2023年完成中国、美国、新加坡三地针对肝癌、结直肠癌、胃癌、食道癌、胰腺癌等癌种的药品临床试验申报,并陆续有产品进入1期和2期临床试验。

本文由药明康德内容团队根据公开资料整理编辑,欢迎个人转发至朋友圈。转发授权请在「医药观澜」微信公众号留言联系我们。转载授权请在「医药观澜」微信公众号留言联系我们。其他合作需求,请联系wuxi_media@wuxiapptec.com。
免责声明:药明康德内容团队专注介绍全球生物医药健康研究进展。本文仅作信息交流之目的,文中观点不代表药明康德立场,亦不代表药明康德支持或反对文中观点。本文也不是治疗方案推荐。如需获得治疗方案指导,请前往正规医院就诊。




 个人中心
个人中心
 我是园区
我是园区




