 以CAR-T\NK为代表的免疫细胞疗法在白血病、淋巴瘤、多发性骨髓瘤等多种恶性肿瘤疾病的治疗中展现出显著的治疗效果而成为国内外研究的热点,目前全球已有多款细胞治疗药物被FDA批准上市。随着越来越多的免疫细胞疗法进入临床研究和上市申请阶段,对应的质量和生产管理规范问题也越来越受到行业的关注。在免疫细胞治疗产品的生产过程中,培养基补充剂如IL-15、IL-7以及IL-21等细胞因子是T\NK免疫细胞增殖分化的主要试剂,是免疫细胞治疗药物生产的关键原材料。FDA和《中国药典》对这些关键物料的使用均有相关规定,其中FDA CMC建议使用FDA批准的或者临床级别的物料,国内规定使用的原材料要优先选择低风险级别的,比如建议使用GMP级的材料优于非GMP级。因此使用安全性、有效性以及符合规范的细胞因子对于免疫细胞治疗药物的成功研发和顺利申报上市至关重要。
以CAR-T\NK为代表的免疫细胞疗法在白血病、淋巴瘤、多发性骨髓瘤等多种恶性肿瘤疾病的治疗中展现出显著的治疗效果而成为国内外研究的热点,目前全球已有多款细胞治疗药物被FDA批准上市。随着越来越多的免疫细胞疗法进入临床研究和上市申请阶段,对应的质量和生产管理规范问题也越来越受到行业的关注。在免疫细胞治疗产品的生产过程中,培养基补充剂如IL-15、IL-7以及IL-21等细胞因子是T\NK免疫细胞增殖分化的主要试剂,是免疫细胞治疗药物生产的关键原材料。FDA和《中国药典》对这些关键物料的使用均有相关规定,其中FDA CMC建议使用FDA批准的或者临床级别的物料,国内规定使用的原材料要优先选择低风险级别的,比如建议使用GMP级的材料优于非GMP级。因此使用安全性、有效性以及符合规范的细胞因子对于免疫细胞治疗药物的成功研发和顺利申报上市至关重要。
ACROBiosystems百普赛斯致力于开发高质量的,应用于免疫细胞治疗药物临床阶段的相关试剂,特在拥有GMP级质量管理体系平台的基础上,结合细胞治疗药物生产规范,以更严格的质量管理和药品级放行检测标准,成功开发了一系列如IL-15、IL-7、IL-21等高质量的GMP级别细胞因子*。ACRO GMP级细胞因子*可更好助力免疫细胞治疗药物的临床研究,加速临床、上市申报进程。
*ACROBiosystems GMP级产品是为研发,生产或体外使用而设计的,不能直接用于人体。
GMP质量管理体系
经ISO 9001:2015 和 ISO 13485:2016认证
生产厂房具备药品生产许可证
药品B+A级洁净室和自动灌装设备
无菌技术与二级除菌过滤
无动物源性材料和生产环境
人员培训体系
供应商和原材料管理体系
质量文件/记录经QA审查和批准
完整的批生产和检验记录
设备维护和校准程序
分析方法的验证
主要生产设备

全自动罐装设备
灭菌设备

全方位质量放行验证(IL-15放行标准为例)
细胞活性高于0.8 x 107 IU/mg
纯度高于95%
内毒素低于10EU/mg
宿主蛋白残留低于0.5ng/ug
无菌检测
支原体检测
外源病毒检测
全面的稳定性数据支持(加速,冻融,长期,运输稳定性验证)
高批间一致性
......
ACRO GMP级细胞因子产品特色
16项质量控制指标
更好的安全性(无菌,支原体,外源病毒,各项杂质残留检测)
高稳定性和批间一致性
更严格GMP质量管理体系
药品级生产厂房
药用级物料/包材
支持线上/线下审计
加速临床/上市申报
完整的细胞/基因治疗产品申报支持文档
提供全套方法学验证报告
FDA DMF(备案中)
产品列表
| 产品名 | 货号 |
|---|---|
| GMP Human IL-15 | GMP-L15H13 |
| GMP Human IL-7 | GMP-L07H14 |
| GMP Human IL-21 | GMP-L21H18 |

验证数据
高纯度
经SDS-PACE验证,(Cat. No. GMP-L15H13)纯度>95%。

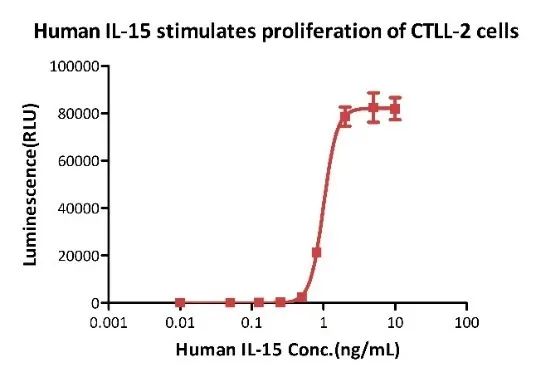
高生物活性
刺激CTLL-2细胞增殖实验结果显示,GMP Human IL-15(Cat. No. GMP-L15H13)的细胞活性高于0.8ⅹ10^7IU/mg(经WHO Human IL-15标品校准,NIBSC 代码:95/554)。
欢迎添加文末ACRO小助手咨询订购
高稳定性
加速和冻融稳定性验证:GMP Human IL-15 (Cat. No. GMP-L15H13) 在25℃加速8/24/48/72h条件下和冻融三次后,细胞活性均保持不变。
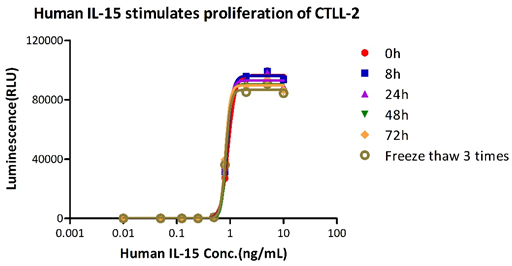
长期稳定性检测(4℃):GMP Human IL-15 (Cat. No. GMP-L15H13) 在4℃下储存1/3/7/10/14d,细胞活性无下降。
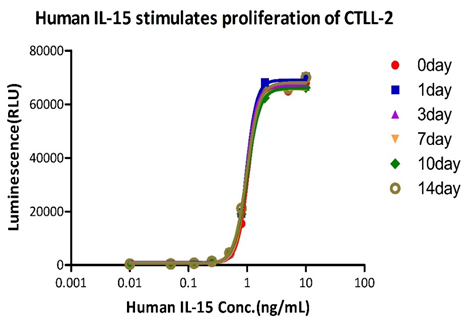
欢迎添加文末ACRO小助手咨询订购
高批间一致性
GMP Human IL-15 (Cat. No. GMP-L15H13)不同批次的细胞活性保持一致,具有高批间一致性。
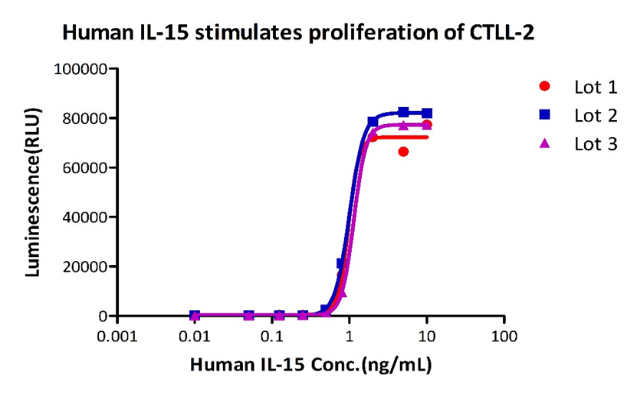
欢迎添加文末ACRO小助手咨询订购


ACROBiosystems
inquiry@acrobiosystems.com
15117918562
(备注:姓名+公司)
请注明:姓名+研究方向!


本公众号所有转载文章系出于传递更多信息之目的,且明确注明来源和作者,不希望被转载的媒体或个人可与我们联系(cbplib@163.com),我们将立即进行删除处理。所有文章仅代表作者观点,不代表本站立场。




 个人中心
个人中心
 我是园区
我是园区





