


识别二维码立即免费报名


南京汉欣医药科技有限公司
——上海站展位号:W26-2
南京汉欣医药科技有限公司是一家坐落于江苏生命科技创新园的高科技医药科技企业,是美药星(南京)制药有限公司的全资子公司,注册资本1.06亿元。公司专注于创新药和大分子药物的自主研发,并为客户提供国际化的药品研发CRO/CDMO服务。公司位于江苏生命科技创新园C5幢,拥有13000平米的现代化综合研发大楼,含发酵、纯化、多肽、合成、酶催化、制剂、分析等各类实验室30余间,实验室内有价值近亿元的各类先进仪器,能够完成各类产品的研发、小试和中试,商业化生产则依托于其母公司美药星进行。
汉欣医药目前拥有员工近200人,包括海归博士多名,硕士占比50%以上。公司科研人员占比超过90%,形成了十余支专业化的研发团队,从事生物药、化药、健康产品等多方面的研发工作,是一支有创新能力和高效率的研发队伍。
汉欣医药与多所国内外顶尖大学和研究机构都有良好的合作,与南京大学、中国药科大学、江南大学、南京中医药大学等保持着深度的产学研合作。
发展历程:
1
2010年
研发团队成立。
2
2012年
基因重组团队成立。
3
2015年
协助客户研发的某蛋白酶注射液美国NDA获批。
4
2016年
制剂团队成立。
5
2017年
汉欣医药正式挂牌成立。
6
2018年
协助客户研发的两个化学药和一个多糖药美国ANDA获批;第一个基因重组API在美国申报DMF;独立科研大楼投入使用。
7
2019年
第一个基因重组API在美申报临床;多个药品和基因重组研发项目团队成立。
合作模式:
以中国价格向客户提供达到美欧要求的CRO/CDMO服务。
利用我方在美欧的临床资源,完成符合美欧要求的临床,客户可利用临床数据进行全球申报。
提供中英双语文件,帮助客户进行中美欧国际化申报。
利用我方美欧市场网络,帮助客户开拓药品海外市场。
引进配套投资基金投资客户项目。
功能模块/细分:
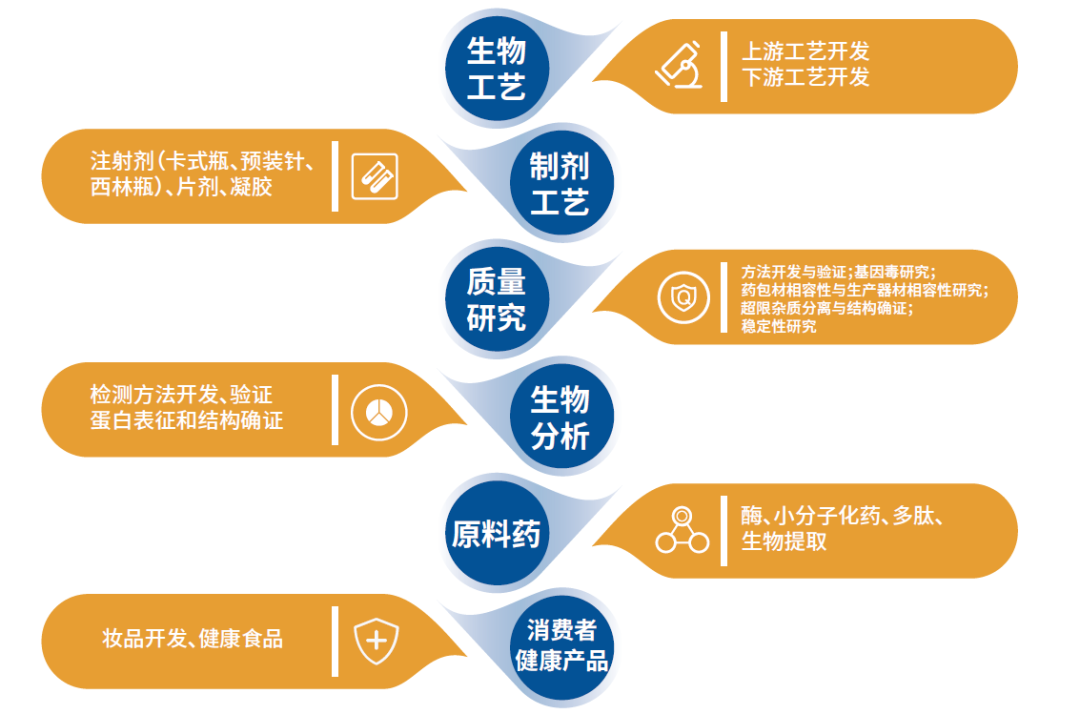
生物工艺开发(上游):
团队和平台能够同时运行多个处于不同阶段的工艺开发项目。工艺开发团队以及多样化的技术平台能够承接起始于任何不同开发阶段的项目。上游开发团队能够支持的项目类型包括:
♦ 独立项目:
● 克隆设计,宿主和克隆筛选,培养基优化等
● 为不同阶段的项目做起始物料,包括RCB/MCB/WCB制备、检测和鉴定
● 以提高产量和/或产品质量为目的的工艺优化
♦ 支持IND申报的微生物培养工作:
● 菌株构建,工艺优化,放大以及动物安评实验用药生产
● 技术转移至cGMP工厂进行生产以支持全球IND申报
♦ 项目后期的培养工艺开发:
● 技术转移
生物工艺开发(下游)
♦ 技术服务包括:
● 各种层析纯化工艺开发和优化
● 各种层析工艺的放大研究
● 层析填料筛选,动态载量测定,填料寿命和清洗研究
● 超限未知杂质的分离纯化、赋值标化
● 重组蛋白样品的制备
● 病毒灭活和病毒去除过滤工艺开发
● 针对各种纯化工艺单元操作的风险和成本收益评估
根据客户需求,工艺开发团队能够基于现有的蛋白下游纯化平台,快速地建立起生产工艺;其产品整体回收率在30%至70%之间,产品特性、工艺及产品相关杂质含量均在可接受的范围内(如抗体产品DNA < 100 ppb,HCP < 100 ppm等)。同样,不论是对于单克隆抗体还是其他种类的蛋白,我们都提供方法转移,开发和优化以满足客户需求,并且可以通过定制工艺满足客户对于产品质量的特殊要求。例如,对于胰岛素等蛋白生物类似药,可进一步降低DNA和HCP的水平。
对于处于临床晚期阶段的工艺及项目,我们可以设计和实施工艺优化和工艺验证,并协助完成申报流程的CMC部分。在下游工艺开发的每个阶段,从最初的工艺设计,到每一步单元操作的优化,直至最终的工艺放大,non-GMP生产和GMP生产的技术转移,我们都将为客户提供巨大优势的服务。
♦ 强大的研发能力:
汉欣医药下游工艺开发部门拥有10数间实验室用于生物药的低压、高压纯化和干燥,并拥有实验室型蛋白纯化系统10数台,以及中试低压及高压纯化仪10数台,这些系统保证了我们能够快速有效的提供客户所需的服务。
制剂工艺开发:
● 为API生产工艺开发提供制剂相关的前期支持和开发服务;
● 仿制药或生物类似药RLD选择,RLD全面解析;
● 制剂开发关键辅料的筛选;
● 通过统计学实验设计 (DOE) 确定最佳处方及影响因素;
● 基于QbD的生产工艺参数优化;
● 包装材料和容器系统筛选;
● 为GMP生产提供技术转移及工艺放大等支持;
● 开展药物的配伍稳定性研究,包括对稀释效应的评估以及对药液与注射设备相容性的研究等;
开发剂型:__注射剂(包含卡式瓶、预装针、西林瓶溶液、西林瓶冻干粉);固体口服片剂;外用凝胶制剂。
技术平台:__①重组蛋白/克隆抗体生物药的液体和冻干粉技术平台;②混悬剂、乳剂、脂质体、纳米晶等注射剂技术平台;③固体速释制剂及缓控释制剂处方研究与一致性评价技术平台;④注射剂一致性评价技术平台;⑤包材相容性技术平台。
质量研究:
♦ 分析方法开发:
汉欣医药能够采用色谱技术(GC、HPLC、UPLC)及其他多种检测技术(旋光、UV、IR、MS、MS/MS、TOF、FID、ICP、NMR等),提供完整的分析方法学服务,见下表。

♦ 质谱能力:
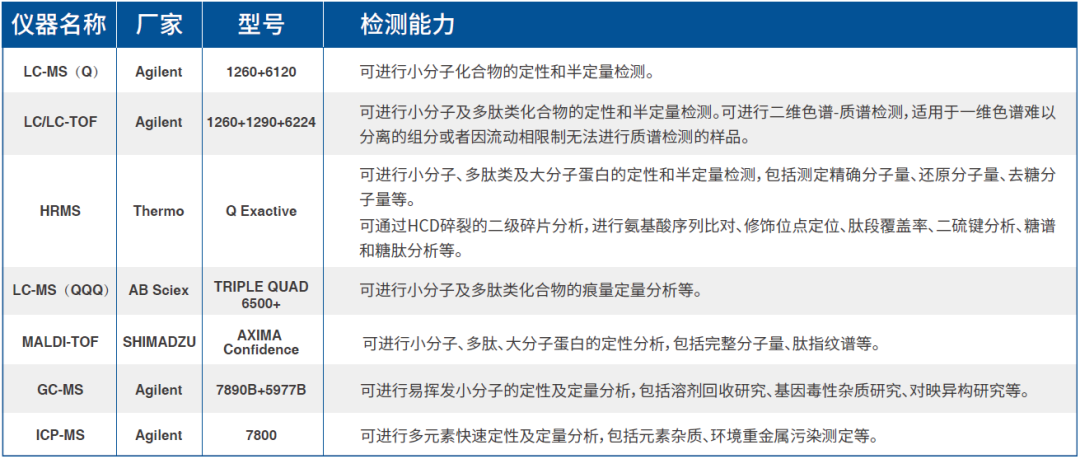
♦ 稳定性研究:
生物分析检测服务:
表1:生物检测分析服务
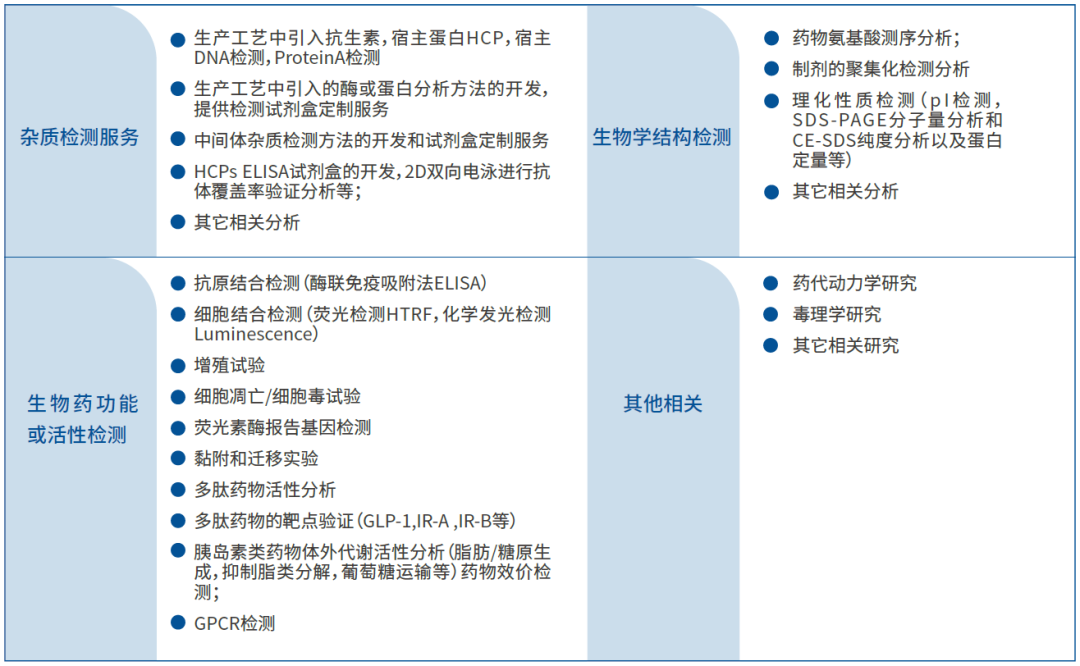
蛋白表征:
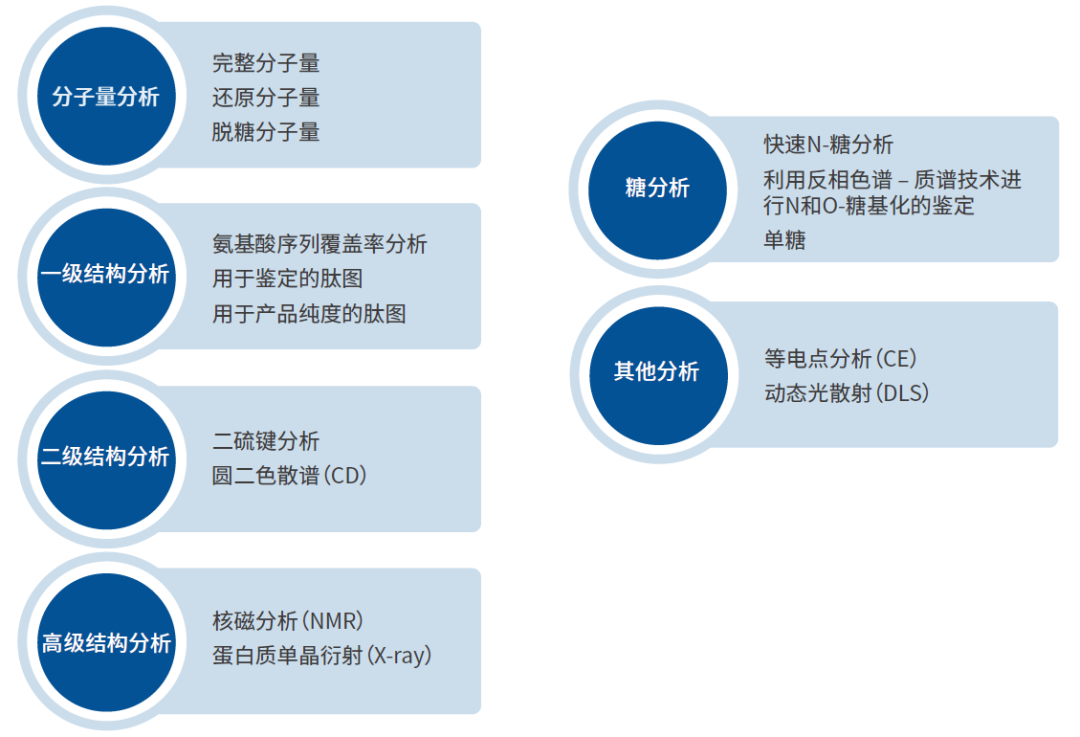
原料药:
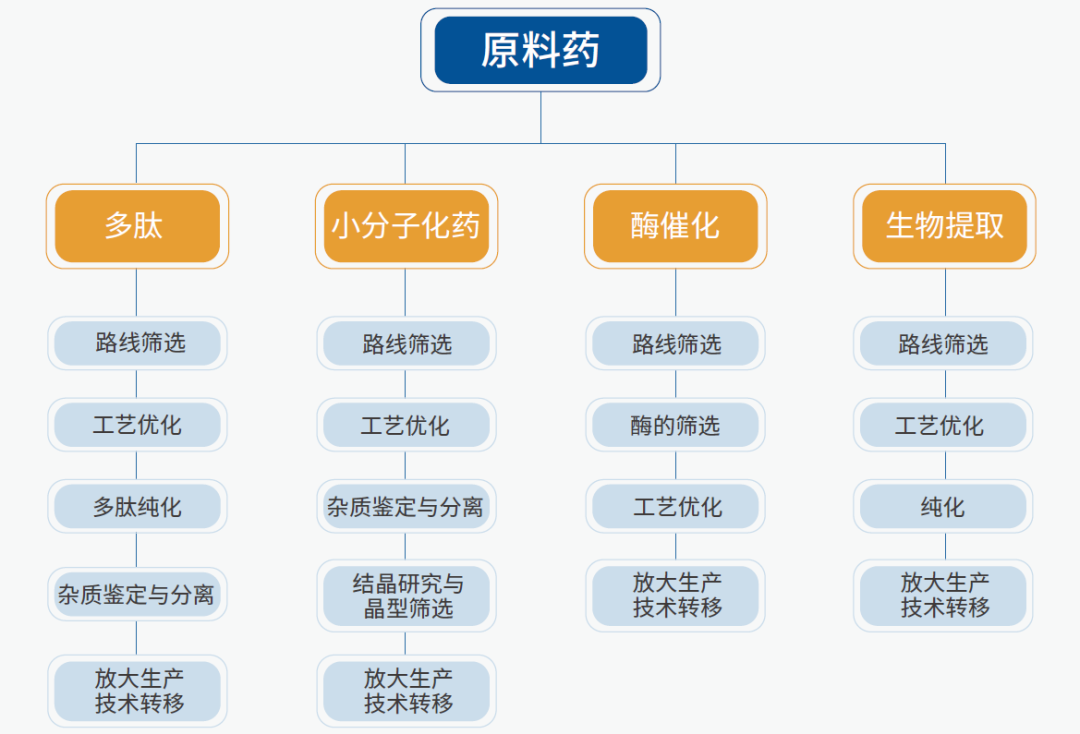
消费者健康产品:
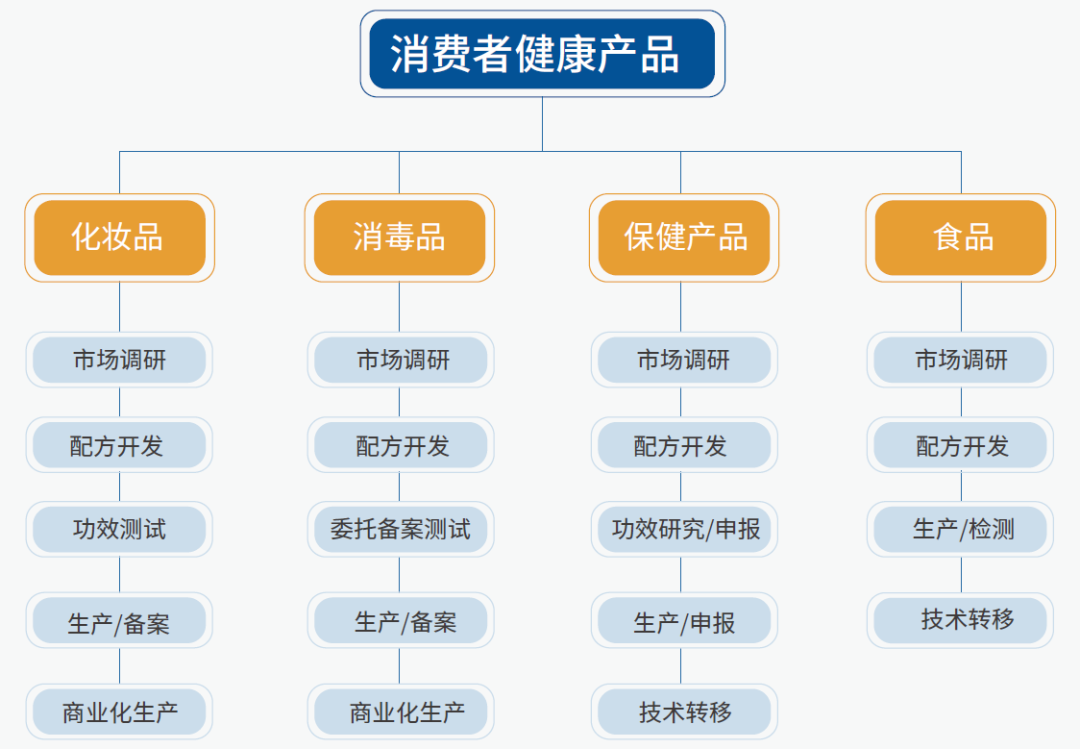
原料药生产:
上游拥有多个1000L和5000L规模的微生物反应器,下游拥有数台低压层析系统(柱直径200cm~1200cm)和数台高压层析系统(柱直径200cm~600cm),可以满足不同客户对原料生产的不同需求。
● 经过验证的内部公用系统。
● A-D级洁净区
● GMP多温度段(-80℃到35℃)仓库
● 动物、微生物和细胞检验
● 两条独立的供电线路
● 备用大型柴油发电机
● 用于关键设备、冰箱和仪器的UPS电源
● 生物垃圾和废水处理系统
♦ 项目管理:
由专职项目经理负责管理客户项目的各个方面。项目经理是项目联系人,与项目/客户专属的CMC负责人一起,协调项目组成员的沟通和互动,确保可交付成果和成本目标按时达成。为便利于整个项目过程中的交流互动,我们欢迎客户在技术转移的过程中现场办公,在项目的关键阶段提供协助,或作为“驻厂人员”。
严格遵循药品生产质量管理规范,以确保持续稳定地产出高质量的产品。
配备有门类齐全的先进仪器、设备、设施及完善的质量管理系统以保证对研发,生产和服务的严格监管,使得产品能够满足美国药典、中国药典、欧洲药典等标准。
♦ 业绩/里程碑:
● 2014年至2019年期间,多次接受并通过美国FDA检查
● 至今已向美国FDA提交近20个产品的注册资料
● 生物原料车间通过FDA检察官现场检查
● 在美已批多个原料药
● 多个生物原料药在美临床

制剂产品灌装生产:
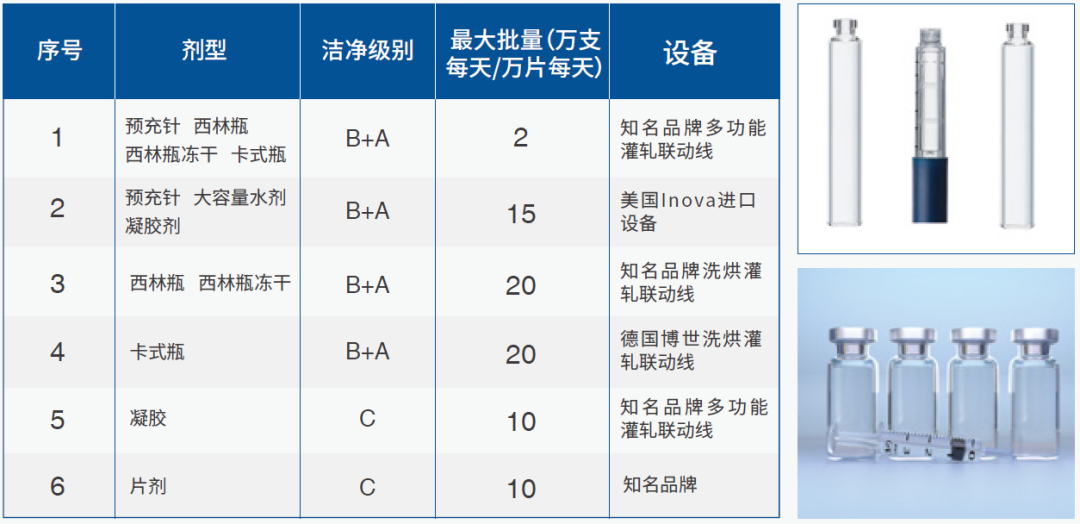
为客户提供一站式研发和生产服务,符合中美欧等全球申报的要求
● 药品制剂生产工艺开发
● 分析方法开发和验证
● 工艺验证、验证批生产
● 非临床研究
● 临床样品生产(原料+制剂)
● 注册申请资料撰写
● IND申请
● 进行临床I期/II期研究
● 进行临床III期研究(整合集团内美国研究机构资源)
● 中美欧NDA/BLA上市申报
荣誉成果:

合作伙伴:

联系我们:

张大志:15611932168(微信同号)

识别二维码可添加微信好友






 点击“阅读原文”查看2020年线下会议安排!
点击“阅读原文”查看2020年线下会议安排!



 个人中心
个人中心
 我是园区
我是园区




