11 月份
获批临床报告
◆ 11 月获批临床的新药共有 124 个受理号,涉及 86 个品种(附名单)
本报告数据来源:Insight 数据库、CDE 药物临床试验登记与信息公示

本月获批临床新药品种
Insight 数据库(https://db.dxy.cn)申报进度库显示,2021 年 11 月获批临床的新药共有 124 个受理号,涉及 86 个品种,下图为具体名单:
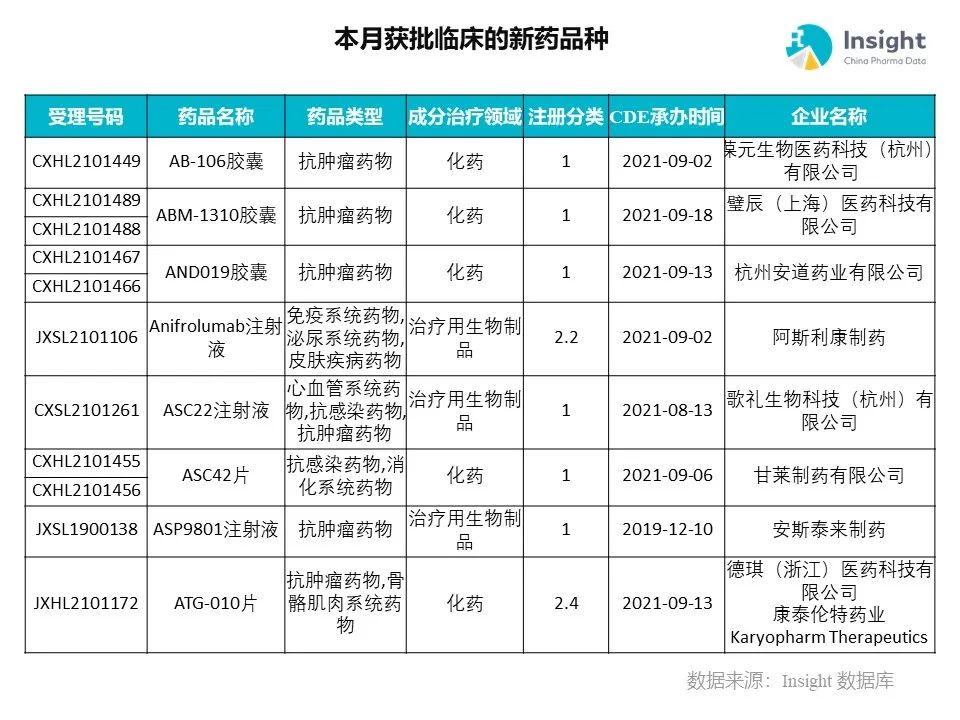
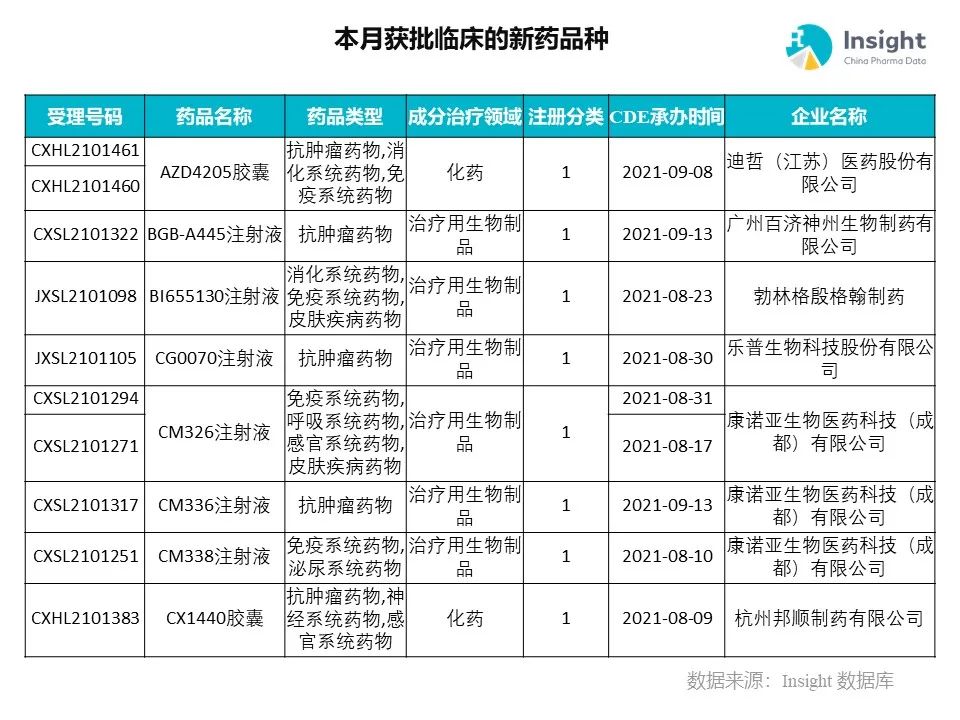
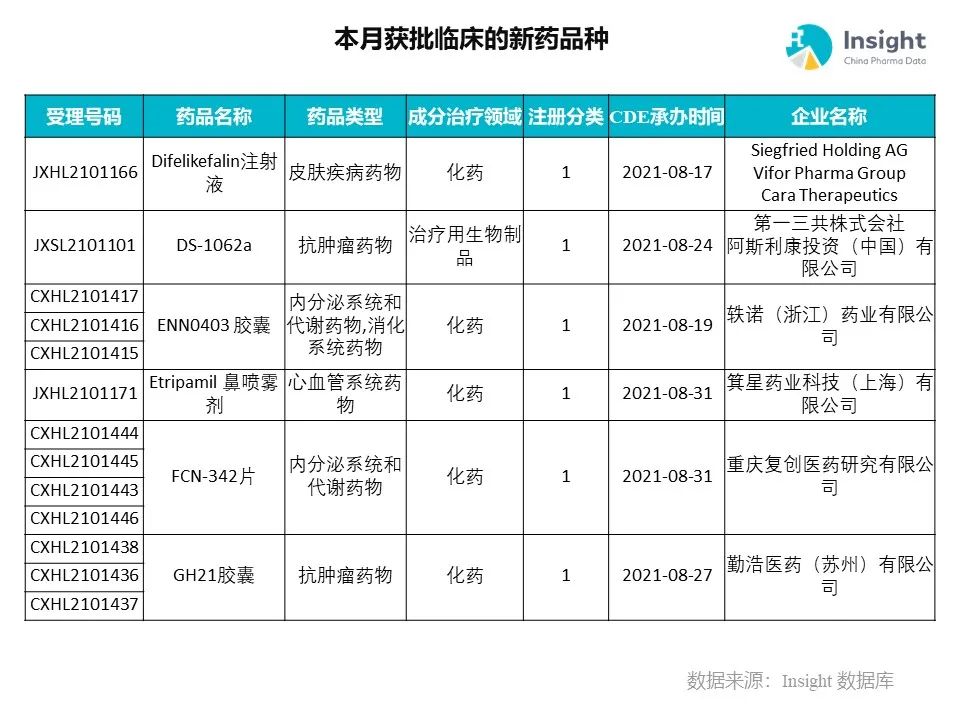
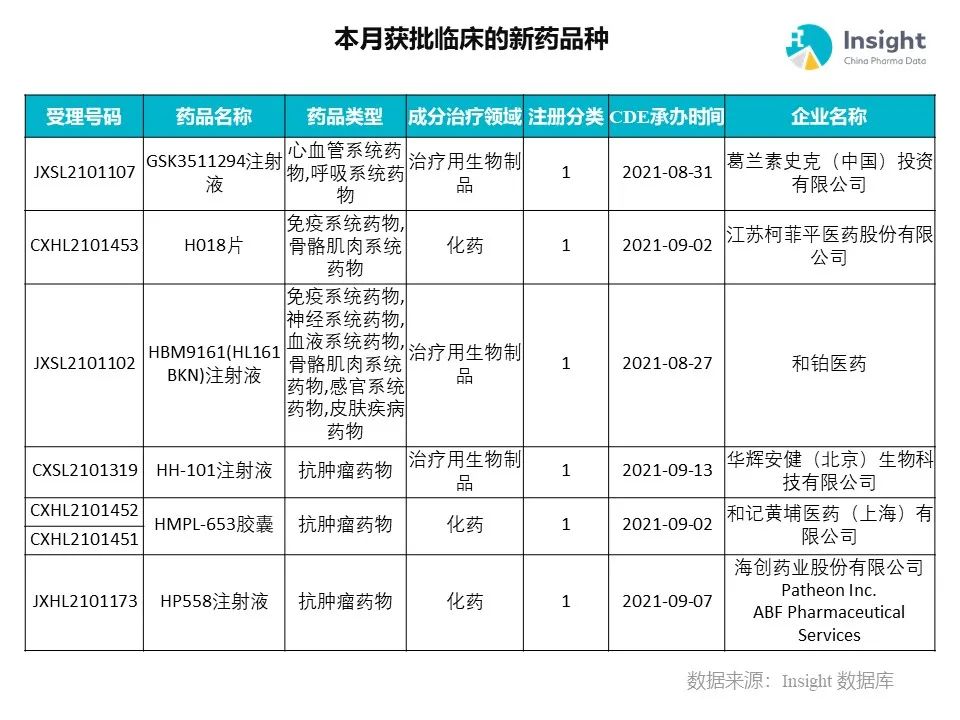
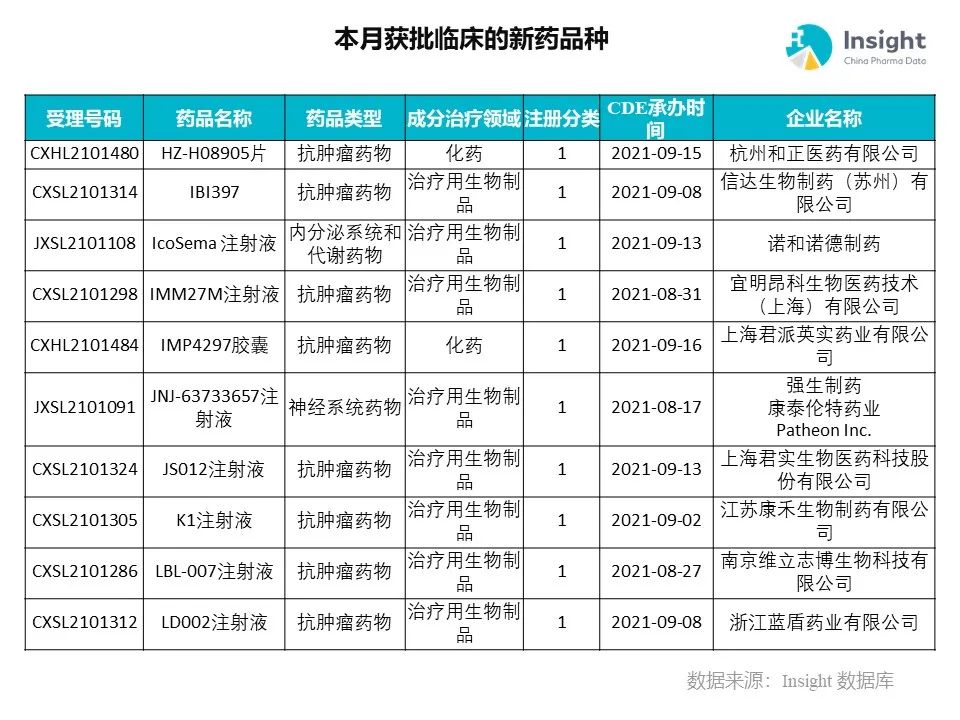
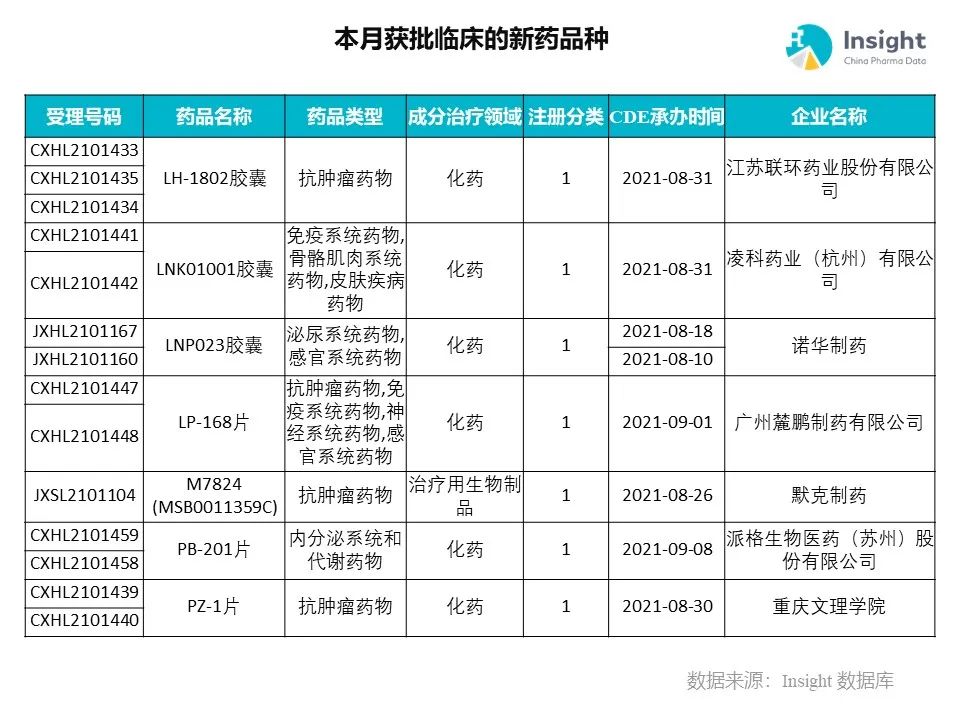
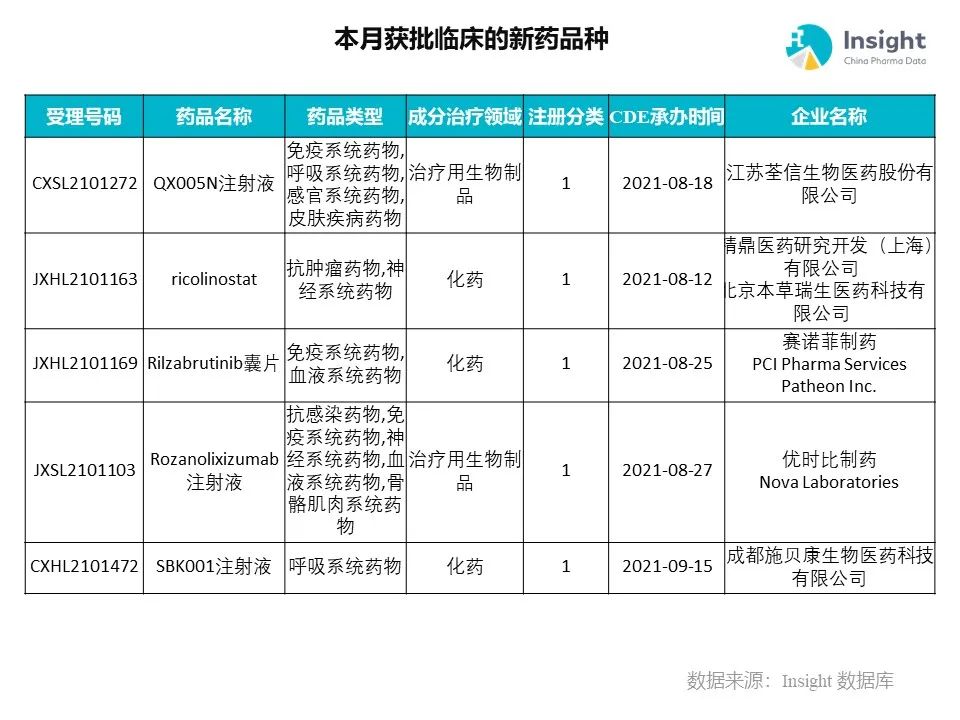
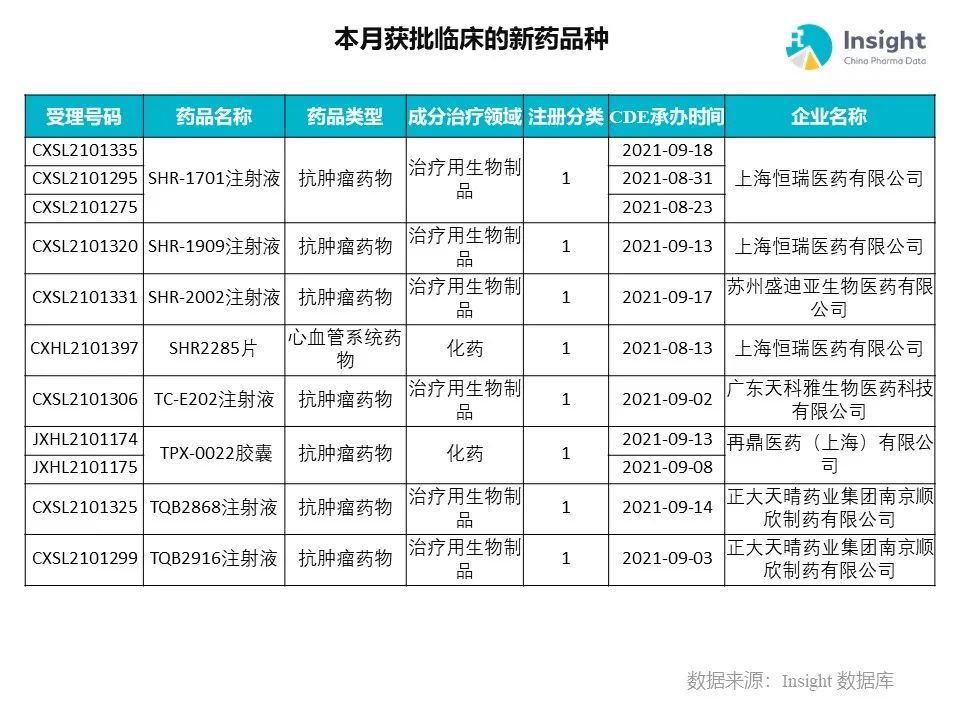
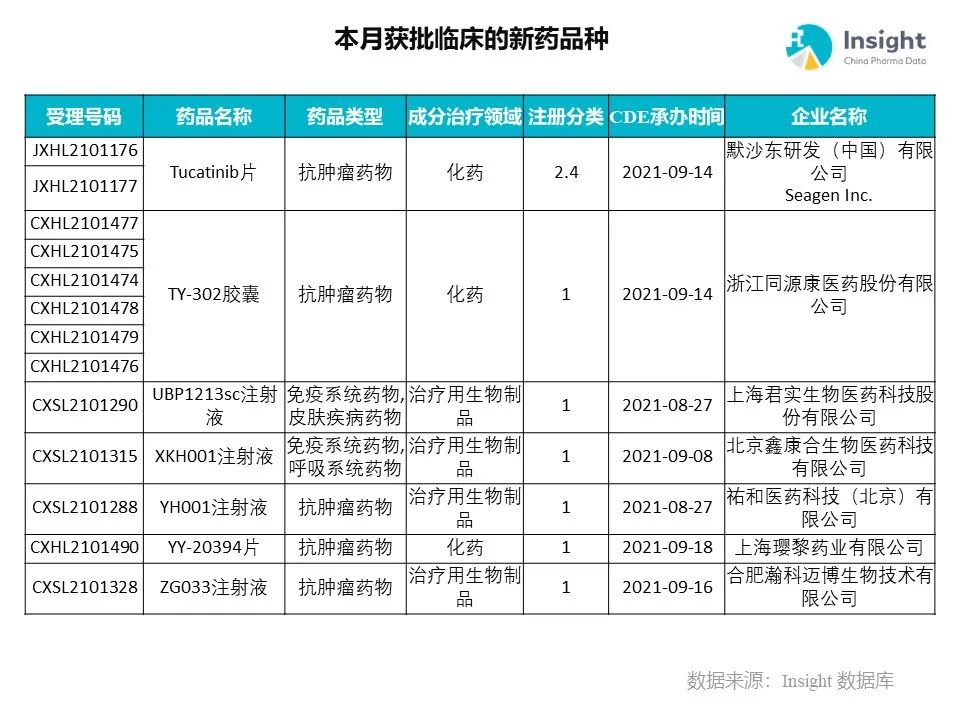
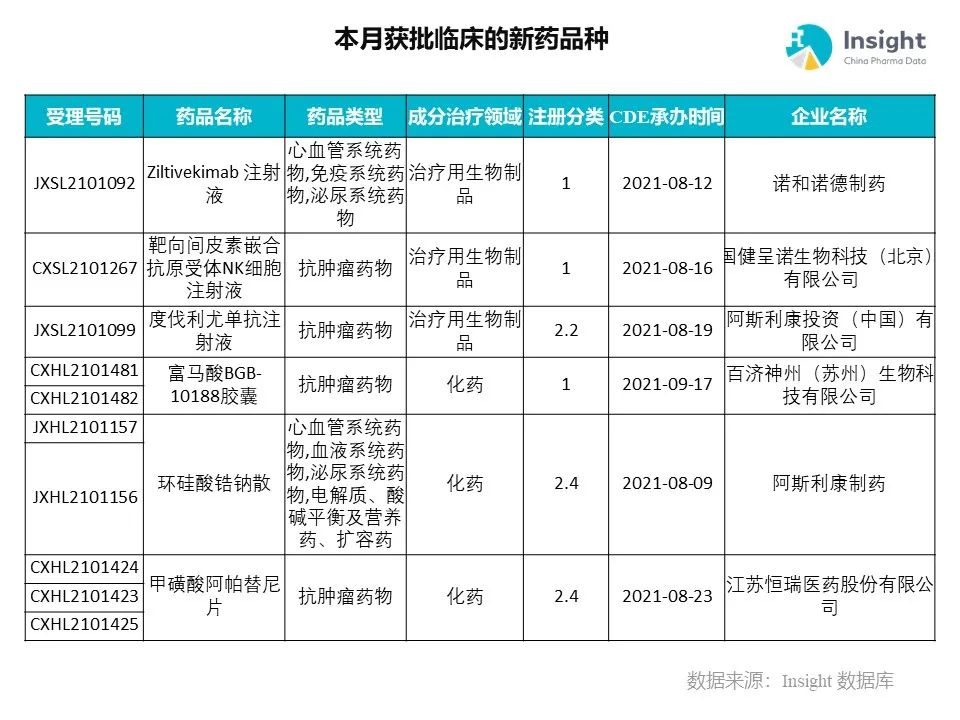
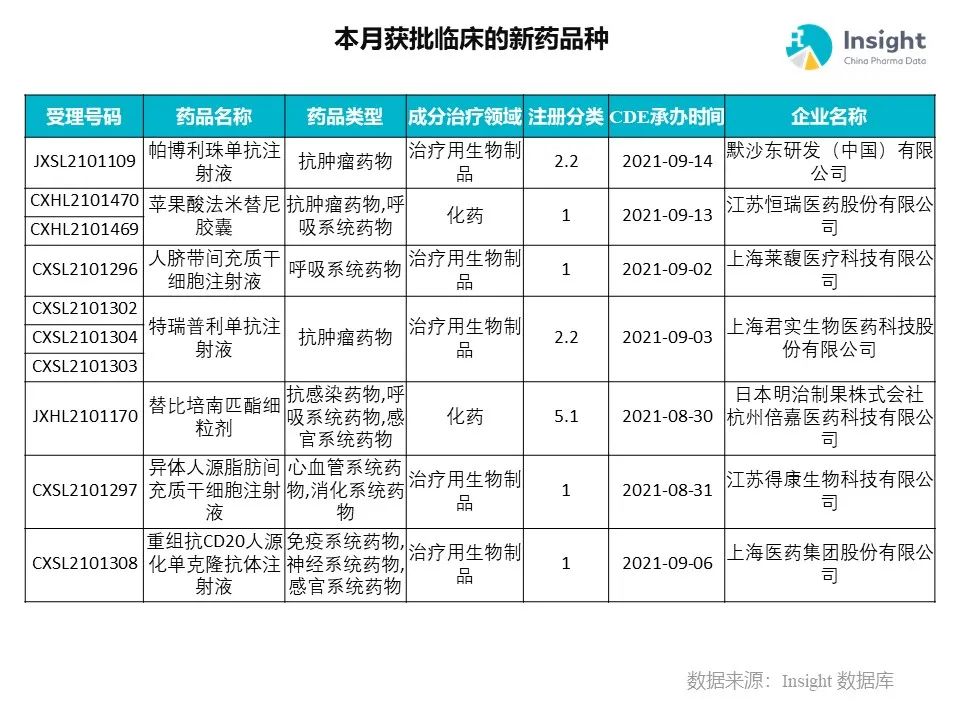
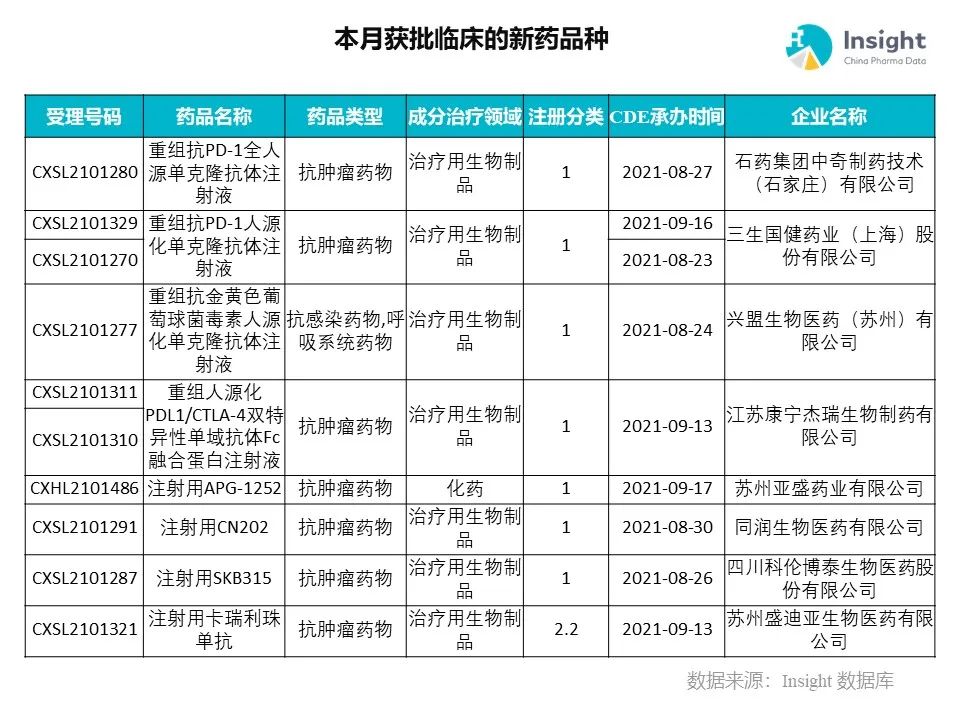
下面是本月获批临床品种的部分重点产品介绍,文章略长,可选择性阅读。

获批临床新药品种介绍
11 月新药获批临床的受理号共 124 个,涉及 86 个品种,部分产品介绍如下。
药品名称:ABM-1310 胶囊
企业名称:璧辰医药
ABM-1310 是一种口服的,具有高选择性、高水溶性以及高血脑屏障渗透性的小分子 BRAF 抑制剂,也是壁辰医药的首个候选药物,在临床前动物模型中显示出血脑屏障渗透方面的独特优势,有望成为恶性肿瘤脑转移的新一代 BRAF 抑制剂。
药品名称:AND019 胶囊
企业名称:安道药业
AND019 具有全新化学结构,是第三代选择性雌激素受体(ER)降解剂(SERDs)。临床前研究表明,它能利用机体自身的蛋白质自降解技术,与癌细胞表面的雌激素受体相结合,从而降低雌激素水平,阻断 ER 信号传导,达到抑制肿瘤细胞增殖的目的。今年 10 月,AND019 已经获得 FDA 批准开展临床试验。此次在中国,这款产品获得的临床试验适应症为:ER+/HER2-乳腺癌。
药品名称:ASC22 注射液
企业名称:歌礼生物
ASC22 注射液是一款可皮下注射的抗 PD-L1 单克隆抗体,具有皮下注射、常温下稳定等优点,歌礼从康宁杰瑞获得其用于所有病毒性疾病治疗的独家权益。本次获批临床的适应症是人类免疫缺陷病毒 (HIV) 感染。
药品名称:ASP9801 注射液
企业名称:安斯泰来
ASP9801 注射液为一种携带表达 IL-7 和 IL-12 的基因的溶瘤病毒,目前正在全球进行 1 期临床试验。溶瘤病毒是一类经过特殊设计的病毒,可选择性在肿瘤细胞内大量复制繁殖,直至癌细胞裂解、死亡。当癌细胞在病毒的感染下破裂死亡时,新生成的病毒颗粒会被释放,进一步感染周围的癌细胞。
药品名称:BGB-A445 注射液
企业名称:百济神州
BGB-A445 为百济神州自主研发的一种定向 OX40 抗原的激动剂抗体,与其它 OX40 抗体相比的差异化主要在于,它不阻断 OX40-OX40L 结合,从而能够保持抗原递呈细胞 OX40L 的信号,并且使天然配体刺激达到 OX40 最大程度激活。此次这款产品获批的临床试验适应症为:晚期实体瘤。
药品名称:CG0070 注射液
企业名称:乐普生物
CG0070 属于溶瘤病毒,是乐普生物从美国 CG Oncology, Inc. 引进的产品,乐普获得其在中国区的产品开发权益和全球供货权益。
药品名称:CM336 注射液
企业名称:康诺亚生物
CM336 注射液是康诺亚国内申报的首款双抗,本次获批临床适应症为:复发或难治性多发性骨髓瘤。其活性成分为重组抗 BCMA 和 CD3 人源化双特异性抗体,通过特异性结合 BCMA 阳性靶细胞和 CD3 阳性 T 细胞,将免疫 T 细胞招募至靶细胞周围,激活 T 细胞,诱导 T 细胞介导的肿瘤细胞杀伤(TDCC)作用杀伤靶细胞。
药品名称:GH21 胶囊
企业名称:勤浩医药
GH21 是勤浩医药自主开发的,具有全球知识产权的小分子 SHP2 抑制剂,本次获批临床的适应症为晚期实体瘤。此前,勤浩医药已将 GH21 中国以外的产品开发和商业化权利授予沪亚生物国际,这项合作涉及金额高达 2.82 亿美元。
药品名称:HH-101 注射液
企业名称:华辉安健
HH-101 是华辉安健研发的具有免疫激活作用的免疫检查点抑制剂,已在临床前动物模型中表现出优异的治疗效果。本次获批临床适应症为:晚期实体瘤。
药品名称:HMPL-653 胶囊
企业名称:和记黄埔
HMPL-653 胶囊是和黄医药自主研发的强效、高选择性小分子 CSF-1R 抑制剂,本月首次在中国获批临床,适应症为晚期恶性实体瘤及腱鞘巨细胞瘤(TGCT)。
药品名称:HP558 注射液
企业名称:海创药业
HP558 注射液为海创药业引进的潜在「first-in-class」在研新药,拟开发用于转移性食管鳞状细胞癌(ESCC)。该药是一款特异性靶向 CD44v6 的抑制剂,已在欧洲完成临床 1 期试验。
药品名称:IcoSema 注射液
企业名称:诺和诺德制药
IcoSema 是长效胰岛素 Icodec 与长效 GLP-1 类似物司美格鲁肽(semaglutide)的组合,目前已在全球开展针对 2 型糖尿病的 3 期临床试验。此次,该产品在中国首次获批临床,适应症为:糖尿病。
药品名称:IMM27M 注射液
企业名称:宜明昂科
宜明昂科的 IMM27M 注射液临床试验申请获批,适应症为晚期实体瘤。IMM27M 是针对 CTLA-4 靶点的 IgG1 抗体。该抗体经过基因工程改造显著增强了抗体依赖性细胞毒性 (ADCC) 活性,可以全面清除肿瘤微环境中的 Treg 细胞。
药品名称:JNJ-63733657 注射液
企业名称:强生制药
强生的 JNJ-63733657 注射液临床试验申请获批,适应症为阿尔茨海默病。JNJ-63733657 由强生旗下杨森公司开发,该药靶向 tau 蛋白中间区域的一个超磷酸化表位。tau 蛋白是神经细胞中和微管结合的可溶性蛋白,病理性 tau 蛋白的沉积和在大脑的扩散,与 AD 患者的认知能力下降有紧密的相关性。
药品名称:LH-1802 胶囊
企业名称:联环药业
LH-1802 是化药 1 类抗肿瘤创新药,拟定适应症为血液瘤或实体瘤。主要作用机制为抑制赖氨酸特异性去甲基化酶 1(Lysinespecific demethylase 1, LSD1),调控组蛋白 2 的甲基化水平。
药品名称:LNK01001 胶囊
企业名称:凌科药业
LNK01001 是凌科药业开发的 1 类新药,本次是该药首次在中国获批临床,拟开发用于治疗类风湿关节炎。这也是凌科药业首个申报临床的药物。
药品名称:LNP023 胶囊
企业名称:诺华制药
LNP023 胶囊获批临床,适应症为原发性 IgA 肾病、早中期年龄相关性黄斑变性。LNP023 是一种口服特异性替代补体途径因子 B 抑制剂,能高效抑制补体替代通路中因子 B,可能在治疗多种替代通路功能异常导致的疾病同时,不影响其它补体通路介导的对微生物入侵的免疫反应,降低患者受到感染的风险。
药品名称:Rilzabrutinib 囊片
企业名称:赛诺菲
Rilzabrutinib 囊片获批临床,适应症为成人免疫性血小板减少症。布鲁顿氏酪氨酸激酶是 B 细胞受体 (BCR) 信号通路的关键组成部分,对各种免疫细胞的发育和功能都很重要,包括 B 淋巴细胞和巨噬细胞。抑制 BTK 可调节与大脑和脊髓神经炎症相关的适应性和先天性免疫细胞。赛诺菲去年 8 月通过收购 Principia 公司获得了包括 rilzabrutinib 在内的三款 BTK 抑制剂。
药品名称:TC-E202 注射液
企业名称:天科雅生物
TC-E202 为工程化分泌抗 PD-1 单抗的 HPV 特异性 TCR-T 细胞,本次获批的是一项 1/2 期临床研究,适应症为:HPV16 阳性既往治疗失败的复发或者转移性宫颈癌。
药品名称:TPX-0022 胶囊
企业名称:再鼎医药
再鼎医药引进的 TPX-0022 胶囊获得两项临床默示许可,拟开发治疗 MET 基因变异的局部晚期或转移性非小细胞肺癌(NSCLC)、胃癌或实体瘤患者。Elzovantinib(TPX-0022)是 Turning Point Therapeutics 开发的一种口服 MET/SRC/CSF1R 抑制剂。2021 年 1 月,再鼎医药以高达 3.61 亿美元获得了该药在大中华区的开发和商业化独家授权。
药品名称:XKH001 注射液
企业名称:鑫康合生物
XKH001 是由鑫康合自主研发、具有全球知识产权的首个 IL-25 单抗。IL-25 又被称为 IL-17E,是 IL-17 家族细胞因子中的一员,主要由上皮细胞和天然免疫细胞产生,当其与受体结合后,会激活 2 型免疫细胞,进而起始、放大并维持 Th2 型免疫应答。研究表明,IL-25 在 2 型炎症疾病组织中的表达过高,与过敏性哮喘,特应性皮炎等炎症疾病密切相关。
药品名称:注射用 APG-1252
企业名称:亚盛药业
APG-1252(pelcitoclax)为亚盛医药自主研发的新型 Bcl-2/Bcl-xL 双靶点抑制剂,采用前药设计来提高其治疗指数、降低细胞通透性和血小板毒性。APG-1252 对 Bcl-2 和 Bcl-xL 具有高度结合亲和力。此前,APG-1252 已经在美国和中国获批开展临床试验,适应症为非小细胞肺癌等实体瘤。此次该产品在中国获批的临床试验适应症为:单药治疗复发或难治性 NHL 及联合西达本胺治疗复发或难治性 PTCL。
药品名称:注射用 SKB315
企业名称:科伦博泰
注射用 SKB315 是公司开发的全新的具有自主知识产权的靶向 Claudin18.2 的 ADC 药物,拟用于治疗晚期实体瘤。
▲以上数据来源于 Insight 申报进度数据库
本报告在每月 11 号左右定期发布,敬请期待。以上品种介绍根据企业公开披露信息整理。

推荐阅读
点击阅读原文
申请试用数据库





 个人中心
个人中心
 我是园区
我是园区




