▎药明康德内容团队编辑
X4 Pharmaceuticals今日宣布,其在研CXCR4拮抗剂mavorixafor,在治疗WHIM综合征患者的关键临床3期试验中获得积极结果。数据分析显示,试验达成主要与关键次要终点。即药物组患者体内中性粒细胞与淋巴细胞的绝对数量维持在具临床意义阈值之上的时间,明显优于安慰剂组患者。X4将针对这些数据,在2023年上半年与美国监管单位讨论关于递交上市申请与商业化的可能。若获批,mavorixafor将有可能成为WHIM综合征患者的首个疗法。

WHIM综合征是一项由于CXCR4/CXCL12通路过度活化,造成白细胞自骨髓移动与迁移至系统循环降低的罕见、遗传性联合免疫缺陷疾病。WHIM综合征患者的中性粒细胞与淋巴细胞数量极低,因此经常出现反复性的感染,并具高风险罹患肺病与部分种类癌症、抗体生产量降低,以及出现因潜伏人乳头状瘤病毒(HPV)感染而造成的难治性疣粒的情形。
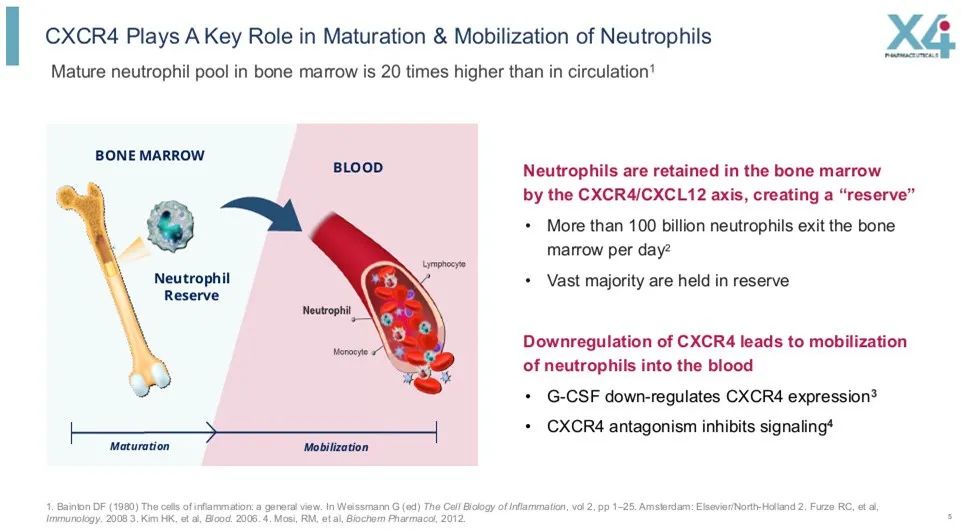
▲CXCR4拮抗剂药理机制(图片来源:参考资料[2])
Mavorixafor是一款在研CXCR4小分子拮抗剂,针对WHIM综合征患者的失能情形所开发。Mavorixafor曾获得美国FDA授予突破性疗法认定、快速通道资格、罕见儿科疾病认定与孤儿药资格,用于治疗WHIM综合征。
这次所公布的4WHIM试验是一项双盲的全球多中心关键3期试验,共有31位经遗传检测确认的12岁以上WHIM综合征患者入组,随机分配接受每天一次口服400 mg的mavorixafor(n=14)或安慰剂(n=17)治疗,疗程共52周。
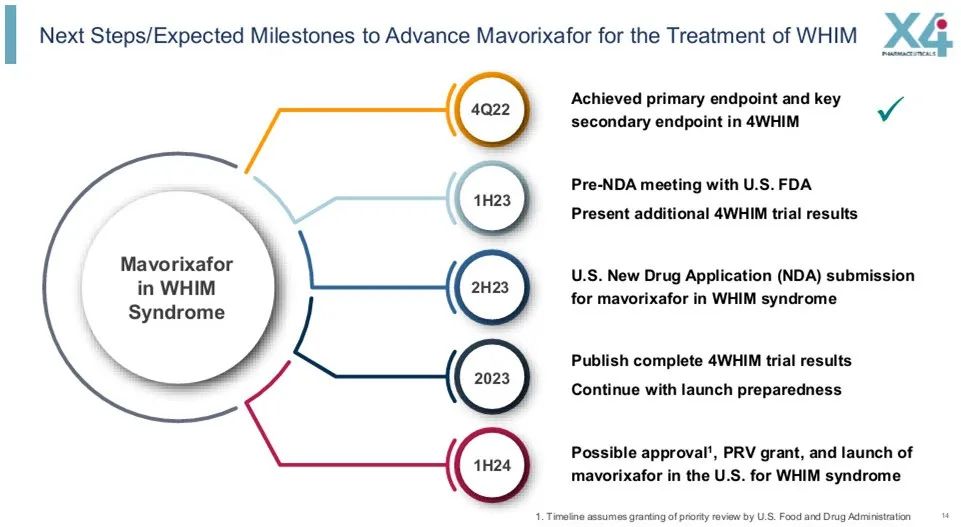
▲Mavorixafor治疗WHIM综合征的预期里程碑(图片来源:参考资料[2])
数据分析显示,试验达成主要终点,即mavorixafor组患者在为期52周的临床试验的4个不同时间点上,TATANC数值在临床与统计上优于安慰剂组。TATANC为患者在24小时内维持中性粒细胞数(ANC)大于500个细胞/微升的时间(ANC小于这一数值意味着患有严重性中性粒细胞减少症)。Mavorixafor与安慰剂组患者的平均TATANC分别为15.04小时与2.75小时(P<0.0001)。
试验亦达成关键次要终点,即mavorixafor组患者的TATALC数值,在临床与统计上优于安慰剂组。TATALC为患者维持绝对淋巴细胞数(ALC)大于淋巴细胞减少症(lymphopenia)临床阈值(即1000个细胞/微升)的时间。Mavorixafor与安慰剂组患者的平均TATALC分别为15.80小时与4.55小时(P<0.0001)。
安全性方面,mavorixafor的耐受性良好,没有观察到治疗相关严重不良反应,亦无因安全性问题中断试验的情形。
“Mavorixafor是首个持续改善患者严重慢性中性粒细胞减少与淋巴细胞减少的在研疗法,这是WHIM综合征最明显的两项病征,”X4的临时首席医学官Murray Stewart博士说道,“在达成这些关键试验终点之后,我们现在计划于2023年上半年与美国监管单位讨论,为递交mavorixafor上市申请做准备。”
药明康德为全球生物医药行业提供一体化、端到端的新药研发和生产服务,服务范围涵盖化学药研发和生产、生物学研究、临床前测试和临床试验研发、细胞及基因疗法研发、测试和生产等领域。如您有相关业务需求,欢迎点击下方图片填写具体信息。
▲如您有任何业务需求,请长按扫描上方二维码,或点击文末“阅读原文/Read more”,即可访问业务对接平台,填写业务需求信息

▲欲了解更多前沿技术在生物医药产业中的应用,请长按扫描上方二维码,即可访问“药明直播间”,观看相关话题的直播讨论与精彩回放
参考资料:
[1] X4 Pharmaceuticals Announces Positive Top-Line Results from 4WHIM Global, Pivotal Phase 3 Trial of Once-Daily, Oral Mavorixafor in WHIM Syndrome. Retrieved November 30, 2022 from https://investors.x4pharma.com/news-releases/news-release-details/x4-pharmaceuticals-announces-positive-top-line-results-4whim
[2] Current Corporate Presentation. Retrieved November 30, 2022 from https://investors.x4pharma.com/static-files/eae36b57-f69f-4fba-ad24-eb1012be88b2
免责声明:药明康德内容团队专注介绍全球生物医药健康研究进展。本文仅作信息交流之目的,文中观点不代表药明康德立场,亦不代表药明康德支持或反对文中观点。本文也不是治疗方案推荐。如需获得治疗方案指导,请前往正规医院就诊。
版权说明:本文来自药明康德内容团队,欢迎个人转发至朋友圈,谢绝媒体或机构未经授权以任何形式转载至其他平台。转载授权请在「药明康德」微信公众号回复“转载”,获取转载须知。


分享,点赞,在看,聚焦全球生物医药健康创新



 个人中心
个人中心
 我是园区
我是园区




