点击关注我们
有观点,有态度
这是医业观察公众号的第1205-4期文章
2021年10月1日,美国Merck(默沙东)宣布,其和Ridgeback发开的口服抗病毒药Molnupiravir对于治疗COVID-19安全有效。因为结果超出预期的好,该研究提前终止。
(满屏的药丸,都在讲Merck的故事)
3期临床试验主要结果
本次公布的3期MOVe-OUT临床试验中期分析,为多中心RCT研究,本次共评估了775名受试者的数据。
受试者均实验室确诊的轻度至中度COVID-19,至少有一个与病重相关的危险因素(如肥胖、年龄>60岁、糖尿病和心脏病),并且症状出现在随机化前5天内。
该研究在全球招募受试者,其中拉美人群占55%、欧洲人群占23%、非洲人群占15%。
主要疗效指标是随机分组后29天内住院/或病死的百分比。
在评估的病例中,Delta、Gamma和Mu等突变株占到感染者的80%。
主要结果:
服用Molnupiravir患者中7.3%(28/385)人在29天住院或死亡;安慰剂组为14.1%(53/377);由此,Molnupiravir将病重/病死率降低了50%,p=0.0012。
在29天的观察期内,共有8名受试者死亡,均在安慰剂组。
Molnupiravir治疗组与安慰剂组出现的任何不良事件(35% vs. 40%)差异均无统计学意义,包括药物相关不良事件(治疗组12% vs. 安慰剂组11%)。与安慰剂组有3.4%因不良事件而停止治疗相比,明显多于Molnupiravir治疗组的1.3%。
本3期临床试验原计划招募1550名患者,由于中期分析展示了非常积极的结果,在和FDA沟通后停止招募及进一步试验。
目前Merck在向FDA申请紧急使用授权(EUA)。
Molnupiravir成功的基础
临床前研究
2期临床试验结果
进一步的分子作用机制证实
2021年8月11日,马普研究所在Nature SME发表了一篇很好的文章,报道了潜在的高效抗病毒药Molnupiravir的分子作用机制。
这项研究介绍了Molnupiravir诱导病毒RNA复制发生突变的机制。Molnupiravir的活性形式是β-D-N4-羟基胞苷(NHC)-三磷酸,病毒的RdRp会错误使用NHC-三磷酸,而不使用三磷酸胞苷或三磷酸尿苷作为催化底物。
NHC会使病毒RNA复制掺入大量A和G,从而导致RNA产物发生突变。包含诱变产物的RdRp-RNA复合物的结构分析表明,NHC可以与 RdRp活性中心的G或A形成稳定的碱基对,这解释了该药物如何逃避校对并合成突变的RNA。
这种两步诱变机制可能适用于各种病毒聚合酶,因此Molnupiravir可具有广谱抗RNA病毒的活性。
后续影响
另外一个抗病毒药物,曾经的“人民的希望”,吉利德公司研发的瑞德西韦也是针剂,所以无法在门诊早期使用、而只能用于住院的重症患者;并且,越来越多证据显示,瑞德西韦治疗重症COVID-19患者无效。
吉利德公司也曾尝试研发瑞德西韦吸入剂,但2021年7月30日,该公司宣布停止瑞德西韦吸入剂的临床试验,目前早期治疗COVID-19口服抗病毒制剂的希望,就落在了Molnupiravir身上。
默沙东的抗病毒药物Molnupiravir终期临床试验展现出了远超市场意料的积极结果,极大地满足了目前最重要、而远为解决的临床问题。
正如,美国FDA前局长Scott Gottlieb说:
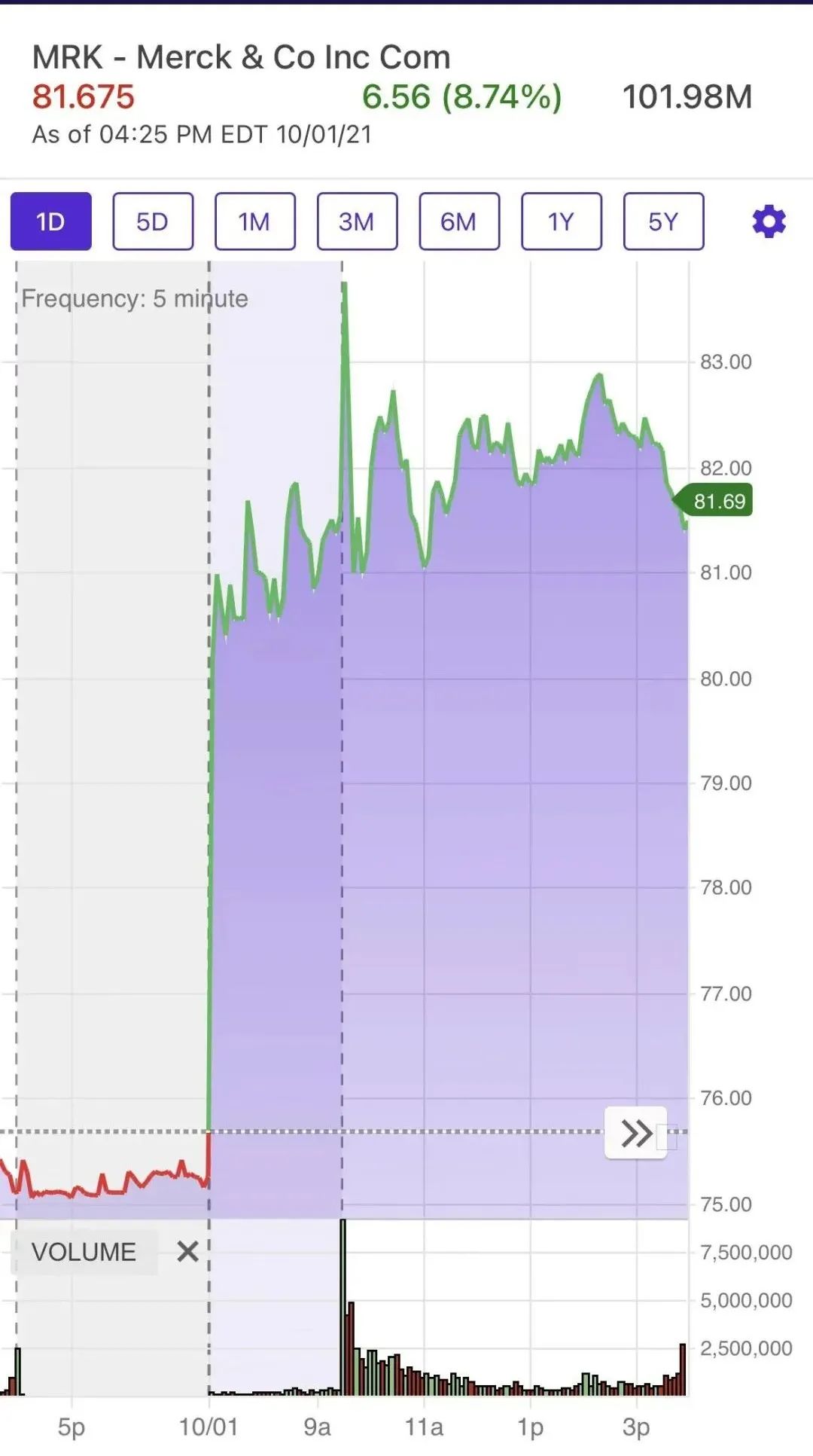
(Merck) |
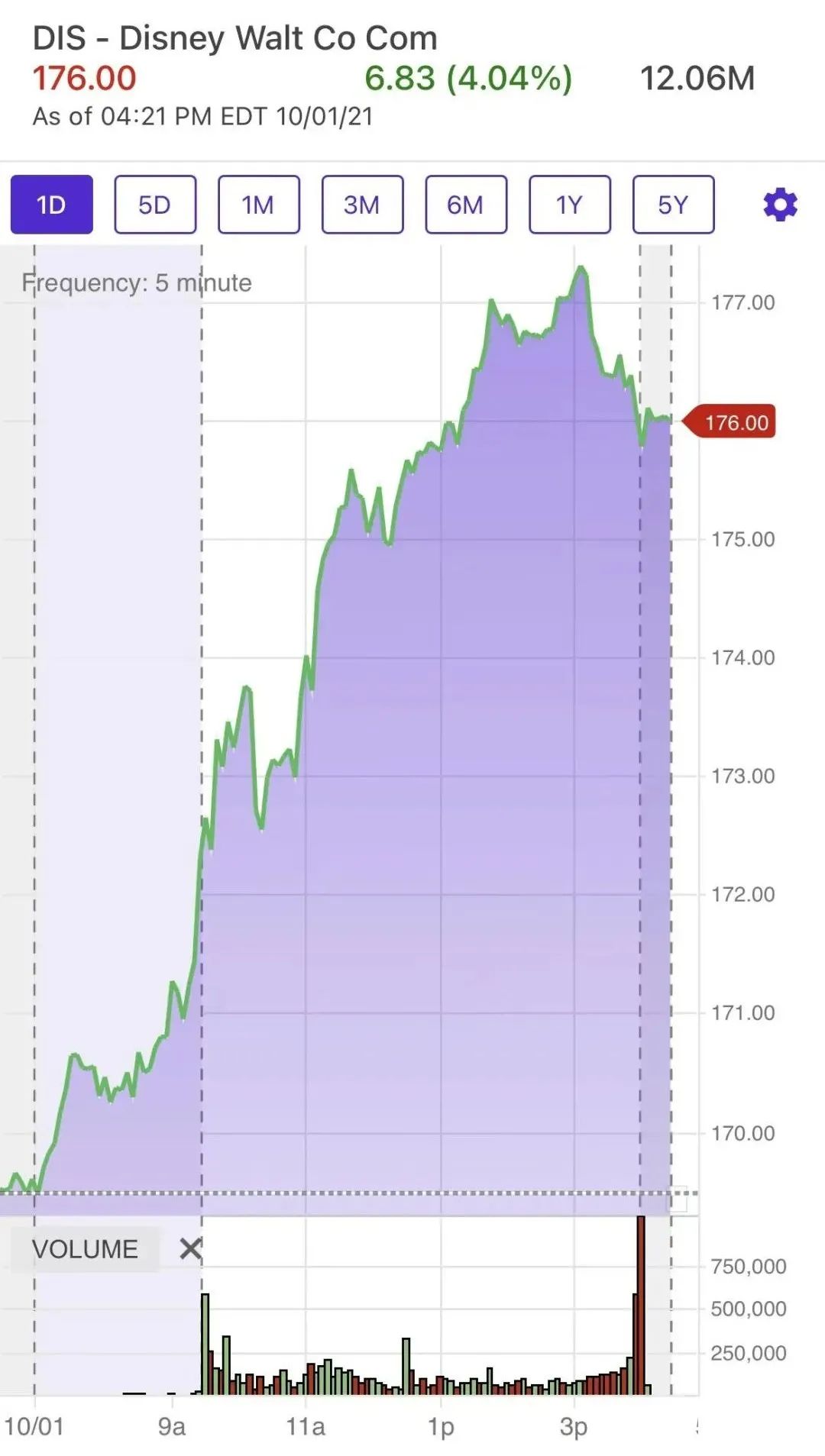
(迪士尼) |
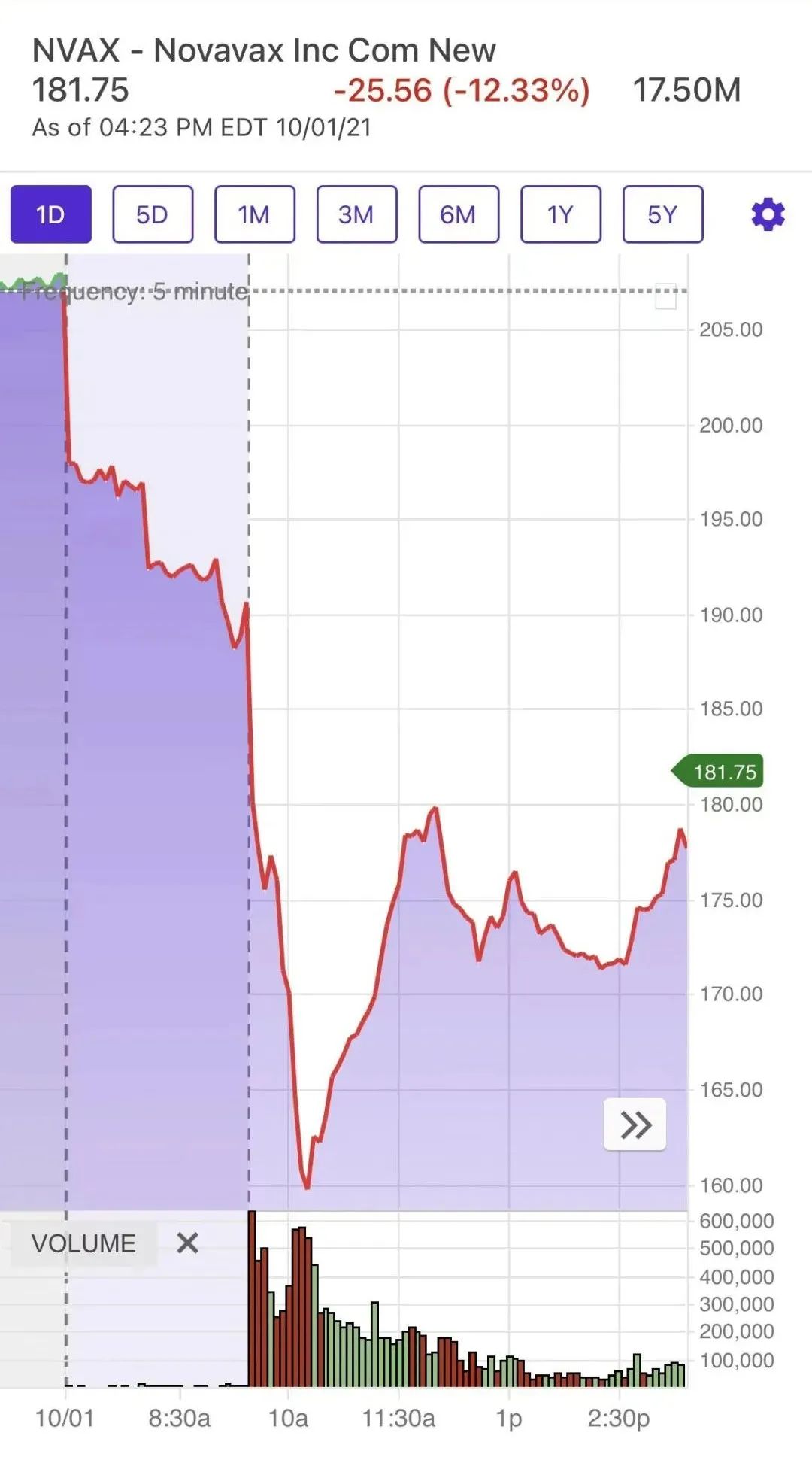 (疫苗公司Novavax) (疫苗公司Novavax) |
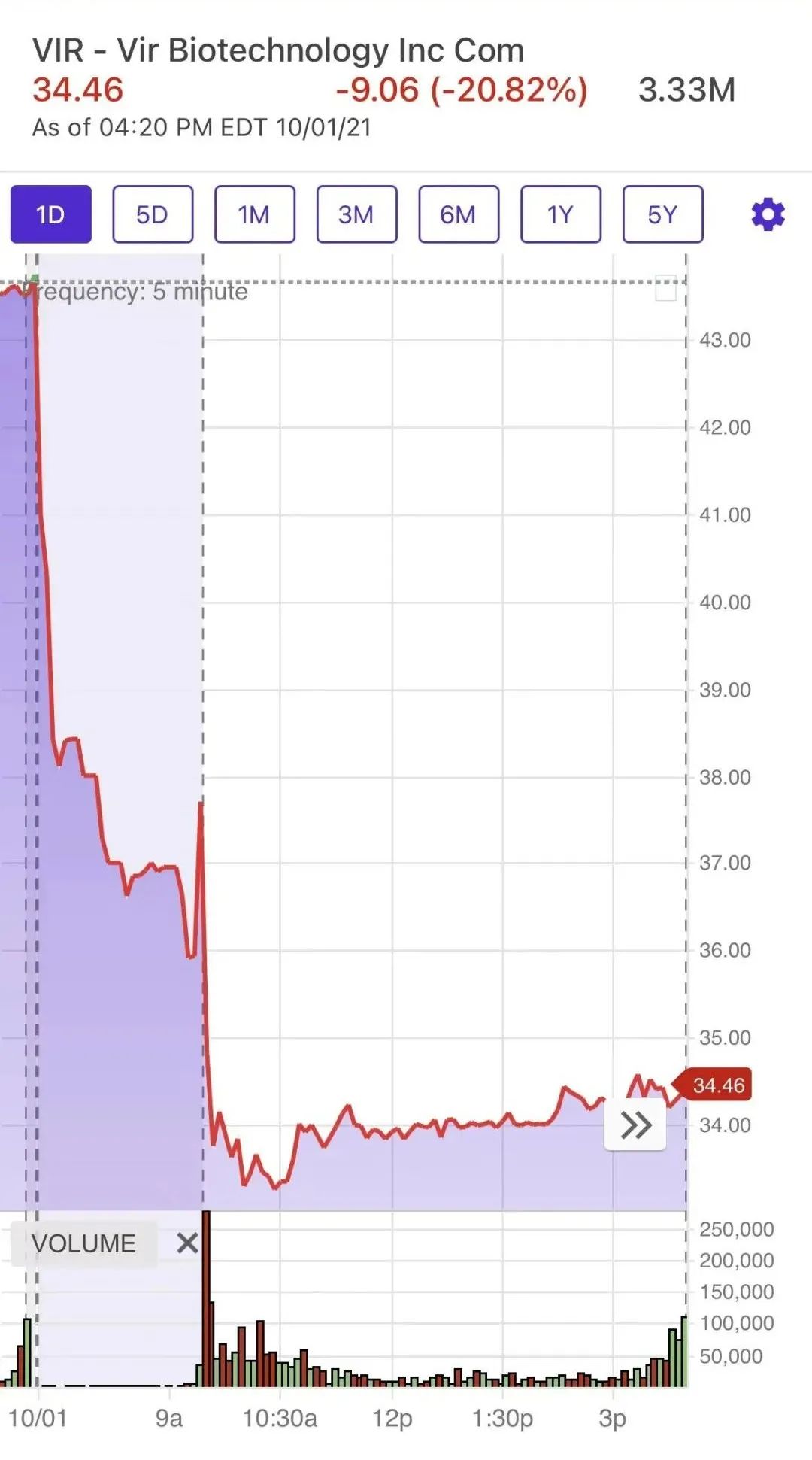
(单抗公司Vir) |
(Merck的“药丸”,疫苗和单抗公司的“要完”?)
但抗病毒药物作为感染后使用的治疗方案,实际上无法替代疫苗作为感染前使用的预防手段。即,人类暂时还离不开疫苗,接种疫苗仍然是预防感染COVID-19的基础。也由此,疫苗公司的股价在大幅下挫后,逐渐恢复。
但口服抗病毒药物显然会替代部分抗病毒单克隆抗体的使用。
不过,也需要看到,目前的口服抗病毒药物只能降低50%的重症/病死率。即经过口服抗病毒药物治疗后的感染组,仍有7.3%出现重症/病死,仍不能满足人类所需。
这意味着,寻找更有效的抗病毒药物,以及抗病毒药物联合单抗治疗,仍是治疗COVID-19的需要。

The End
文章仅代表作者本人观点,与医业观察立场无关。文章图片均来源于网络,如有侵权,请联系作者删除,欢迎联系小编。 @今日话题
欢迎点击关注公众号

喜欢就点个赞和在看吧!



 个人中心
个人中心
 我是园区
我是园区