您还不是认证园区!
赶快前去认证园区吧!
6 月 25 日,Insight 数据库显示,安进的 AMG890(Olpasiran)在国内首次启动了 1 期临床。Olpasiran 是一款靶向 Lp(a) 的小干扰 RNA (siRNA),目前正开发用于动脉粥样硬化性心血管疾病(ASCVD)患者,以降低心血管事件风险。
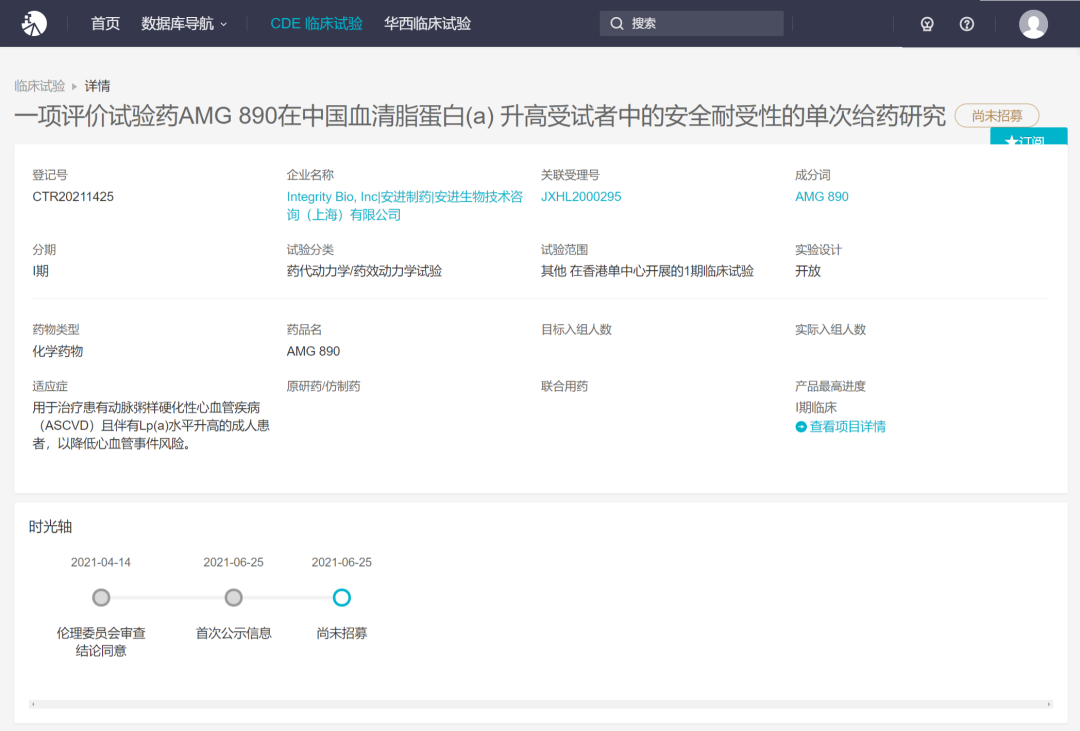
来自 Insight 数据库(http://db.dxy.cn/v5/home/)
AMG890 是安进于 2016 年 9 月与 Arrowhead 公司达成合作而获得的一款针对 Lp(a) 的 siRNA 疗法,已获得 FDA 的快速通道认定,正处于临床 2 期阶段。Lp(a) 即脂蛋白(a),是心肌梗塞和其他动脉粥样硬化事件的危险因素之一。目前全球范围内尚无可降低心脑血管事件的 Lp(a) 靶向药物获批上市。
在 2020 AHA 会议上,AMG890 公布了首次人体试验结果。结果显示,AMG890 安全性及耐受性良好,可显著降低 Lp(a) ,在剂量 ≥ 9mg 时观察到其降低 Lp(a) 的中位值 > 90%;同时 AMG890 疗效持续时间长,在 ≥9 mg 剂量组疗效可持续 3 ~ 6 个月,有望实现每季度或半年一次给药。

来自 2020 AHA
根据 Insight 数据库,安进最初于 2020 年 11 月首次在国内递交临床试验申请,2021 年获批临床。该药是一款潜在的重磅品种,据奥本海默在一份报告中表示,olpasiran 有潜力推动安进的长期增长,预计 2030 年销售额将达到 15 亿美元。
推荐阅读
诚心合作,非诚勿扰
投稿:微信 insightxb;
PR 稿对接:请加微信 insightxb





 个人中心
个人中心
 我是园区
我是园区




