写意报告丨氟来居上——浅谈氟唑帕利的研发历程
收藏
关键词:
研发
资讯来源:同写意 + 订阅账号
发布时间:
2021-11-24

▲ 同写意专业策划,数百位大咖齐聚广州,设医药领袖峰会、主旨论坛以及 11 场专业主题论坛,敬请期待!
应同写意邀请,恒瑞医药临床研发肿瘤副总经理张晓静在“
首届中国(苏州)太湖医药创新大会
”上做了《氟来居上——浅谈氟唑帕利的研发历程》的报告,本文系根据报告内容整理,并经报告人确认。
PARP抑制剂的演变历史可以回溯到1922年,哥伦比亚大学的遗传学家Calvin Bridges在做果蝇杂交时发现,同时具有两个特定基因突变的果蝇不能存活,其中任何一个基因单独突变却不会给果蝇带来致命伤害。
20多年后的1946年,同在哥伦比亚大学工作的Theodore Dobzhansky再次发现类似现象,并将其正式命名为“合成致死”。直到1997年,Stephen Friend发表文章,大胆提出“合成致死”理念可用于抗癌药物开发。
PARP因其潜在的“合成致死”效应逐渐受到重视,多家创新药企致力于PARP抑制剂的研发。17年后,随着奥拉帕利在2014年首次上市,“合成致死”终于从理论成为现实。至今为止,已有6个PARP抑制剂上市。如今,PARP抑制剂的临床研发正在卵巢癌、乳腺癌以及前列腺癌等各大瘤种和各类人群中加速进行。
氟唑帕利是恒瑞具有自主知识产权的新型PARP抑制剂,于2020年底附条件获批第一个适应症
(单药治疗既往经过二线及以上化疗的伴有BRCA1/2致病性或疑似致病性突变的复发性卵巢癌)
成功上市,第二个适应症
(用于铂敏感复发性上皮性卵巢癌、输卵管癌或原发性腹膜癌成人患者在含铂化疗达到完全缓解或部分缓解后的维持治疗)
于2021年年中获得批准。氟唑帕利的开发从立项到最后获批用了约十年时间。
氟唑帕利于2015年开始首次人体研究,2017年启动关键临床研究,2019年递交首个单臂关键临床的上市申请,2020年附条件获批上市,2021年激活的完全批准,得益于精心布局得临床研发策略。在2018年、2019年开展首个单臂关键临床研究时,两项Ⅲ期临床研究也已经在同步积极推进。
因此在氟唑帕利首个适应症的单臂关键临床上市申请的审评过程中,才能够滚动递交首个Ⅲ期临床研究结果,为监管部门审阅及评估氟唑帕利的有效性和安全性提供了更多的数据支持。
氟唑帕利在临床研究阶段展示出的确定的疗效,取决于该产品立项之初采用的氟取代策略。该策略帮助产品在维护稳定性的同时,极大增加了活性。在首次人体研究设计中探索了从10mg QD到200mg BID共11个剂量组,同时探索了QD和BID的给药方式。最终基于安全性数据,PK数据及初步的疗效数据确定150mg BID为最大耐受剂量及继续开发的RP2D。
由于卵巢癌目前的3年复发率高达70%,5年生存率,尤其是铂敏感复发到最后的铂耐药,一直到5年生存率只有不到30%。因此,如何减少复发、延长无化疗间期已成为卵巢癌治疗亟待解决的问题。
基于该人群显著的临床治疗需求,以及氟唑帕利首次人体研究79例患者中47例晚期标准治疗后卵巢癌患者中的显著疗效信号,选定BRCA突变的精准人群,开展后线治疗的单臂关键性研究,希望与历史数据对照得到比较好的数据,尝试获批上市。关键研究是一项单臂、开放、多中心研究。
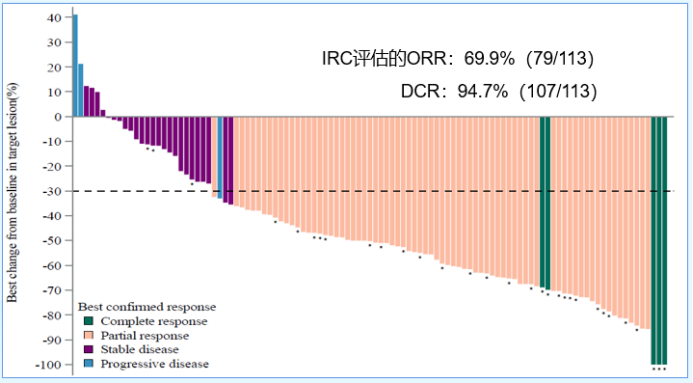
共入组113例既往经过二线及以上化疗的伴有BRCA1/2致病性或疑似致病性突变的复发性卵巢癌患者,接受氟唑帕利150mg bid连续给药,28天为一个给药周期,用药直至疾病进展、毒性无法耐受或撤知情,主要终点为IRC评估的ORR,次要终点包括DOR,PFS,OS,安全性等。
最终研究结果显示,IRC评估的ORR达到69.9%,DCR达到94.7%,DOR也是比较长的,各终点均达到了方案预设,甚至比预设的还要更好。
由于确定了通过单臂关键临床研究数据申请附条件上市申请的计划,考虑到获批后后续还需要开展验证性临床研究,从CDP
(临床研发计划)
的角度,后续计划了两项III期随机对照研究来支持上市申请的完全批准。
氟唑帕利的第一个Ⅲ期临床研究是在铂敏感复发性卵巢癌患者再次接受含铂化疗以后CR/PR的患者中,观察氟唑帕利维持治疗对比安慰剂治疗的有效性和安全性。研究主要终点为BIRC基于RECIST1.1标准评估的PFS。
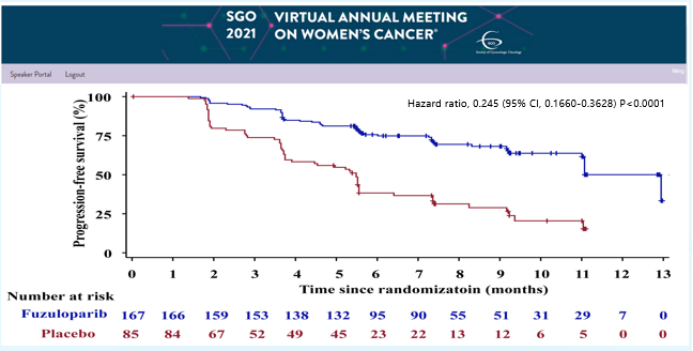
从关键时间节点可以看到,这项研究推进还是比较快的。2019年4月第一例患者入组,7个月内完成全部入组,经过半年时间等待足够的事件数后,进行期中分析,并于2020年9月递交Pre-NDA。
2021年3月,主要研究者中国医学科学院肿瘤医院的吴令英教授在SGO大会上对本研究的结果进行了口头报告。经BIRC评估,氟唑帕利维持治疗组的PFS与安慰剂组相比Hazard ration是0.245,远超出方案预设。
在开展氟唑帕利单药Ⅰ期和Ⅲ期临床研究的同时,同期在进行的一项氟唑帕利联合阿帕替尼在卵巢癌和三阴性乳腺癌中的探索性研究也取得了令人鼓舞的初步结果。
根据前期氟唑帕利单药以及与阿帕替尼联合的探索性研究结果,在氟唑帕利的第二项III期随机对照研究-晚期卵巢癌一线维持治疗中设计了三臂研究,在对照组基础上,设计了氟唑帕利单药治疗组和氟唑帕利联合阿帕替尼的联合治疗组,试图回答在PARP抑制剂单药维持的基础上,联合VEGFRi是否为更优的维持治疗基于前期探索性研究结果中获得的信息,随机比例设计为2:2:1,尽量减少暴露在安慰剂中的患者数量。目前,这项晚期卵巢癌一线维持治疗的Ⅲ期研究还在进行中,希望未来有一个好结果。
根据前期探索性研究结果,氟唑帕利目前除了在卵巢癌的布局外,正在开展一项在BRCA突变、HER2-乳腺癌中的Ⅲ期研究和一项氟唑帕利联合阿比特龙在去势抵抗性前列腺癌中的国际多中心Ⅲ期研究。
另外,氟唑帕利在其他多个瘤种也有一些探索,包括联合阿比特龙、联合阿帕替尼、联合贝伐单抗、在胰腺癌中联合化疗、在小细胞肺癌中联合替莫唑胺和免疫的治疗等,这些探索性研究都在进行中。希望通过更多的探索和验证性研究的数据,未来氟唑帕利能够带给更多的肿瘤患者新的治疗机会。
【首届中国(苏州)太湖医药创新大会】
相关报道文章推荐




 药选址
药选址



