信达生物公布 GLP-1R/GCGR 双激动剂 Ib 期临床数据
收藏
关键词:
临床期临床信达临床数据生物GLP
资讯来源:Insight数据库 + 订阅账号
发布时间:
2021-12-07
2021 年 12 月 7 日,信达生物宣布胰高血糖素样肽-1 受体(glucagon-like peptide-1 receptor, GLP-1R)/胰高血糖素受体(glucagon receptor, GCGR)双激动剂 IBI362(LY3305677)在中国 2 型糖尿病患者中的多次给药、剂量递增 Ib 期临床研究结果被 2021 年国际糖尿病联盟大会(IDF 2021)接收为大会摘要并以线上壁报的形式发表。
该研究是一项随机、双盲、安慰剂对照 Ib 期临床研究,旨在于血糖控制不佳的中国 2 型糖尿病患者中评估 IBI362 多次剂量递增给药的安全性、耐受性和药代/药效动力学特征,同时设立度拉糖肽作为开放标签的活性对照组。
研究分 3 个队列,每个队列入组 14 例受试者,按 8:4:2 随机分别接受 IBI362、安慰剂或 1.5 mg 度拉糖肽,每周一次皮下注射给药,连续给药 12 周。IBI362 或安慰剂以 1.0-2.0-3.0 mg(队列 1),1.5-3.0-4.5 mg(队列 2)或 2.0-4.0-6.0 mg(队列 3)的剂量滴定方案给药,每个剂量水平给药 4 周。
研究结果显示,IBI362 耐受性良好,最常报告的治疗期不良事件为食欲减退和胃肠道相关不良事件,且绝大部分事件为一过性且程度较轻。第 12 周时,队列 1、2 和 3 中接受 IBI362 治疗的受试者的糖化血红蛋白水平较基线变化的平均值分别为−1.46%,−2.23% 和−1.66%,度拉糖肽组为−1.98%。
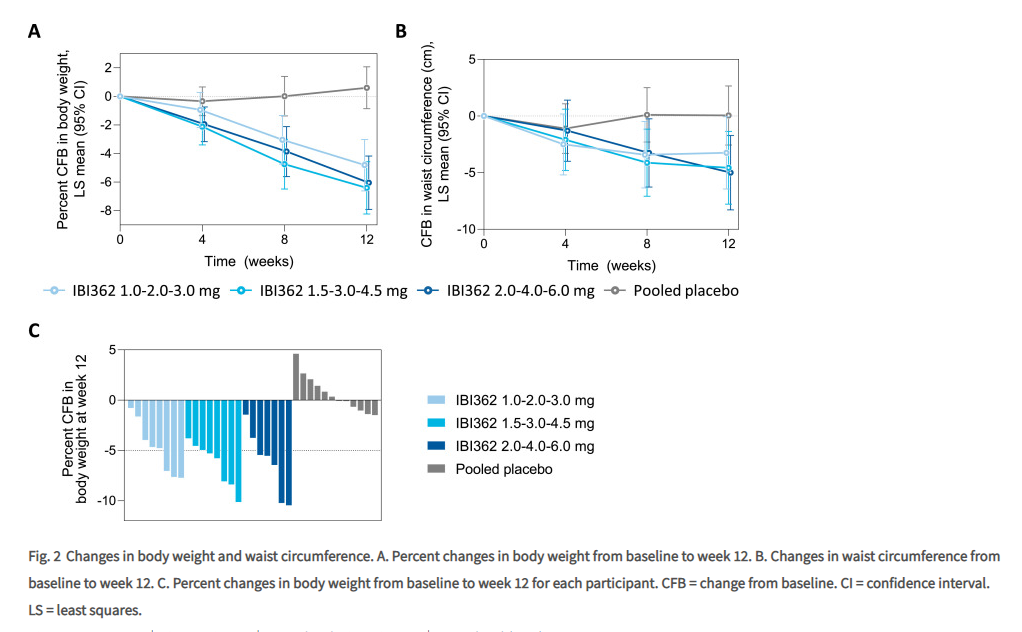
考虑到样本量有限带来的变异可能对结果产生影响,剔除第 12 周时每个给药组糖化血红蛋白水平较基线变化的极大值和极小值后,队列 1、2 和 3 中接受 IBI362 治疗的受试者的糖化血红蛋白水平较基线变化的校正平均值分别为−1.46%,−2.28% 和−1.87%,度拉糖肽组为−1.46%。同时,队列 1、2 和 3 中接受 IBI362 治疗的受试者第 12 周时的平均体重较基线分别下降 0.9%、5.0% 和 5.4%,度拉糖肽组下降 0.9%。接受 IBI362 治疗的受试者的腰围、体重指数、血压和血脂等指标也观察到有不同程度改善,其整体趋势与 IBI362 1b 期减重研究的趋势类似 [1]。
DOI: https://doi.org/10.1016/j.eclinm.2021.101088
IBI362(LY3305677)是信达生物制药与礼来制药共同推进的一款胃泌酸调节素创新化合物(OXM3),是具有同类最优潜力的 GLP-1R 和 GCGR 双激动剂。
作为一种与哺乳动物胃泌酸调节素类似的长效合成肽,IBI362 利用脂肪酰基侧链延长作用时间,允许每周给药一次。
IBI362 的作用被认为是通过 GLP-1R 和 GCGR 的结合和激活介导的,与 OXM 具有相似作用机制,因此预计其可以改善葡萄糖耐量并减轻体重。除了 GLP-1R 激动剂具有的促进胰岛素分泌、降低血糖和减轻体重等作用外,IBI362 还可能通过 GCGR 的激活具有增加能量消耗和改善肝脏脂肪代谢等效应。通过开发同时激动多个与代谢相关的靶点来治疗代谢性疾病是目前国际上新药研发最新的趋势。
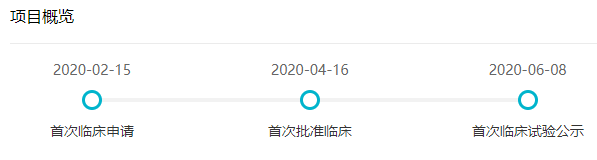
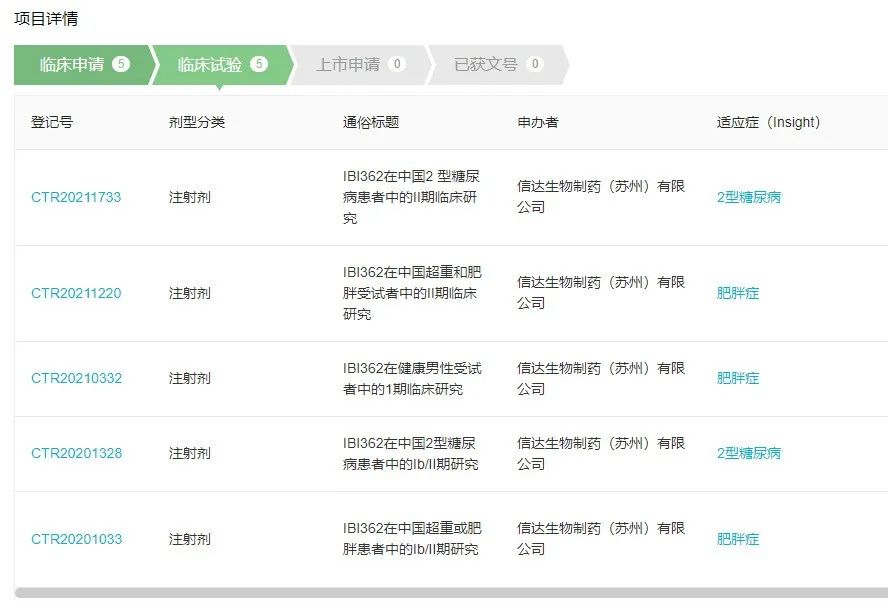
根据 Insight 数据库,IBI362 最早在今年 2 月申报临床,目前已经启动 5 项临床试验,针对肥胖症和 2 型糖尿病,最高处于临床 2 期。
来自:Insight 数据库(http://db.dxy.cn/v5/home/)
免责声明:
本文仅作信息分享,不代表 Insight 立场和观点,也不作治疗方案推荐和介绍。如有需求,请咨询和联系正规医疗机构。
投稿:微信 insightxb;邮箱 insight@dxy.cn
 药选址
药选址

