▎药明康德内容团队报道
今日
,中国国家药监局(NMPA)官网公示,武田(Takeda)公司的
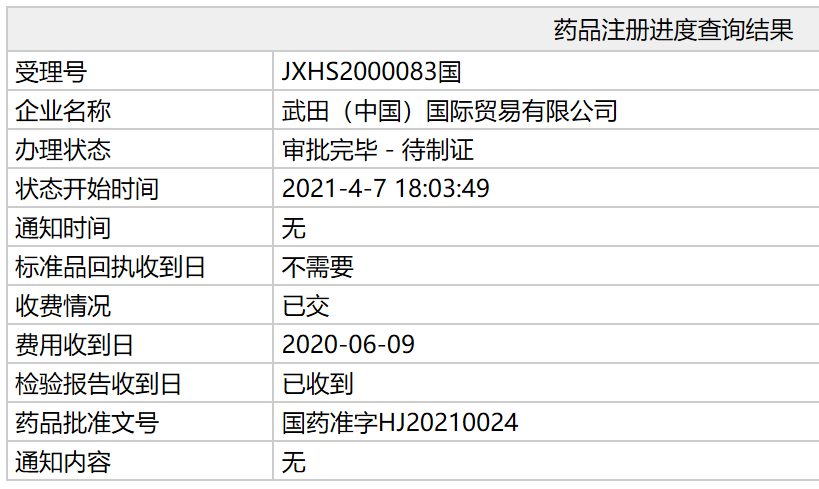
醋酸艾替班特(icatibant,英文商品名:Firazyr)注射液上市申请审评审批状态已更新为:审批完毕-待制证,国药准字HJ20210024。这意味着该药已正式在中国获批,适应症
为遗传性血管水肿(HAE)急性发作。
此前,该药物已在中国被纳入临床急需境外新药名单,且被纳入优先审评。
艾替班特是一款选择性缓激肽B2受体拮抗剂
,
由武田旗下Shire公司研发
。
它通过抑制与遗传
性血管水肿的栓塞局部肿胀、炎症、疼痛症状有关的缓激肽的影响,从而治疗急性
遗传性血管
水
肿
的栓塞局部肿胀。
艾替班特最早于2008年在欧盟获得批准,用于治疗成人HAE的急性发作。2011年,艾替班特获得美国FDA批准上市,用于18岁及以上成年人的HAE急性发作治疗。2017年,它在欧盟获得扩大适应症人群的批准,用于2岁及以上儿童和青少年HAE患者。
在中国,根据NMPA药品审评中心(CDE)官网信息,武田公司于2020年6月在中国递交醋酸艾替班特注射液上市申请并获受理。
同年10月,
艾替班特的新药上市申请纳入优先审评,适应症为——用于治疗成人、青少年和≥2岁儿童的遗传性血管性水肿急性发作。

截图来源:CDE官网
遗传性血管水肿是一种罕见的遗传性疾病,主要表现为反复发生的皮肤、呼吸道和内脏器官肿胀,当水肿发生于气道时,可致喉水肿,如果抢救不及时,可窒息死亡。当水肿发生于胃肠道,会类似急腹症的表现,常误诊为阑尾炎、急性胰腺炎等,导致急诊进行剖腹探查。此病不仅有可能危及生命,也给患者和家属带来了沉重的经济和精神负担。
2018年,中国发布《第一批罕见病目录》,遗传性血管水肿被收录其中。公开数据显示,当前中国约2.8万HAE患者,患病率约为1/10000~1/50000。针对HAE,目前中国仅有一款预防类药物,尚无有效药物用于急性发作期的治疗。
此次武田「醋酸艾替班特注射液」正式在中国获批上市,意味着该类患者迎来一款急性治疗药物。
版权说明:本文来自药明康德内容团队,欢迎个人转发至朋友圈,谢绝媒体或机构未经授权以任何形式转载至其他平台。转载授权请在「医药观澜」微信公众号留言联系我们。
欢迎扫码关注“
医药观澜
”微信公众号,了解更多中国医药创新动态。

注:本文旨在介绍医药健康研究进展,不是治疗方案推荐。如需获得治疗方案指导,请前往正规医院就诊。
参考资料:
[1]中国国家药监局药品注册进度查询. Retrieved Apr 7,2021, from http://sq.nmpa.gov.cn/datasearch_nmpa/schedule/search.jsp?tableId=43&tableName=TABLE43&columnName=COLUMN464,COLUMN475&title1=药品注册进度查询
[2]中国国家药监局药品审评中心. Retrieve
d Apr 7,2021, from http://www.cde.org.cn/news.do?method=changePage&pageName=service&frameStr=3
[3]FDA Approves Shire's Firazyr (icatibant injection) for Acute Attacks of Hereditary Angioedema (HAE). Retrieved August 25, 2011, from https://www.drugs.com/newdrugs/fda-approves-shire-s-firazyr-icatibant-acute-attacks-hereditary-angioedema-hae-2824.html









 个人中心
个人中心
 我是园区
我是园区




