速递!科越医药双靶点补体药物在中国获批2期临床
收藏
关键词:
药期临床临床药物靶点获批医药
资讯来源:医药观澜 + 订阅账号
发布时间:
2022-10-17
▎药明康德内容团队报道
今日(10月17日) ,科越医药宣布,其开发的双靶点补体生物制剂KP104的2期临床试验申请已获得中国国家药品监督管理局(NMPA)批准,拟开发用于治疗阵发性睡眠性血红蛋白尿症(PNH)。
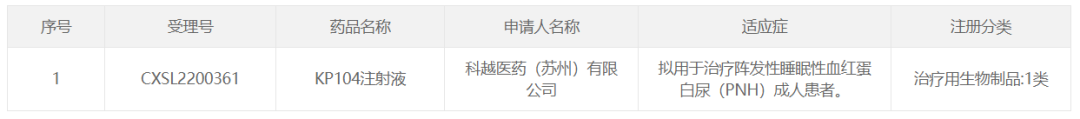 截图来源:CDE官网
截图来源:CDE官网
阵发性睡眠性血红蛋白尿症是一种罕见的危及生命的血液系统疾病,它的特征是体内产生异常红细胞,并被机体认定为"异物",从而导致补体系统过度激活和红细胞破坏。PNH患者可能出现贫血、血栓和骨髓功能受损。目前针对PNH的补体靶向治疗是通过抑制单个补体靶点来实现的。虽然这些药物可减轻溶血,但最近的研究表明,同时抑制补体旁路途径和末端途径的治疗可能会更有效地改善患者的病情。
科越医药致力于研发补体靶向疗法治疗免疫介导疾病。根据科越医药新闻稿介绍,KP104是该公司开发的一种创新型双靶点补体生物制剂,它能特异性地同时抑制补体旁路和末端途径,从而有效地、协同性地抑制补体,以更加有选择性的精准治疗补体介导的疾病。此外,该药还被设计成具有延长的半衰期和效能,其配方可用于静脉注射和皮下给药。

临床1期首次人体试验(FIH)SYNERGY-1的数据已证明,KP104 具有双靶点作用机制。今年早些时候,美国FDA已授予KP104治疗PNH的孤儿药资格。科越医药将在今年晚些时候举行的2022年美国肾脏学会年会上公布已经完成的临床1期试验的完整数据。
目前,KP104正进入针对多个适应症的2期临床试验,包括IgA肾病(IgAN)、C3肾小球病(C3G)、继发于系统性红斑狼疮的血栓性微血管病(SLE-TMA)和阵发性睡眠性血红蛋白尿症 。2期临床试验将在全球范围内进行,包括美国、中国、澳大利亚和韩国。而本次在中国获批的正是一项2期临床试验,旨在中国阵发性睡眠性血红蛋白尿症患者中评估KP104的有效性、安全性、耐受性、药代动力学(PK)和药效学(PD)。
科越医药中国和亚洲研发与运营总裁闫慧女士说,本次临床的获批是科越医药加速推动KP104这新一代补体药物用于治疗像PNH这样的补体介导疾病道路上的一个重要里程碑。KP104被设计用于同时阻断两个关键的补体靶点,对于那些需要更有效治疗手段的PNH患者来说,公司相信KP104将是一个突破性的治疗选择。
[1]科越医药宣布KP104用于治疗阵发性睡眠性血红蛋白尿症(PNH)的II期临床试验申请已获得中国国家药品监督管理局批准. Retrieved Oct 17, 2022. From https://www.prnasia.com/story/379159-1.shtml
本文由药明康德内容团队根据公开资料整理编辑,欢迎个人转发至朋友圈。转发授权请在「医药观澜」微信公众号留言联系我们。其他合作需求,请联系wuxi_media@wuxiapptec.com。
免责声明:药明康德内容团队专注介绍全球生物医药健康研究进展。本文仅作信息交流之目的,文中观点不代表药明康德立场,亦不代表药明康德支持或反对文中观点。本文也不是治疗方案推荐。如需获得治疗方案指导,请前往正规医院就诊。
 截图来源:CDE官网
截图来源:CDE官网




 个人中心
个人中心
 我是园区
我是园区




