国内外多团队首创!Science子刊发表「无免疫抑制」胰岛移植,授权公司计划推进临床试验
收藏
关键词:
移植临床Science免疫
资讯来源:DeepTech深科技 + 订阅账号
发布时间:
2022-05-23
1 型糖尿病(T1D),也称胰岛素依赖型糖尿病。
作为一种自体免疫性疾病,该疾病主要是由于免疫介导的胰腺 β 细胞破坏从而导致胰岛素缺乏。
1 型糖尿病患者可以选择长期注射胰岛素的方式来调节血糖,或是通过移植捐赠者的胰岛 β 细胞从而自行产生胰岛素。不过,接受移植的患者必须终生服用免疫抑制药物以防止移植细胞被排斥。而这又将导致其免疫系统被削弱,这类患者群体往往更易面临免疫系统疾病与癌症风险。
该技术将供体胰岛与一种新型免疫调控蛋白同时移植以促进免疫耐受,并用生物工程技术将其固化在由大网膜构建的微环境中。基于在非人灵长类动物(猕猴)体内进行的胰岛移植结果表明,其在患糖尿病的非人类灵长类动物中能够稳健地控制血糖并建立起局部耐受。
这种局部免疫调节策略在成功控制 1 型糖尿病的同时也无需长期服用抗免疫排斥药物,
表现出巨大的转化潜力。
同样值得注意的是,
目前 SA-FasL 微凝胶免疫耐受平台的技术许可已授权给美国初创公司iTolerance,该公司以 “无需终生免疫抑制的再生医学” 为目标,合成的生物材料 SA-FasL 微凝胶 —— iTOL-100 正是该公司的首推产品。
iTolerance 公司方指出:“
这种基于生物材料的策略提供了现成的免疫调节能力,无需对供体胰岛细胞进行修饰,从而增加了其临床相关性和潜在适用性的广度。
”
无需长期服用抗免疫排斥药物
“免疫系统是一种严格的防御机制,它能够在充满感染的环境中保证个体的生命健康”,该研究通讯作者之一,来自 MU 医学院的儿童健康、分子微生物学和免疫学教授 Haval Shirwan 介绍道,“当免疫系统错误地将胰腺中产生胰岛素的细胞识别为感染并破坏它们时,就会出现 1 型糖尿病。”
过去二十年间,Shirwan 及其同事 Esma Yolcu 专注于研究细胞凋亡(apoptosis)机制。此前,已有诸多研究是针对于细胞凋亡与癌症、自体免疫性疾病之间进行探究,例如通过激发癌细胞的细胞凋亡,以达到治疗的目的。
也称为细胞程序性死亡,是指人体自身为维持内环境稳定,由基因控制的细胞自主、有序的死亡,是一种主动的细胞死亡过程。
现在,研究团队
利用细胞凋亡机制来破坏相关的免疫细胞,
从而抵抗移植排斥反应,而该过程将通过一种被附着在供体胰岛细胞表面的 FasL 分子来实现。
研究团队首先设计了聚乙二醇(PEG)的合成微凝胶,使用链霉亲和素(SA)与 FasL 组成嵌合蛋白,然后将呈递 SA-FasL 的微凝胶与未修饰的同种异体胰岛共同移植到糖尿病小鼠体内,利用生物工程技术将其固化在由大网膜构建的微环境中。
▲图丨通过合成微凝胶于局部环境中呈现 SA-FasL(来源:Science Advances)
“当 FasL 分子与位于个体自身免疫 T 细胞上的 Fas 分子相互作用时,就会引发细胞凋亡,从而导致免疫细胞死亡”,该研究的第一作者之一 Yolcu 介绍,“因此,该技术目的是生产一种新型 FasL 并将其呈现在移植的胰岛细胞或微凝胶上,以防止被‘流氓’免疫细胞排斥。在胰岛细胞被移植后,‘流氓’免疫细胞会来到移植物上进行破坏,但其与 FasL 结合后将会死亡。”
试验的手术部分由哈佛大学麻省总医院的胰岛移植专家雷骥及其团队完成。雷骥认为,与目前将供体移植到肝脏的临床方法相比,将胰岛移植到大网膜具备优势:“
如果遇到并发症,可以将其移除。因此,大网膜是移植治疗糖尿病的更安全位置,可能特别适合干细胞衍生的 β 细胞和生物工程细胞。
”
在移植结束后,受体动物仅使用单一抗排斥药物(雷帕霉素)治疗三个月。
结果证实,在接受 SA-FasL 微凝胶胰岛移植的猴子中,它们的空腹胰岛素水平与患上 T1D 之前水平相同且存活超过六个月。当研究人员移除移植物时,动物的血糖水平再次升高。此外,它们的肝肾功能也正常,并且没有移植排斥的迹象。
这些结果充分表明,
该试验方案不仅实现了移植术后受体无需终生服用抗免疫排斥药物,且成功实现了对于 T1D 的长期控制。
目前,该研究小组正在计划开展人体临床试验。Shirwan 补充道,
其目标是有一天能够为医院提供一种 “现成的疗法”。
“无免疫抑制的再生医学” 准备进入产业化
显而易见的是,生物材料可以在实验室内集中制造并被运送到任何地方,这一优势为 “现成疗法” 提供了可行性。
来自佐治亚理工学院的联合研究负责人 Andrés J. García 教授介绍:“在之前的工作中,我们发现这种生物材料是一种有效的免疫调节分子,能够让受体永久接受移植细胞。而现在,该策略已被证明对非人类灵长类动物有效。”
▲图丨简便的生产及输注方式(来源:iTolerance)
“我们的策略是使用先进的合成材料,以可控、持续的方式在移植物微环境中实现局部呈现 FasL,” 该公司对此介绍道,“SA-FasL 对于表达 Fas 的细胞具有强大的凋亡活性,然而,对于胰岛细胞表面进行化学修饰以呈现 SA-FasL 则大大限制了其应用。”
在此之前,混合供体嵌合体是实现临床耐受的唯一方案,但仅限于少数患者,并且这种疗法仍然具有引发急性或慢性移植物抗宿主病的风险。现在,
这种基于生物材料的策略提供了现成的免疫调节能力,为更广泛的临床应用提供了可能。
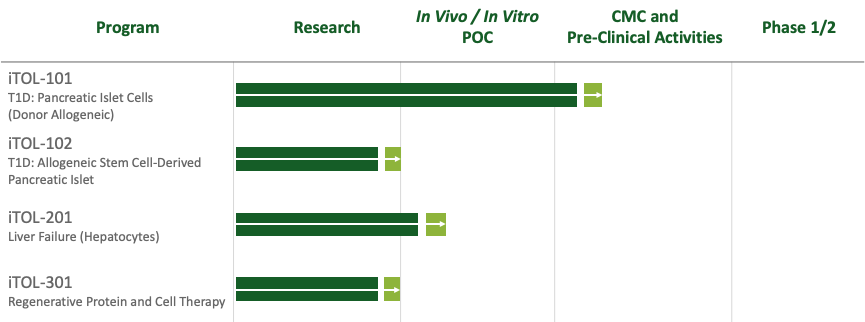
凭借专有的技术平台,iTolerance 于今年 3 月完成了 1710 万美元的可转换票据融资。并且,除了 iTOL-100 项目之外,该公司的另一个基于干细胞衍生的主导项目也在同步推进中。
总的来说,该项研究成果是迄今为止在围手术期使用单一种类免疫诱导方案,并无需长期使用抗排斥药物,且成功控制血糖的首个案例。
其创新之处不仅在于使用合成生物材料呈现 FasL 分子这一方式,还包括使用受体猴大网膜作为移植胰岛细胞的载体,大网膜经过生物工程技术改造形成了容纳胰岛细胞和 SA-FasL 微凝胶的局部微环境(网膜袋)。
相关研究人员指出:“在这个移植微环境内,微囊泡上的 FasL 和 T 细胞膜上的 Fas 结合后,启动了 T 细胞的程序性死亡,阻断了 T 细胞对异体胰岛细胞的攻击。与此同时,移植在胰岛细胞周围的 FasL 还吸引了更多的 Treg,进一步抑制了局部免疫反应。”
不过,该试验也存在一定局限性。据相关研究人员介绍,本次试验中所采用的非人灵长类动物糖尿病模型是在注射化学药物链脲佐菌素(Streptozocin)后引发,而人类 1 型糖尿病则是自身免疫性疾病。因此还需要在临床阶段开展进一步的论证工作。








 药选址
药选址








