
3 月 10 日,万春医药撤回了与恒瑞合作的「注射用普那布林浓溶液」国内上市申请,NMPA 也发布了相应通知件。
此前在 2021 年末,普那布林的上市批准也曾收到 FDA 发出的 CRL,建议补充临床试验后再重新递交。



截图来自:NMPA 官网
普那布林曾经历过高光时刻。FDA 和 NMPA 都授予其突破性疗法认定,后在 2021 年 5 月,万春医药在中美同步提交普那布林的新药上市申请,联用 G-CSF 用于成年非随性恶性肿瘤患者化疗导致的中性粒细胞减少症(CIN),并被两国监管机构纳入优先审评审批。2021 年 8 月,普那布林二/三线治疗 NSCLC 的全球多中心 III 期临床达到主要终点,企业表示拟在 2022 上半年申报上市。
普那布林优先审评信息

截图来自:CDE 官网
CIN 适应症的上市申请基于 III 期试验 PROTECTIVE-2(即 106 研究;登记号:NCT03294577)的积极数据。在这项临床中,普那布林与 G-CSF 培非格司亭联合治疗显著减少了化疗引起的重度中性粒细胞减少(CIN)的发生率,在主要和所有关键次要终点方面均都达到优效性。
具体而言,在联合治疗组中,第一周期 4 级 CIN 的预防率超过 100%;联合治疗组中未发生 4 级 CIN 的患者百分比为 31.5%,而对照组这一数值为 13.6%,具有统计学显著差异(CI:17.90 [7.13,28.66],p=0.0015)。
从适应症来看,普那布林与拥有庞大抗肿瘤管线和 G-CSF 培非格司亭的恒瑞相当相配。2021 年 8 月 26 日,恒瑞宣布与万春达成合作,获得普那布林产品的大中华区权益,以与自身产品线产品联用互补。这项交易包括 2 亿元首付款、7 亿元潜在研发里程碑和 4 亿元潜在商业化里程碑,恒瑞还同步宣称将对万春进行 1 亿元股权投资。这笔交易令万春股价大涨,将万春医药的股价带到了历史最高点。
普那布林权益流转历史
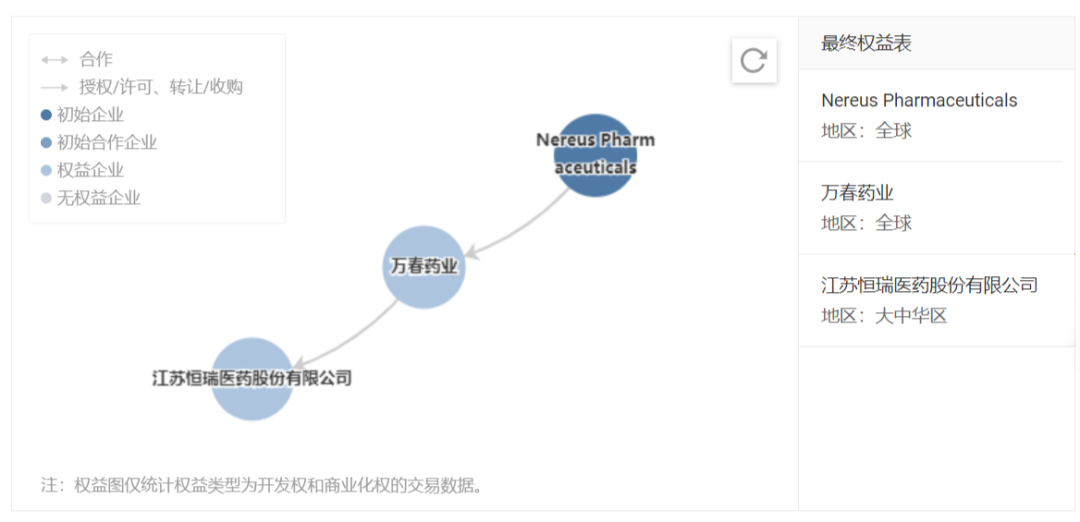
截图来自:Insight 数据库网页版(http://db.dxy.cn/v5/home/)
然而好景不长,至暗时刻很快来到。在 2021 年 9 月份的 ESMO 大会中,万春药业公布了普那布林用于 NSCLC 的 3 期临床数据,股价却不升反跌 30%,外界质疑声音主要集中在其试验设计的合理性方面。
万春医药的普那布林 3 期临床开始时 PD-1/L1 单抗在相应地区尚未上市或尚未成为标准疗法,因此三期临床中经 PD-1/PD-L1 治疗比例不高(20% 左右);同时其美国入组人数比例偏低,导致市场对于普那布林能否获得 FDA 批准仍持观望态度。
这些因素在如今看起来十分熟悉,和信迪利单抗等国产创新药在出海路上遭遇的困境十分相似。同年 12 月 1 日,万春医药宣布收到 FDA 的完整回复函(CRL),首次海外上市之旅正式宣告夭折,股价当日便狂跌 60% 以上。合作方恒瑞也迅速发布公告作澄清说明:已向万春支付 2 亿元的首付款,但尚未参与到临床开发当中;而此前达成的 1 亿元股权投资也尚未完成缴款和股权交割。双方将进一步协商普那布林后续研发计划及合作事项。
万春药业近 3 年股价走势

截图来自:MarketWatch
而今日,随着 NMPA 通知件的发布,普那布林在国内的首次上市申请也暂时搁浅。恒瑞发布的最新公告也表示,公司尚未开展任何关于普那布林的临床研究,且目前没有后续研发计划。
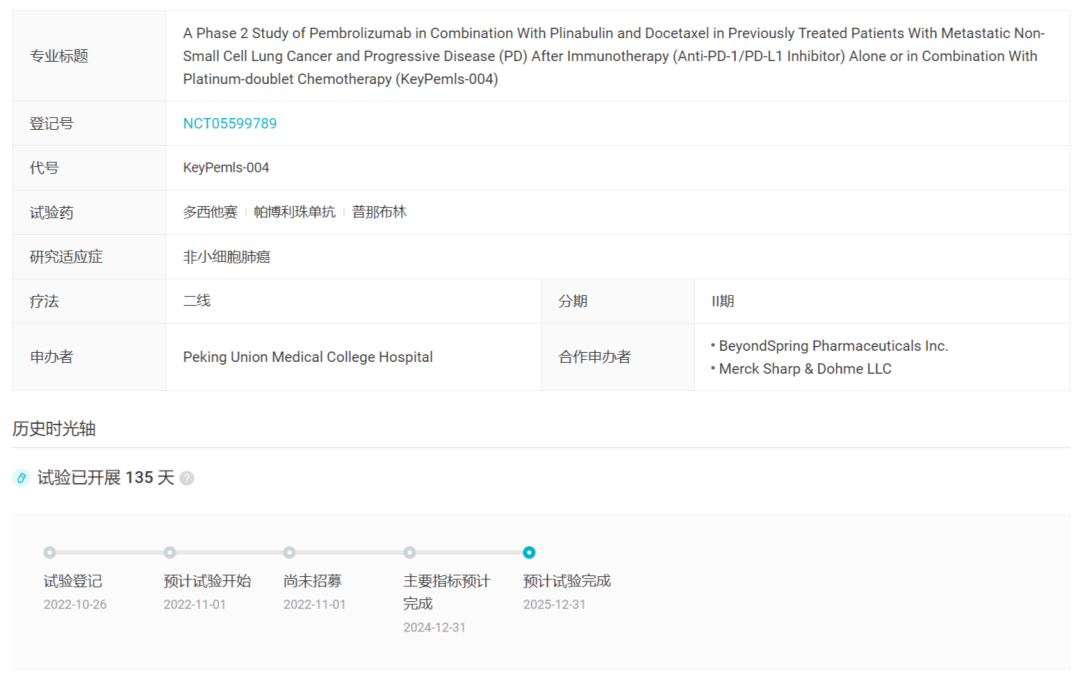
不过据 Insight 数据库显示,在 2021 年连遭挫折后,2022 年普那布林仍有一项新的临床试验登记。这是一项 2 期临床试验,联用 K 药和多西他赛二线治疗 NSCLC,试验代号为 KeyPemls-004(NCT05599789)。
免责声明:本文仅作信息分享,不代表 Insight 立场和观点,也不作治疗方案推荐和介绍。如有需求,请咨询和联系正规医疗机构。
编辑:加一
PR 稿对接:微信 insightxb
投稿:微信 insightxb;邮箱 insight@dxy.cn
点击卡片进入 Insight 小程序
国内审评进度、全球新药开发…
随时随地查!

多样化功能、可溯源数据……
Insight 数据库网页版等你体验
点击阅读原文,立刻解锁!



 个人中心
个人中心
 我是园区
我是园区




