
由于治疗手段有限,胃癌仍然是全球癌症相关死亡的第四大原因
(https://gco.iarc.fr/today)
。大多数胃癌通过Correa途径发展,包括胃炎、萎缩、肠化生、异型增生,最终形成癌症
【1-3】
。基于小鼠模型的谱系追踪研究和基于人类样本的克隆分析表明,胃癌的肠化生和癌症起源都倾向于来自组织驻留干细胞
【4】
。因此,更好地理解胃上皮干/祖细胞将有助于加深我们对于胃癌发生发展的认识,并且可能启发新的治疗策略。虽然胃上皮干细胞在胃的终生自我更新和体内平衡中起着至关重要的作用,但是对于胃上皮干细胞的身份目前仍有争议。尽管一些研究致力于寻找胃上皮干细胞的代表性标志基因,然而这些被鉴定出来的标志基因在不同的研究中并不总是一致。此外,识别胃上皮干细胞的研究主要基于小鼠模型,而小鼠胃上皮干细胞在多大程度上与人类胃上皮干细胞相似目前仍不清楚。
2022年11月15日,北京大学生物医学前沿创新中心
(BIOPIC)
汤富酬团队与北医三院普通外科付卫团队紧密合作,在
Protein & Cell
上发表了题为
Spatially-resolved expression landscape and gene-regulatory network of human gastric corpus epithelium
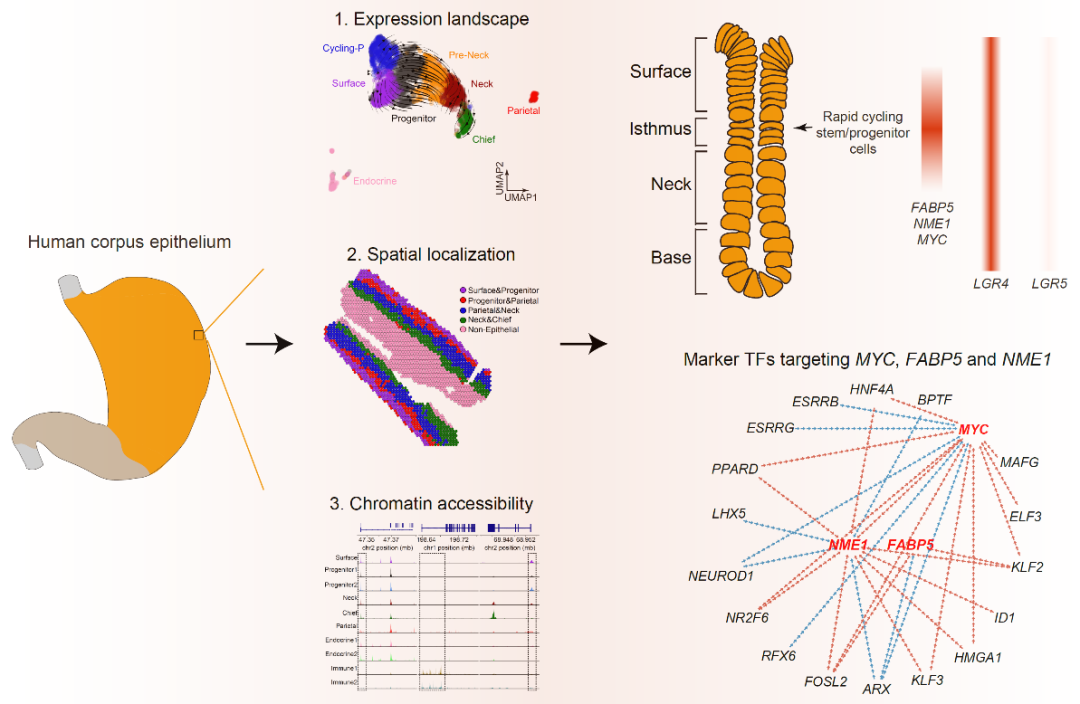
的研究论文。在这项工作中,研究人员首先利用单细胞转录组测序技术构建了人类胃体上皮细胞基因表达图谱,
根据基因表达模式鉴定细胞群体身份,并着重鉴定胃上皮干/祖细胞类群
。然后,研究人员使用空间转录组技术对人类胃上皮细胞类群进行空间定位,并推断不同细胞类型之间的相互作用。之后,研究人员
分析了人类胃体上皮细胞的染色质状态及其对基因表达的调控机制
。最后,研究人员
在人类胃上皮干/组细胞的体外2D和3D培养模型中对相关信号通路和特异性标志基因进行了深入的功能分析和机制研究。
具体来说,研究人员在人类胃体的腺体峡部发现了一类胃上皮干/祖细胞群,这群细胞中的EGF和WNT信号通路被特异性激活来维持其细胞稳态。同时,研究人员发现在人类胃体上皮中,是LGR4而非传统认为的LGR5介导WNT信号通路的激活。更重要的是,研究人员在胃上皮干/祖细胞中鉴定出两个全新的标志基因,FABP5和NME1,并通过基于人类胃上皮干/组细胞的体外2D和3D培养模型的功能实验证明这两个基因对正常胃上皮干/祖细胞和胃癌细胞的稳态维持都至关重要,说明这两个基因实际上是胃上皮干/组细胞的重要调控基因。之后,研究人员在染色质状态这一表观遗传学层面探讨了胃体上皮关键标志基因的表观遗传学调控机制,并确定了多个重要的细胞类型特异性转录因子
(例如胃上皮干/组细胞的重要调控转录因子ID1,KLF2,KLF6,ATF3,ELF3和MYC)
。
综上所述,
该研究在单细胞分辨率系统地揭示了人类胃体上皮细胞的基因表达特征和表观遗传学调控特征,鉴定了胃上皮干/组细胞的重要调控基因FABP5和NME1,确认了EGF和WNT信号通路对于维持胃上皮干/组细胞的重要功能,为未来相关疾病特别是胃癌的诊断和治疗提供了潜在的帮助。
北京大学生物医学前沿创新中心汤富酬教授与北医三院普通外科付卫教授为该论文的共同通讯作者。广州实验室董骥博士、河北农业大学吴兴龙博士、北医三院周鑫博士、北京大学博士生高原、广州实验室王长亮博士和北医三院王文东博士为该论文的并列第一作者。
原文链接:
https://academic.oup.com/proteincell/advance-article/doi/10.1093/procel/pwac059/6827980
制版人:十一
1. N. Uemura et al., Helicobacter pylori infection and the development of gastric cancer. Nihon Rinsho Japanese Journal of Clinical Medicine 345, 784 (2001).
2. P. Correa, Y. H. Shiao, Phenotypic and genotypic events in gastric carcinogenesis. Cancer Research 54, 1941s (1994).
3. P. Correa, Human gastric carcinogenesis: a multistep and multifactorial process--First American Cancer Society Award Lecture on Cancer Epidemiology and Prevention. Cancer Research 52, 6735-6740 (1992).
4. Y. Hayakawa, J. G. Fox, T. C. Wang, The Origins of Gastric Cancer From Gastric Stem Cells: Lessons From Mouse Models. Cell Mol Gastroenterol Hepatol 3, 331-338 (2017).

【非原创文章】本文著作权归文章作者所有,欢迎个人转发分享,未经作者的允许禁止转载,作者拥有所有法定权利,违者必究。











 个人中心
个人中心
 我是园区
我是园区





