6 月 9 日,安斯泰来宣布,已向日本厚生劳动省提交了 Zolbetuximab 的新药申请(NDA),拟用于一线治疗 CLDN18.2 阳性、HER2 阴性的局部晚期不可切除或转移性胃或胃食管交界处(G/GEJ)腺癌。如顺利获批,Zolbetuximab 将成为全球首个获批的 CLDN18.2 靶向疗法。
Zolbetuximab 是安斯泰来在研的一款 CLDN18.2 单抗。
此次 NDA 是基于两项 III 期临床
SPOTLIGHT 和 GLOW 研究
结果。
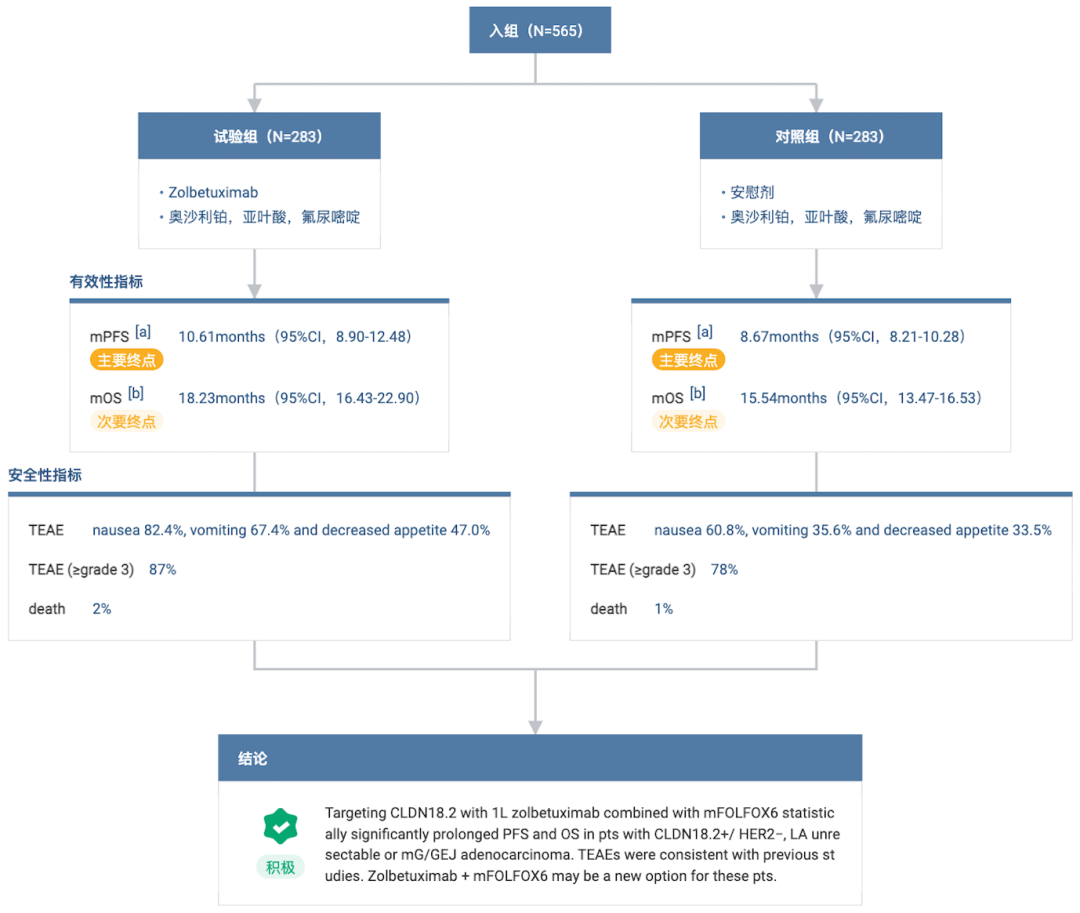
SPOTLIGHT 研究
探索了 Zolbetuximab 联合 mFOLFOX6(奥沙利铂、亚叶酸 + 氟尿嘧啶联合方案)一线治疗 CLDN18.2 阳性、HER2 阴性局部晚期不可切除或转移性胃或胃食管交界处腺癌的疗效和安全性。
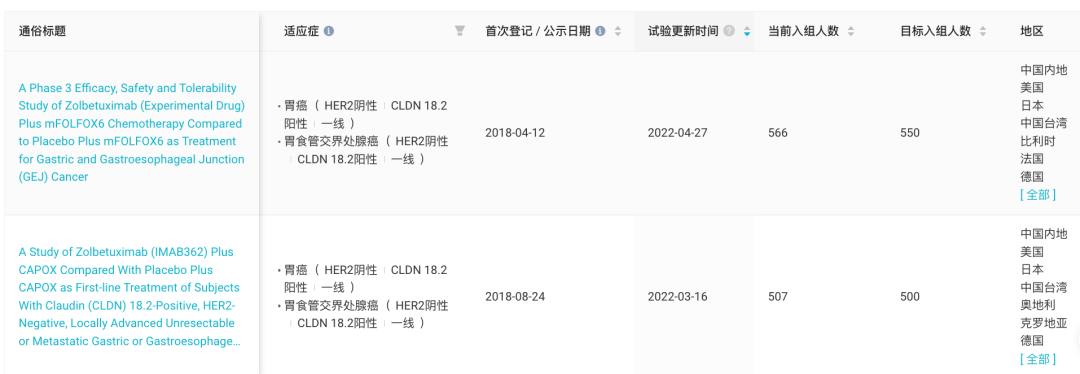
这项全球多中心随机、双盲研究在 220 多家研究中心招募了 566 名患者,安斯泰来表示,该试验将为 Zolbetuximab 在美国、欧洲、亚洲及全球其他国家的后续监管提交提供基础数据。
结果显示达到主要研究终点,与安慰剂组相比,Zolbetuximab 与 mFOLFOX6 联合用药将疾病进展或死亡风险降低了 24.9%(HR=0.751;95%CI: 0.598-0.942;P=0.0066)。治疗组的中位 PFS 为 10.61 个月,安慰剂组为 8.67 个月。
此外,Zolbetuximab 与 mFOLFOX6 联合用药可显著延长 OS,将死亡风险降低了 25.0%(HR=0.750;95%CI:0.601-0.936;P=0.0053)。治疗组和安慰剂组的中位 OS 分别为 18.23 个月和 15.54 个月。
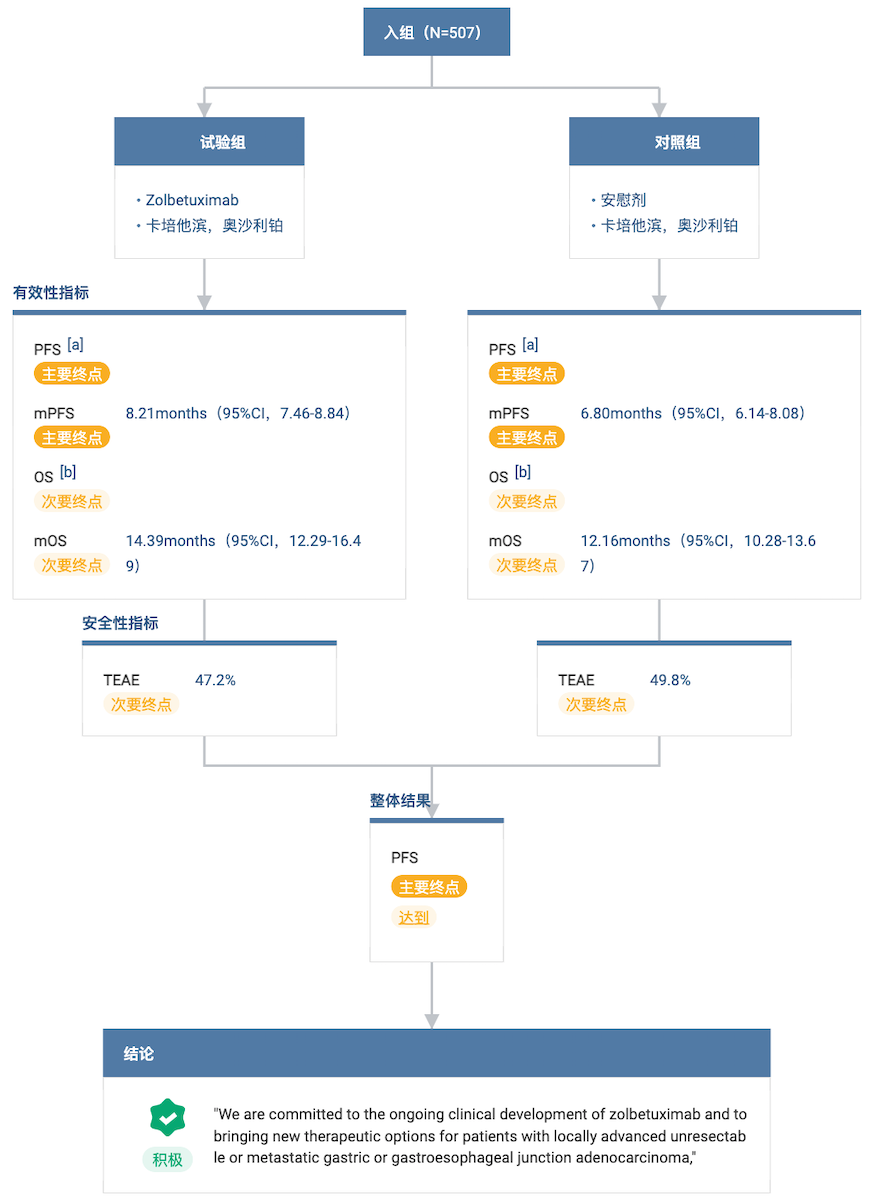
另一项 III 期临床 GLOW 研究则评估了 Zolbetuximab 联合 CAPOX(卡培他滨 + 奥沙利铂)一线治疗胃癌的疗效。
该研究共纳入 507 名 CLDN18.2 高表达(表达水平≥75%)初治 G/GEJ 腺癌患者。
结果显示达到主要研究终点,与安慰剂组相比,Zolbetuximab 联合 CAPOX 将疾病进展或死亡风险降低了 31.3%(HR=0.687;95% CI: 0.544-0.866;p=0.0007)。治疗组的中位 PFS 为 8.21 个月,安慰剂组为 6.80 个月。
此外,研究还表明,Zolbetuximab 联合 CAPOX 显著延长了关键次要终点——总生存期 (OS),将死亡风险降低了 22.9%(HR=0.771;95% CI:0.615-0.965;p=0.0118)。治疗组和安慰剂组的中位 OS 分别为 14.39 个月(95% CI:12.29-16.49)和 12.16 个月(95% CI:10.28-13.67)。
在安全性方面,研究中治疗期间严重不良事件(TEAE)Zolbetuximab 治疗组与安慰剂组的发生率相近(47.2% vs. 49.8%),且与以往研究一致。在 GLOW 研究期间,最常见的治疗期间严重不良事件分别是恶心(68.5% vs. 50.2%)、呕吐(66.1% vs. 30.9%)和食欲下降(41.3% vs. 33.7%)。
据 Insight 数据库显示,
SPOTLIGHT 和
GLOW
这两项研究都同时在中国开展了研究
,前者国内拟入组约 30 人,当前已入组 36 人;后者国内拟入组超 200 人,当前已入组 143 人。这两项临床试验,或许后续也将支持 Zolbetuximab 在中国的上市申请。
CLDN18.2 在多种原发性恶性肿瘤及其转移灶中异常激活和过度表达,尤其在胃癌、胰腺癌中的表达率较高,达到 60% 以上。
胃癌是中国的高发癌种,据 WHO 2020 年度数据,发病率和死亡率均在中国居于第 3 位,在全球占比超过 40%。因此,CLDN18.2 靶点基于其治疗潜力和患者群体之广。
目前全球研发也异常火热,据 Insight 数据库显示,共 66 个临床阶段项目,其中 58 个有中国企业的身影。
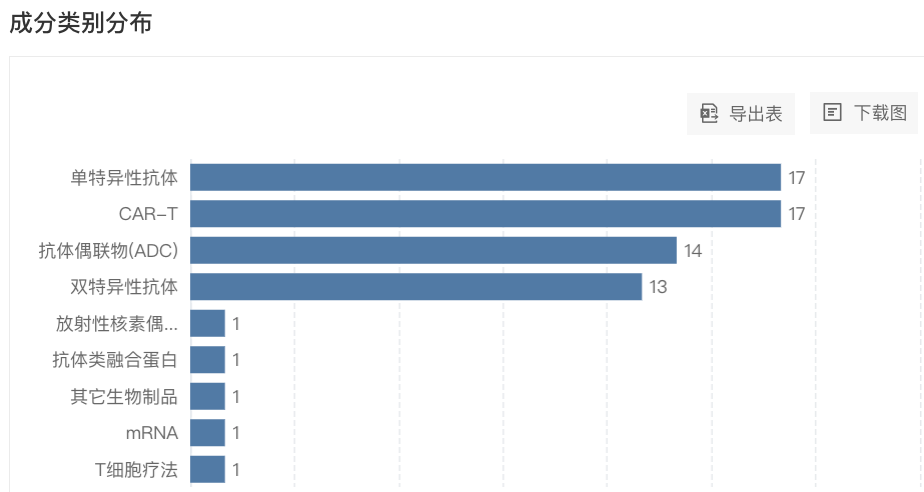
从成分类别来看,进入临床阶段的项目中,涉及单抗、CAR-T、ADC、双抗、抗体类融合蛋白等,其中单抗、CAR-T 并列 TOP1,均有 17 款,ADC、双抗则位居第 2、第 3。
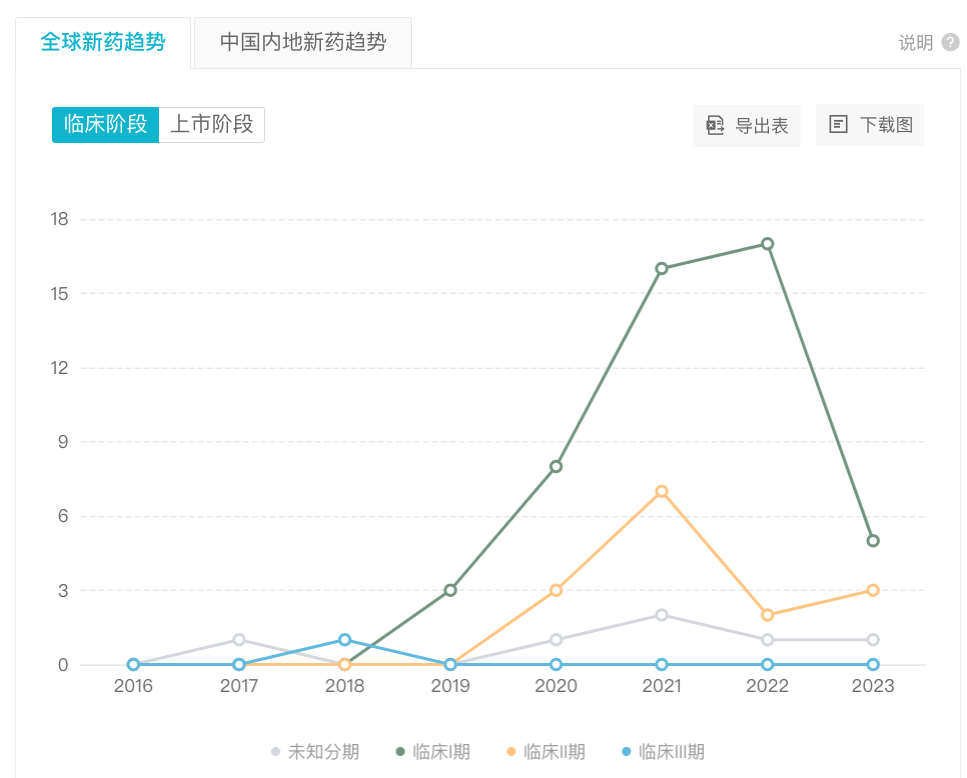
从临床进展来看,CLDN18.2 靶点 2021 年、2022 年进临床项目急增,这两年共有 33 个项目新进 I 期临床,II 期临床阶段有 9 个。
靶向 CLDN18.2 产品申报临床趋势
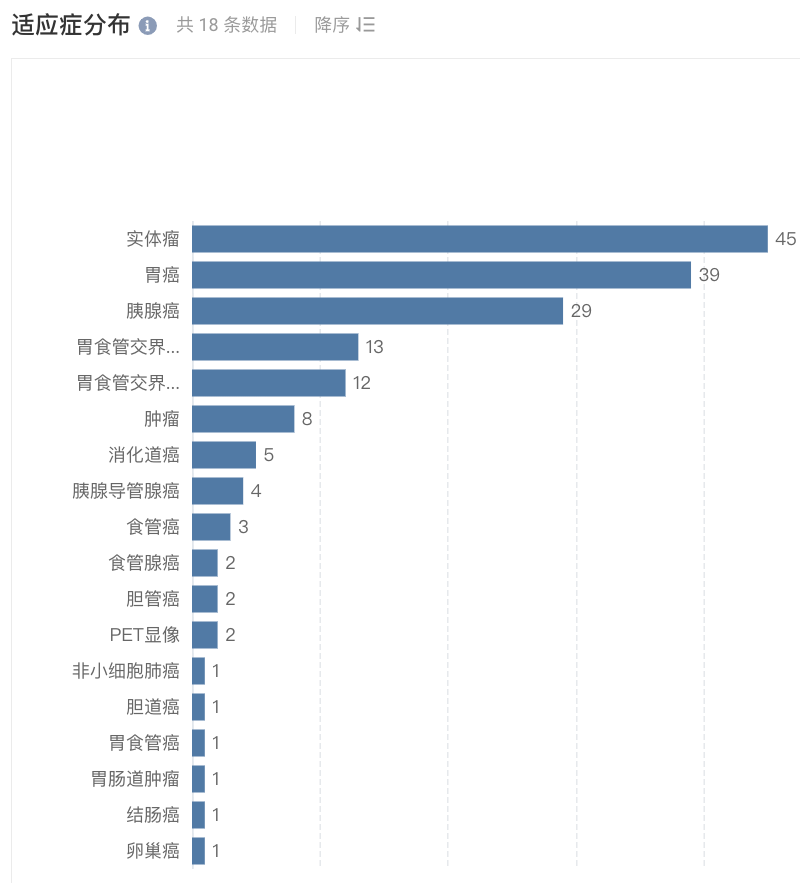
从布局适应症来说,胃癌、胰腺癌布局最多,分别涉及 39、29 个项目。
靶向 CLDN18.2 产品适应症布局(部分)
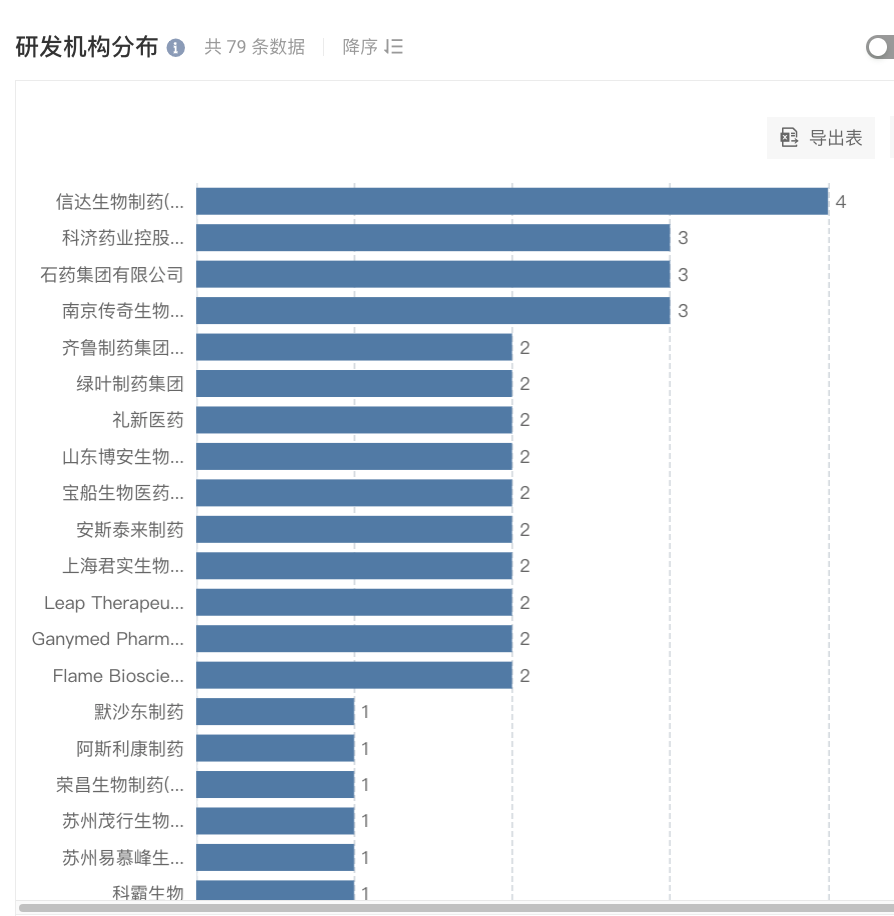
从企业布局来看
,安斯泰来 Zolbetuximab 则是 CLDN18.2 靶点最早的引领者之一,去年 11 月,Zolbetuximab 在 III 期临床试验 SPOTLIGHT 研究中取得了积极结果,成为 CLDN18.2 靶点的首个 III 期临床成功。并于近期在日本申报上市。
信达生物
则同时布局 4 款 CLDN18.2 新药管线,全面囊括了 ADC、CAR-T、双抗、单抗这四大分类,可见对 CLDN18.2 治疗潜力的看好。
信达生物 CLDN18.2 靶点布局及适应症在研阶段
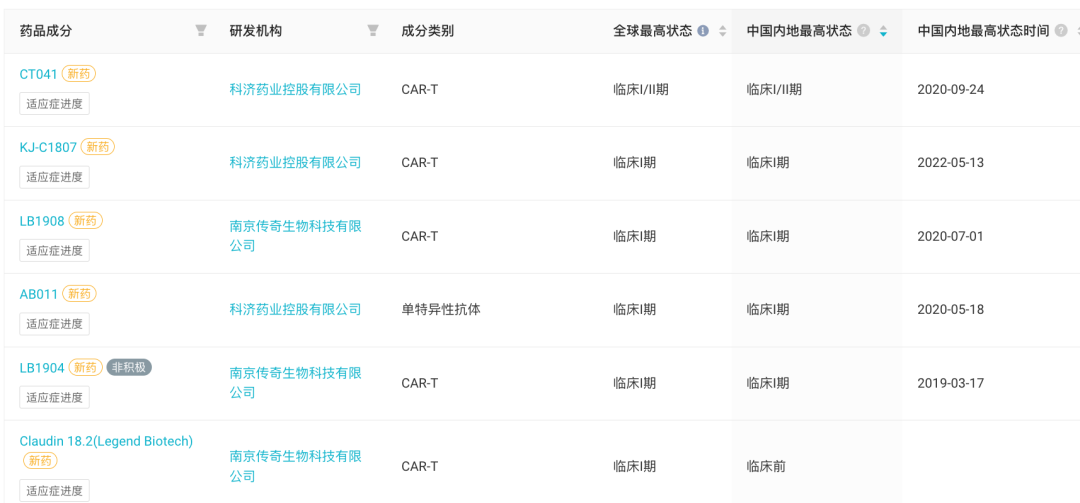
科济药业和传奇生物以 CAR-T 疗法为特色,是这一细分赛道的佼佼者;
科济药业和传奇生物进入临床阶段靶向 CLDN18.2 产品
石药集团则青睐于 ADC,在这一靶点上石药也已经实现了 2 个新药项目出海,证实了关键靶点深度布局策略的初步成功。
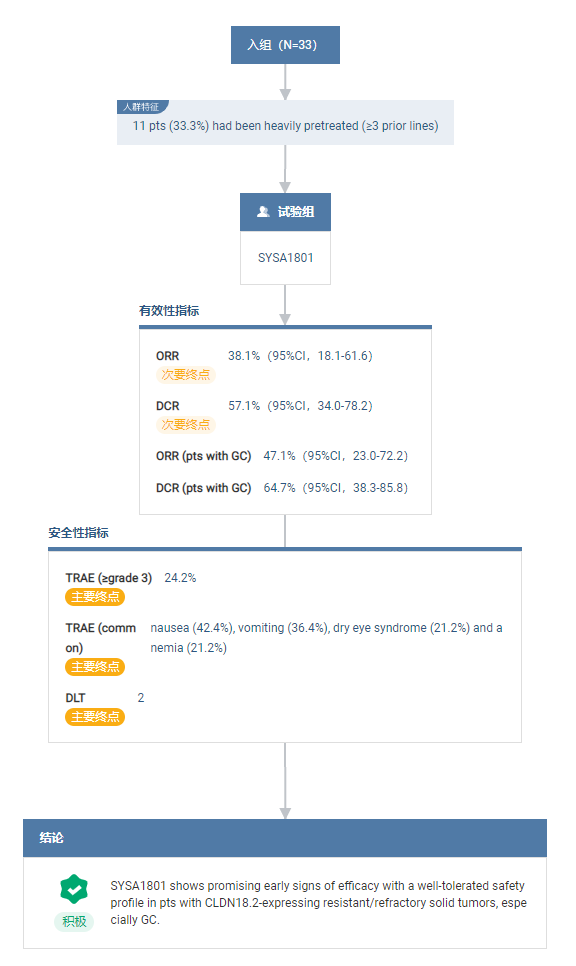
其中,在刚举办的 2023 ASCO 上,石药的 ADC 新药 SYSA1801 首次披露 I 期临床数据。
结果显示,SYSA-1801 在复发/难治性 CLDN18.2 阳性实体瘤中表现出了值得期待的早期疗效信号,同时安全可耐受。
来自:Insight 数据库网页版(http://db.dxy.cn/v5/home/)
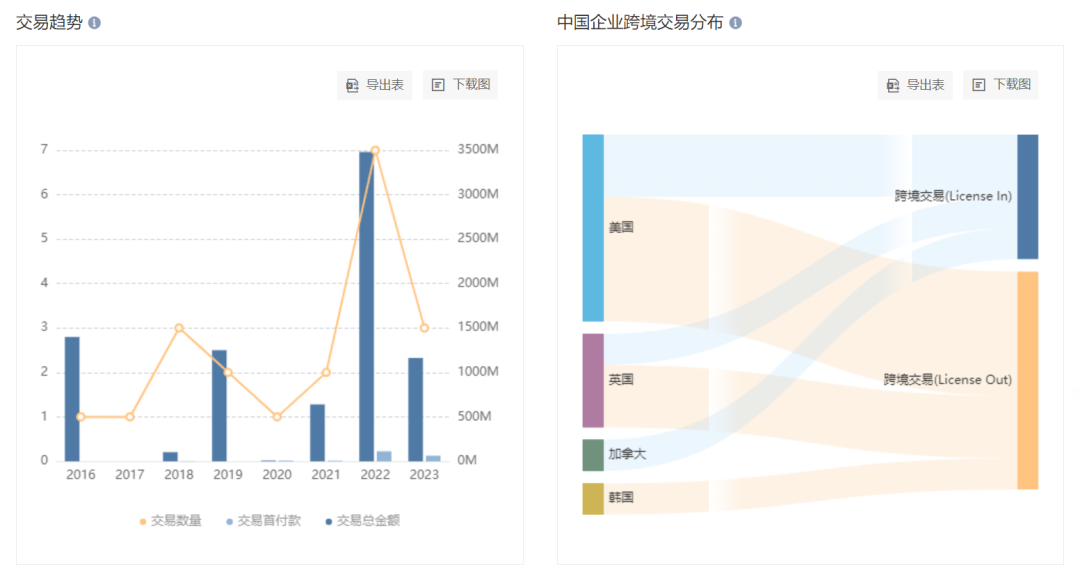
从交易角度看
,发生在这一靶点上的交易项目有 20 项之多,2022 年初迄今已经有 10 项。MNC 企业中阿斯利康对这一靶点尤为关注,引进了 2 款国内企业开发的新药:CMG901(康诺亚,ADC)和 HBM7022(和铂,CD3/CLDN18.2)。
免责声明:本文仅作信息分享,不代表 Insight 立场和观点,也不作治疗方案推荐和介绍。如有需求,请咨询和联系正规医疗机构。
投稿:微信 insightxb;邮箱 insight@dxy.cn
Insight 数据库网页版等你体验
点击阅读原文,立刻解锁!













 药选址
药选址



















