您还不是认证园区!
赶快前去认证园区吧!
注:本文不构成任何投资意见和建议,以官方/公司公告为准;本文仅作医疗健康相关药物介绍,非治疗方案推荐(若涉及)。因水平有限,错误不可避免,或有些信息非最及时,欢迎留言指出。
引言
近日,滨会生物宣布:旗下溶瘤病毒候选药物BS001(OH2)注射液继治疗复发胶质母细胞瘤的临床试验在北京天坛医院启动后,于北美时间8月20日获得美国FDA许可,将在美国开展针对多种实体瘤的临床试验。
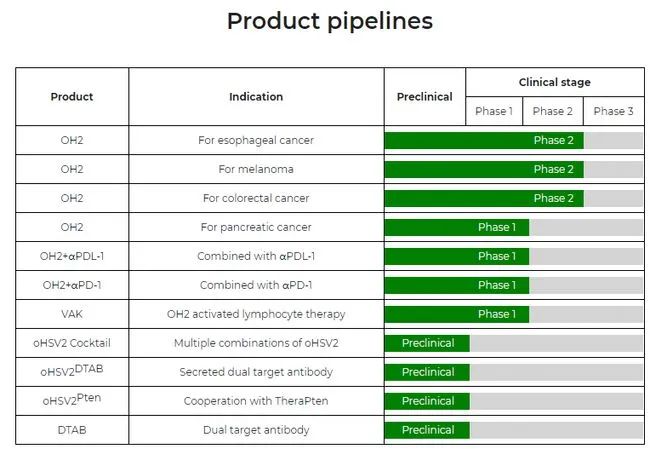
据悉, BS001注射液是全球第一个选择Ⅱ型单纯疱疹病毒(HSV2)作为载体,并且进入临床研究的溶瘤病毒候选药物,也是中国第一个具有完全自主知识产权的新型溶瘤病毒株,首次登上溶瘤病毒免疫治疗的世界舞台。
版权声明:本文转自靶点社,如不希望被转载的媒体或个人可与我们联系,我们将立即删除
↓↓9月29-30日 苏州国际博览中心 ·第三届CMC-China 大会限时免费报名中,点击海报即可报名↓↓




 个人中心
个人中心
 我是园区
我是园区




