您还不是认证园区!
赶快前去认证园区吧!
2021年8月7日/医麦客新闻 eMedClub PR News/--8月5日,乐普生物旗下美雅珂提交的靶向组织因子(TF)的ADC药物MRG004A的临床试验申请获得默示许可。
MRG004A在美国的IND申请于今年2月已经获得FDA的批准,正在开展针对TF阳性晚期或转移性实体瘤的I期研究,如今也是国内第一个获得临床许可的TF ADC药物。

组织因子是一个参与凝血的跨膜蛋白,但是在多种肿瘤中发现TF的异常高表达。TF的异常表达通常与肿瘤生长、血管生成、肿瘤转移和临床治疗预后差相关,因此被认为是一个有吸引力的癌症治疗靶点,有望满足多种实体瘤的未满足临床需求。
全球目前尚无任何靶向TF的药物获批上市,开发进度最快的是Genmab/ Seagen联合开发的tisotumab vedotin,同样也是一款抗体偶联药物。tisotumab vedotin在今年4月获得FDA受理上市,主要适用于化疗期间或化疗后复发或转移的宫颈癌患者。该药物的申请还获得了FDA授予的优先审评资格,将在2021年10月10日迎来FDA的审批决定。
与tisotumab vedotin采用的通过链间硫醇基团的传统偶联技术不同,MRG004A是乐普生物/美雅珂基于从Synaffix引进的GlycoConnect™定点偶联技术和HydraSpace™极性间隔技术开发的一款创新ADC药物。
该项技术对偶联部位具有精准控制,可以降低药物在血液循环中脱落风险和毒性,具有更宽的治疗窗口。在临床前研究中,MRG004A已经在携带Kras G12V突变的胰腺癌及卵巢癌等多个动物模型中表现出显著的抗肿瘤活性,显示出了较好的临床应用潜力。
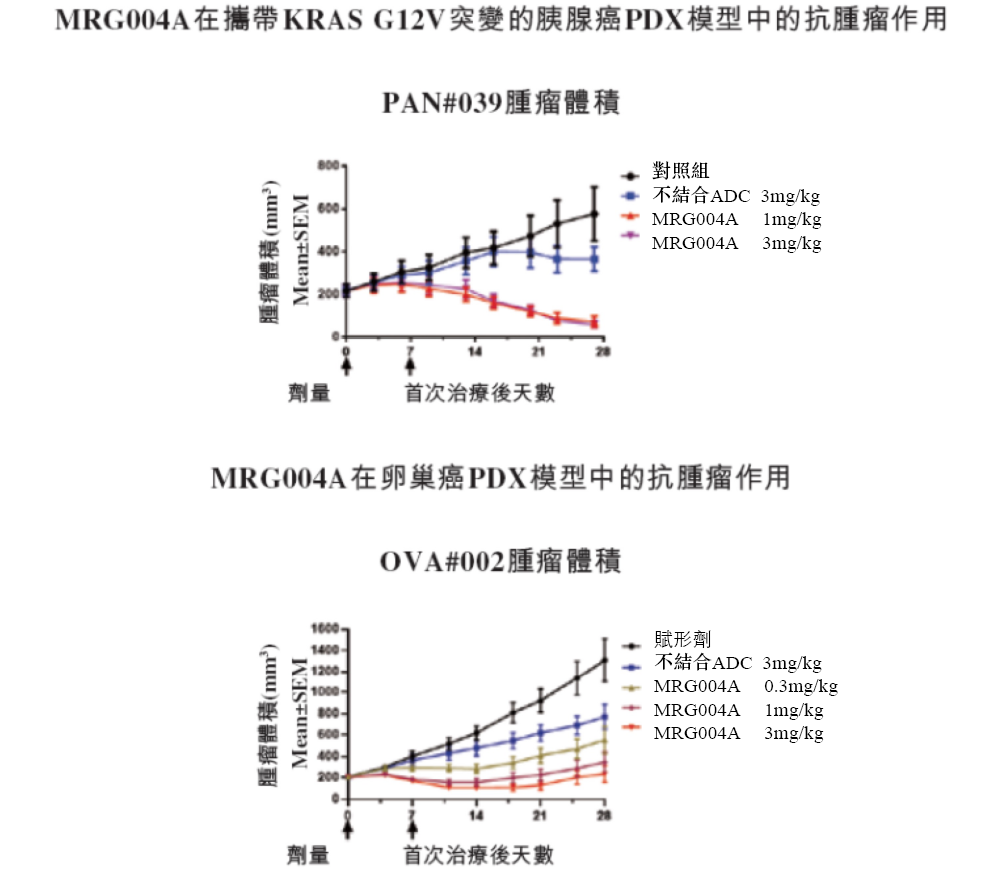
图片来源:乐普生物招股书
总结


 点击“阅读原文”,立即报名!
点击“阅读原文”,立即报名!



 个人中心
个人中心
 我是园区
我是园区




