您还不是认证园区!
赶快前去认证园区吧!

2022年3月23日,诺华宣布177Lu-PSMA-617获得FDA批准,用于治疗PSMA阳性的、经治疗进展的去势抵抗前列腺癌,商品名为Pluvicto。FDA同时批准gallium-68作为PSMA阳性肿瘤的造影剂,商品名为Locametz。

Pluvicto的辐射剂量量度为1000MBq/ml,镥177的半衰期6.647天。
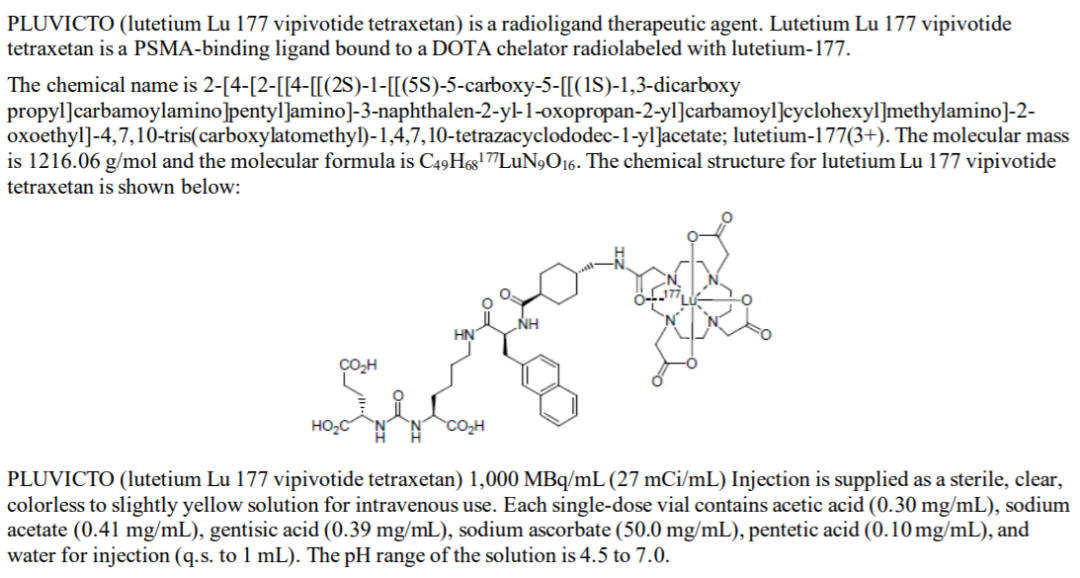
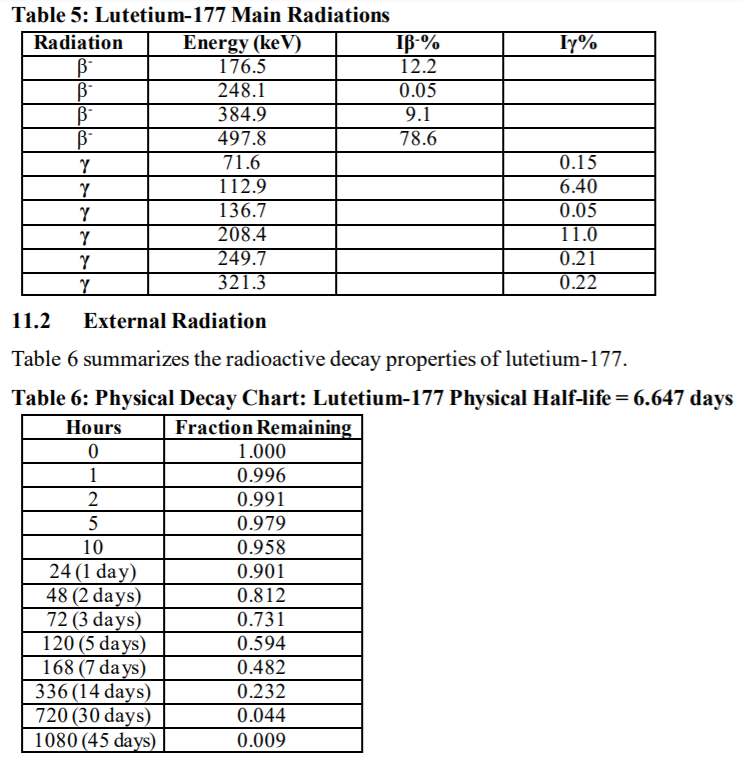
Pluvicto作为一种核药,结合了靶向性配体与放射性同位素疗法,靶向到PSMA阳性细胞,通过放射性同位素导致DNA损伤以杀伤肿瘤细胞。
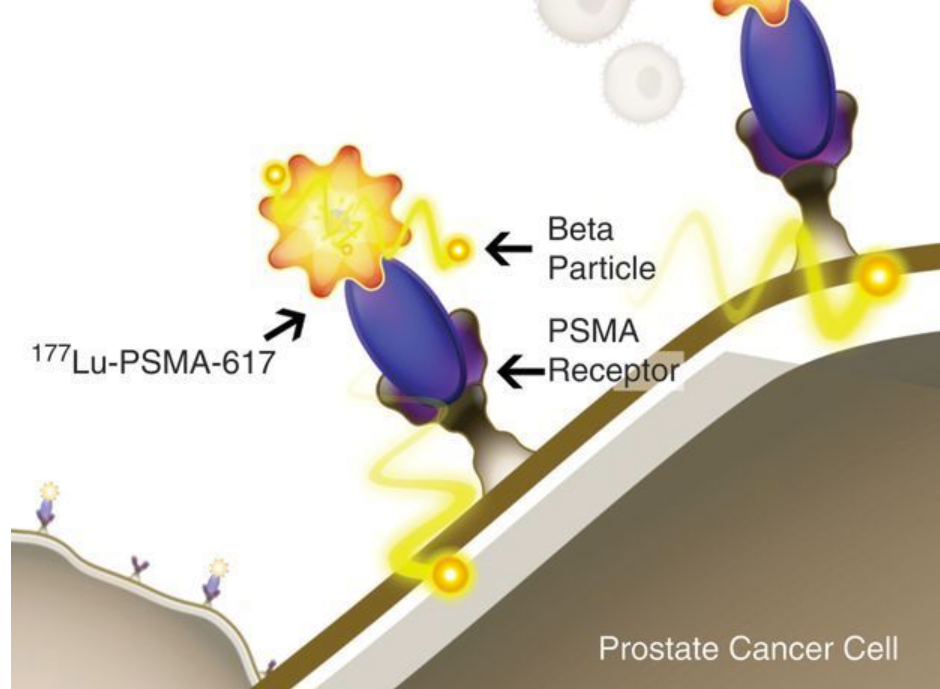
Pluvicto此次获批是依据三期临床VISION的数据,治疗总缓解率为30%,其中完全缓解率为6%,治疗降低38%的死亡风险。
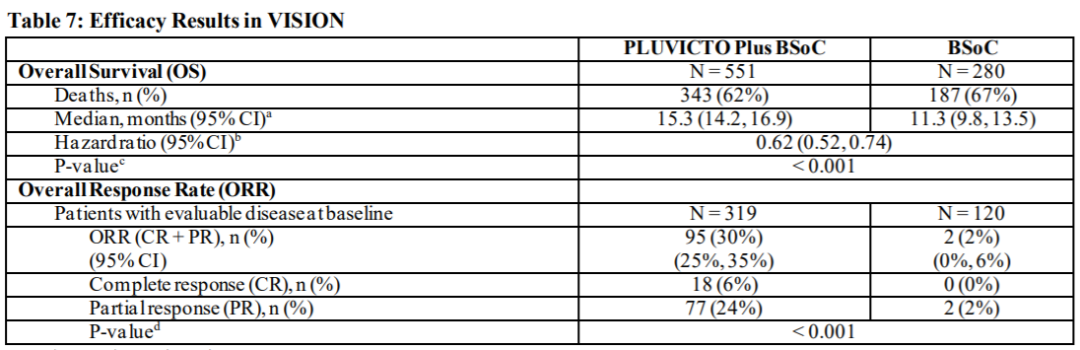
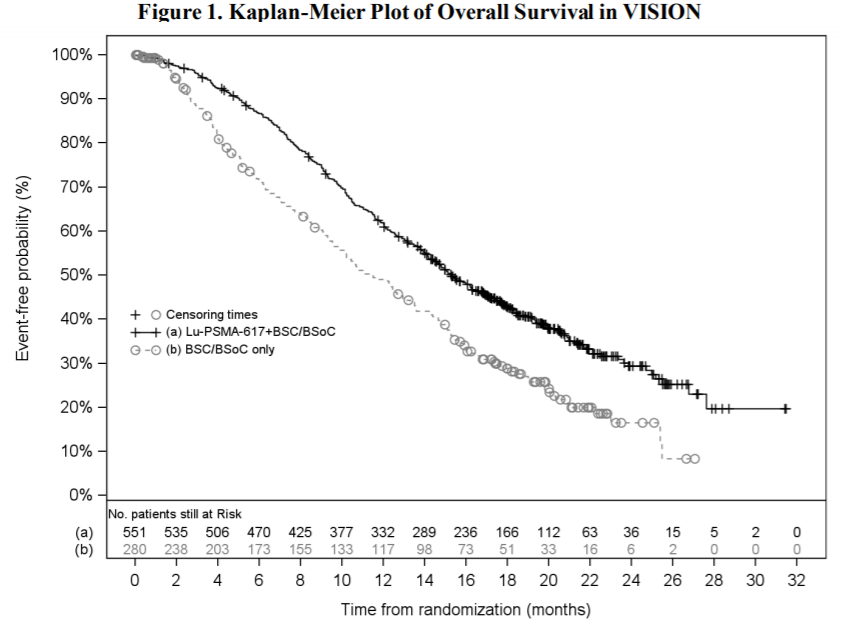
Pluvicto的安全性数据如下。
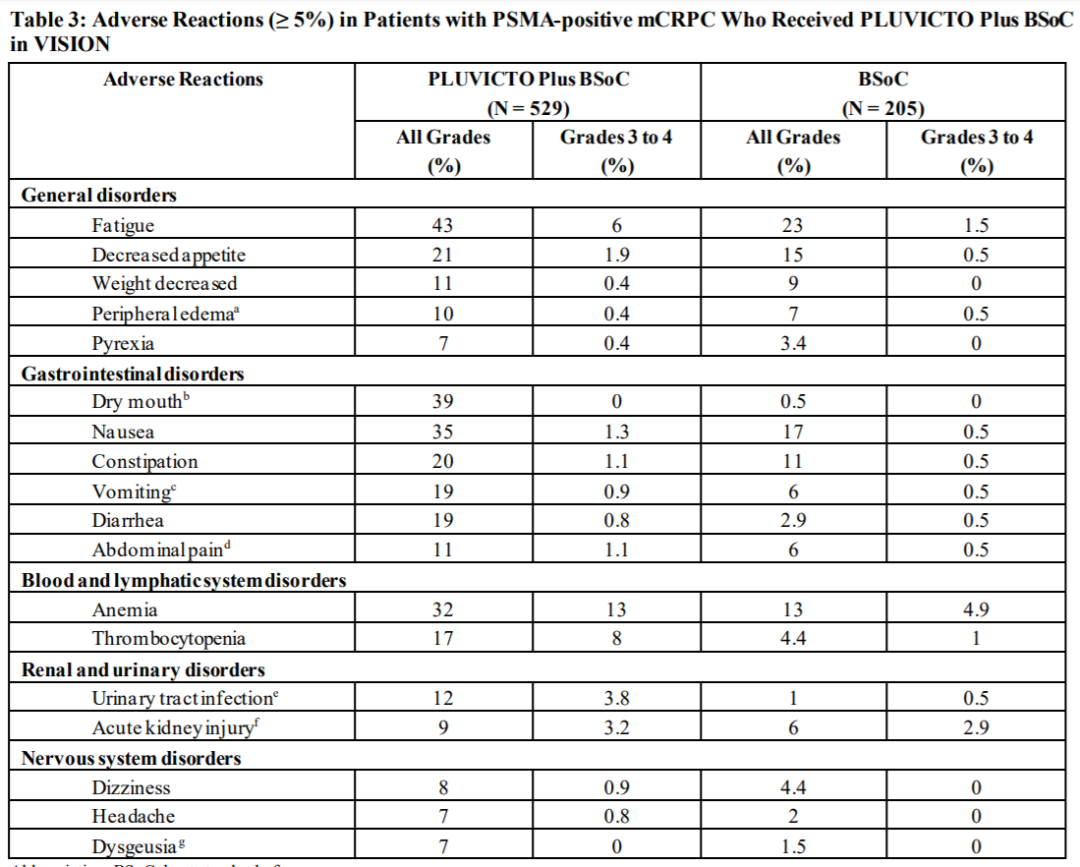
诺华正在拓展Pluvicto的治疗范围。

Pluvicto的获批标志着核药领域的又一个重大进展,对于很多难治性癌症又提供了一种重要治疗手段。诺华还有多款核药在研,多数均采用镥-177同位素。
免责声明



 个人中心
个人中心
 我是园区
我是园区




