

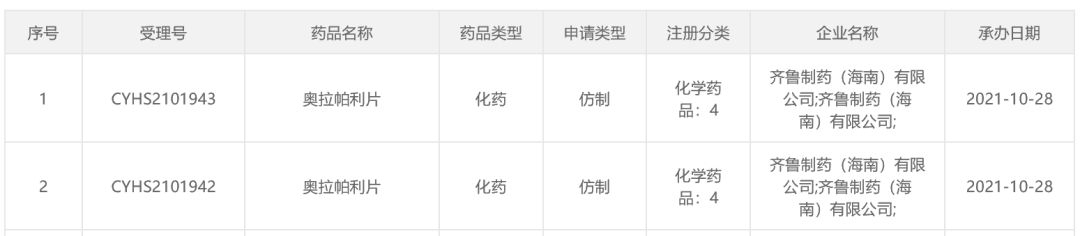
日前,齐鲁制药递交的「奥拉帕利片」4类仿制药上市申请获CDE受理,成为国内首款报产的奥拉帕利仿制药。
奥拉帕利是一款口服多聚ADP核糖聚合酶(PARP)抑制剂,利用肿瘤DNA损伤反应(DDR)途径的缺陷,优先杀死癌细胞。
原研奥拉帕利(olaparib,Lynparza)由阿斯利康研发,最早于2014年先后在欧洲和美国获批,目前Lynparza已在美国获批多个适应症:一线维持治疗BRCAm晚期卵巢癌成人患者;联合贝伐单抗一线维持治疗HRD阳性晚期卵巢癌成人患者;维持治疗复发性卵巢癌成人患者;晚期gBRCAm卵巢癌成人患者;gBRCAm、HER2-转移性乳腺癌成人患者;一线维持治疗gBRCAm转移性胰 腺癌成人患者;携带特定基因突变的转移性去势抵抗性前列腺癌(mCRPC)患者。
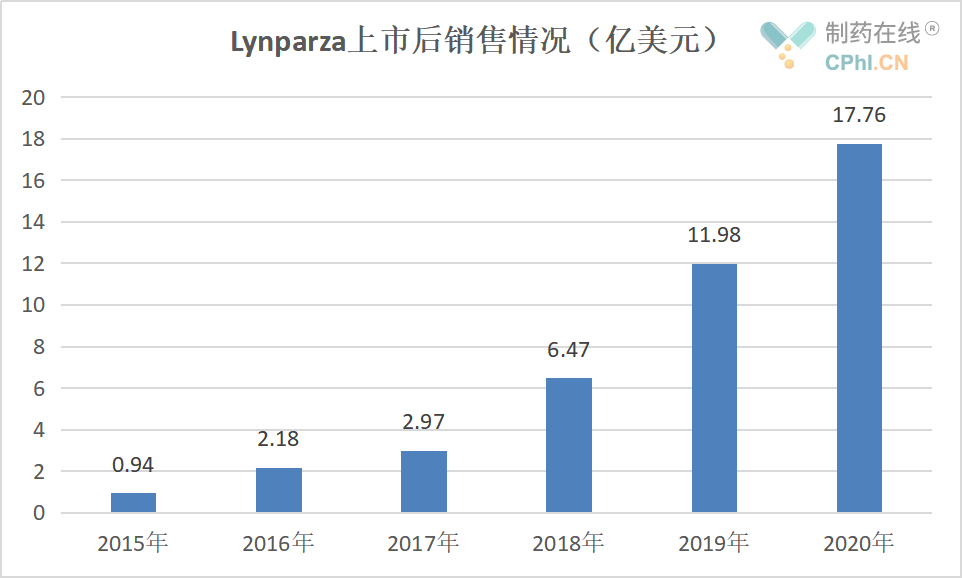
作为全球获批的首个PARP抑制剂,Lynparza市场表现不凡,2019年进入重磅药行列,2020年销售额达到17.76亿美元。
在国内,原研奥拉帕利于2018年12月被NMPA批准用于铂敏感复发性上皮性卵巢癌、输卵管癌或原发性腹膜癌成人患者在含铂化疗达到完全缓解或部分缓解后的维持治疗,商品名为利普卓。
随后,利普卓又先后被NMPA批准用于携带胚系或体细胞 BRCA 突变的(gBRCAm 或 sBRCAm)晚期上皮性卵巢癌、输卵管癌或原发性腹膜癌初治成人患者在一线含铂化疗达到完全缓解或部分缓解后的维持治疗(2019.12),以及单药治疗携带BRCA1/2突变(胚系和/或体细胞系)且在既往新型激素药物治疗后出现疾病进展的转移性去势抵抗性前列腺癌成人患者(2021.06),其中前两个适应症被纳入医保支付范围。
据悉,奥拉帕利化合物专利于2024年过期,目前国内已有多家企业开始布局。其中齐鲁制药率先完成BE试验递交上市申请,宣泰医药、科伦药业处于BE试验阶段,豪森药业、罗欣药业、石药集团等8家企业获批临床。
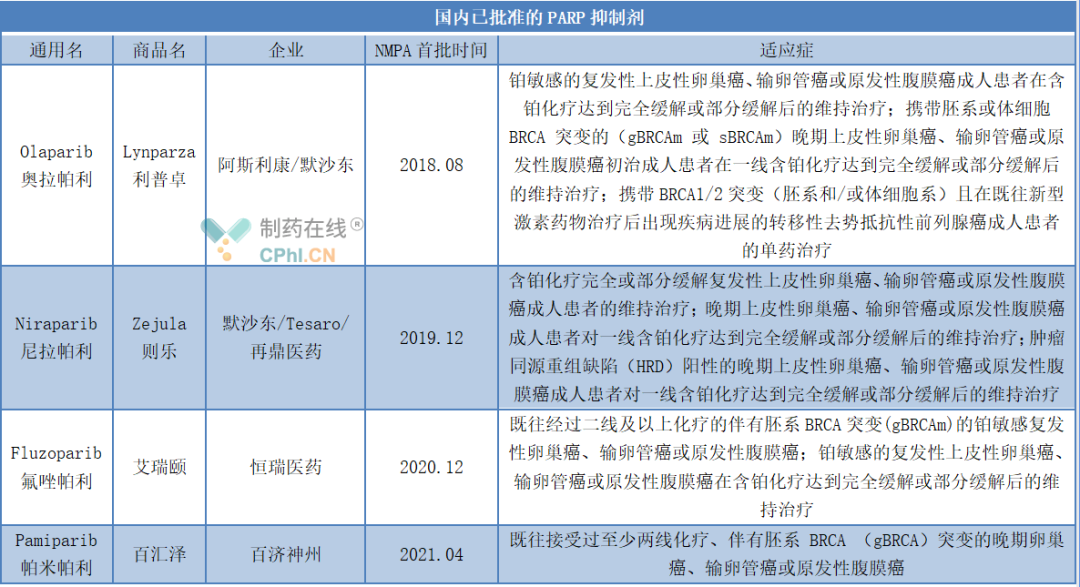
PARP抑制剂是一类重磅肿瘤药,目前国内已经批准4款(详见下表),2款国产,2款进口,其中仅奥拉帕利和尼拉帕利进入2020年医保。随着新一轮医保谈判逼近,氟唑帕利和帕米帕利2款国产PARP抑制剂也有望进入国家医保。
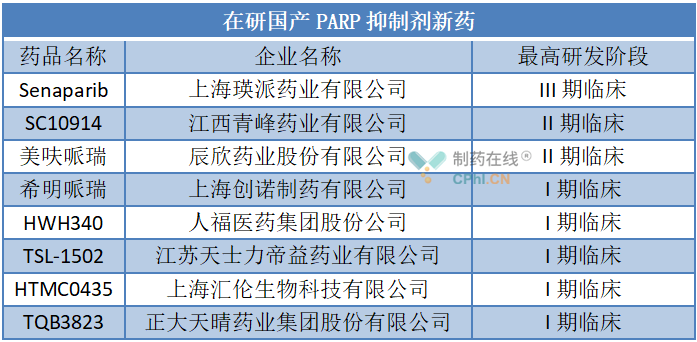
值得一提的是,在PARP抑制剂领域,我国药企似乎更注重于创新,仅布局了奥拉帕利仿制药市场。据insight数据库,目前国内还有多款在研国产PARP抑制剂新药,详见下表。
在首仿领域,今年齐鲁制药已先后取得甲磺酸雷沙吉兰片、二甲双胍维格列汀片、注射用头孢哌酮阿维巴坦钠首仿生产批件,而且还率先在国内递交了地舒单抗生物类似物的上市申请。此外,今年齐鲁制药递交上市申请的厄洛替尼、磷酸奥司他韦干混悬剂、阿普米司特、瑞戈非尼、磷酸特地唑胺、溴莫尼定噻吗洛尔滴眼液、艾曲泊帕乙醇胺、地夸磷索钠滴眼液也均有望冲击国内首仿。
◆ 企业推荐 ◆

◆ 11月培训会预告 ◆
来源:CPhI制药在线
声明:本文仅代表作者观点,并不代表制药在线立场。本网站内容仅出于传递更多信息之目的。如需转载,请务必注明文章来源和作者。
投稿邮箱:Kelly.Xiao@imsinoexpo.com



点击“阅读原文”报名中美双报培训会!



 个人中心
个人中心
 我是园区
我是园区






