重磅!中国首款CAR-T细胞治疗产品正式获批
收藏
关键词:
获批
资讯来源:生物探索 + 订阅账号
发布时间:
2021-06-23
6月22日,国家药监局(NMPA)官网公示显示,复星凯特CAR-T细胞治疗产品阿基伦赛注射液(axicabtagene ciloleucel)已正式获批。这意味着,中国迎来了首款获批上市的CAR-T细胞治疗产品。
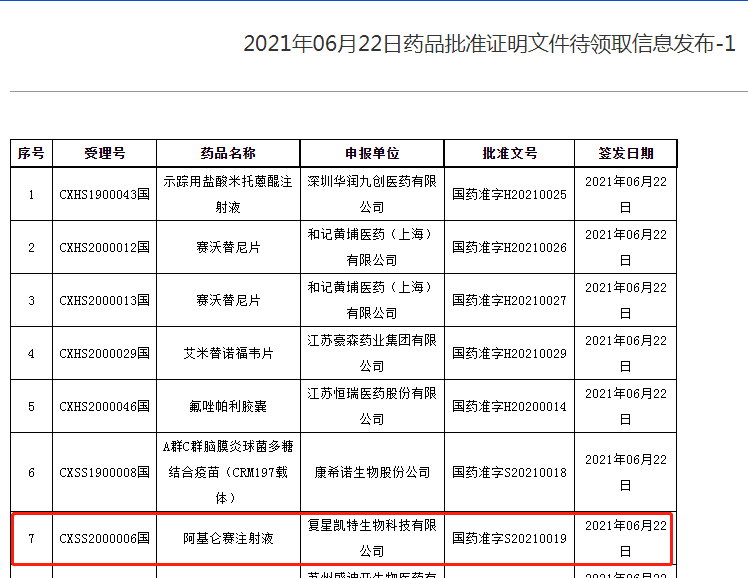
阿基仑赛注射液是复星凯特于2017年初从吉利德子公司Kite Pharma引进的靶向CD19自体CAR-T细胞治疗产品Yescarta。同一年时间,Yescarta率先获得FDA批准上市,成为首款针对特定非霍奇金淋巴瘤的CAR-T细胞药物,并相继在欧洲、加拿大等地获批上市。
根据复星凯特此前公布的信息,阿基仑赛注射液被开发用于治疗两线或以上系统性治疗后复发或难治性大B细胞淋巴瘤,包括弥漫性大B细胞淋巴瘤(DLBCL)非特指型、原发性纵隔B细胞淋巴瘤(PMBCL)、高级别B细胞淋巴瘤和滤泡淋巴瘤转化的DLBCL,复星凯特拥有其在中国包括香港、澳门的商业化权利,并于中国境内(不包括港澳台)进行本地化生产。
尽管阿基仑赛注射液成为我国首款获批上市的CAR-T细胞治疗产品,然而首发能否令复星凯特处于CAR-T领域的优势地位仍然尚未可知。
当前CD19为最热门的细胞治疗靶点,同质化问题较为严重。根据近期《Nature Reviews Drug Discovery》的报告,在全球2000多种细胞疗法中,CAR-T仍然占据主导地位,并且在过去FDA批准的5款CAR-T细胞疗法中,有4款是针对CD19靶点。据媒体报道,在中国 357项的CAR-T临床试验中,涉及CD19靶点的试验就高达175项。
在复星凯特的阿基仑赛注射液之外,国内另一位细胞治疗玩家药明巨诺带来的瑞基仑赛也已于2020年 6 月申报上市,预计很快将获批上市。另外,传奇生物的 cilta-cel 或将于今年年底前在美国上市,并在下半年在中国递交上市申请;科济药业 CT053预计将于 2022 年上半年在国内申请上市。
随着我国首款CAR-T细胞疗法上市,国内细胞疗法领域的商业化竞争逐渐拉开帷幕。据弗若斯特沙利文分析,中国CAR-T疗法的市场规模将由2021年的2亿人民币增长至53亿人民币,并于2030年增长到289亿人民币。群雄逐鹿时代即将来临,国内细胞治疗领域的未来发展,值得期待。
参考资料:
[1]http://www.fosunkitebio.com/about.html
[2]https://www.cn-healthcare.com/articlewm/20210118/content-1181654.html
本文系生物探索原创,欢迎个人转发分享。其他任何媒体、网站如需转载,须在正文前注明来源生物探索。
免疫疗法 | 生物仿制药 | 疫苗 | 耐药性 | 药物靶点 | 健康生活 | 药企新闻 | 药物盘点 | 制药技术 | 药物副作用
白血病
| 肺癌
| 胃癌
| 结直肠癌
| 肝癌
| 乳腺癌
| 胰腺癌
| 心血管疾病
| 神经退行性疾病
| 肠道微生物
体外诊断
| 医疗器械
| 生物纳米
| 3D打印
| 基因检测
| 单细胞测序
| 基因编辑
| 辅助生殖
| 人工智能
| 精准医学
抗癌药
| 4+7带量采购
| 耗材
| 备案制
| 注册人制度
| 健康中国
| 新版基药目录
| AI医疗器械
| 远程医疗
| 同股不同权
IPO
| 融资
| 合作
| 基金
| 港交所
| 科创板
| 创业板
| 研发投入
| 收购
| 市场&消费





 个人中心
个人中心
 我是园区
我是园区




