近日,由中山大学公共卫生学院(深圳)、德国弗莱堡大学和中国疾病预防控制中心病毒病预防控制所合作在Science发表题为“Rare variant MX1 alleles increase human susceptibility to zoonotic H7N9 influenza virus”的论文, 该研究首次证实了宿主遗传突变增加了人感染H7N9禽流感病毒的风险。

A.大样品量,WGS深度测序
该研究采取大样品量WGS深度测序的策略,采集了220位H7N9病人和121位健康个体的基因组数据,测量基因组中存在的单核苷酸突变SNV。为了验证其检测突变的精确度,作者同时抽取一部分样品进行质谱基因分型,两种技术得出的结果具有99.7%的吻合度,说明WGS检测的可靠性。其中生信分析服务由华大基因提供。
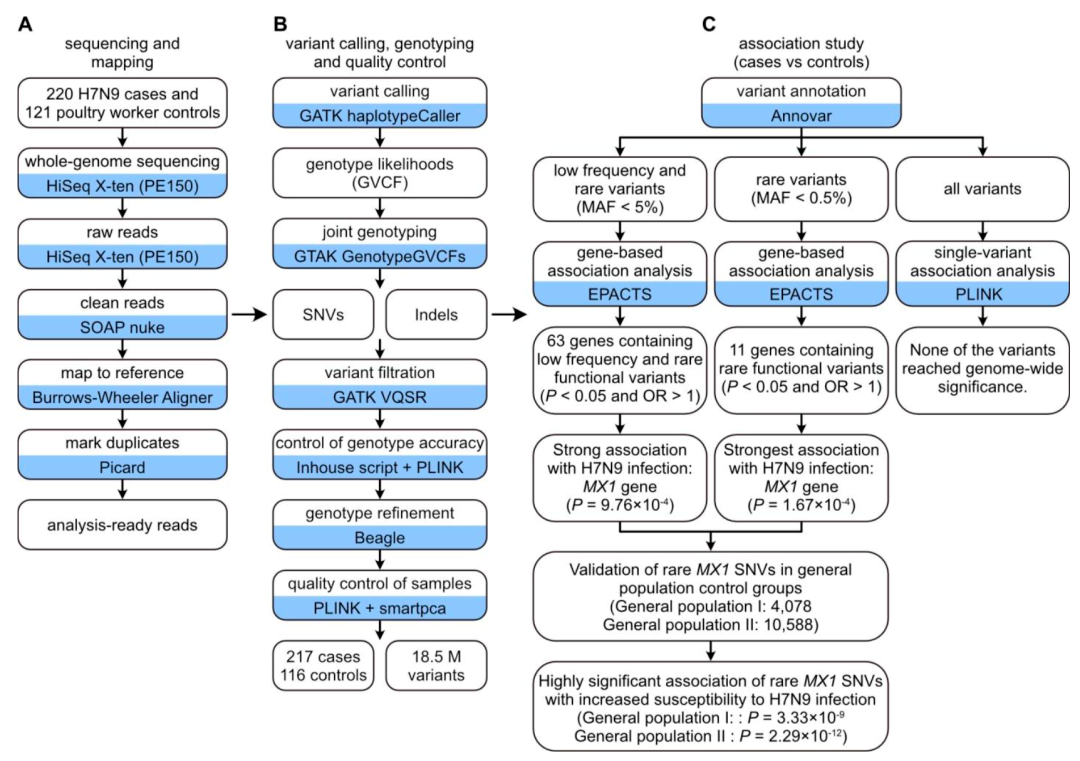
B.关联分析研究
该研究首先进行SNV水平上与H7N9感染之间的关联分析,然而没有得到任何显著结果。接着,研究人员进行基于基因水平考察含有SNV的基因与H7N9感染之间的相关性,结果发现MX1基因与H7N9感染具有较强的相关性。这种相关性体现在,MX1上共发现了分布在21个病人中17种罕见的SNV,而这些SNV在本文对照组的健康人群中并没有发现。
为了体现这种富集性并不具有随机性,作者利用一个样品量更大的数据库——4,078个中国人的健康人群,发现MX1上的突变携带率占1.77%,同时调查了ChinaMap中10,588个样品数据,其中MX1突变携带率仅为1.23%,与该实验中H7N9患者MX1突变携带率(21/217)有很大差异,说明H7N9感染与MX1基因中的SNV突变显著相关。
该研究对患者进行风险分析得出含有MX1 SNV突变的病人患H7N9的风险是非SNV携带者的5.96倍(如表1),这个结果在校正了年龄,性别等因素后依然显著。
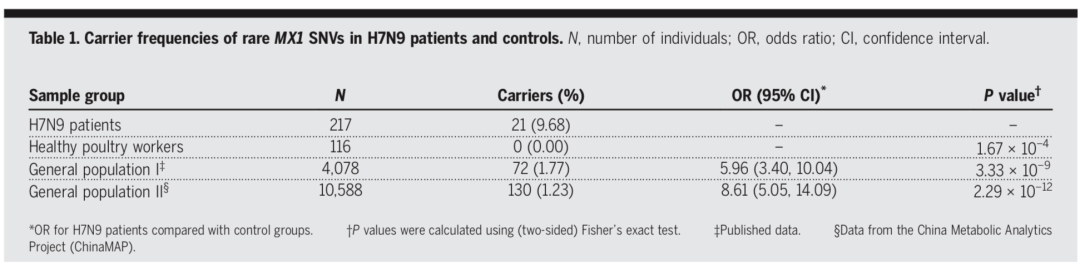
C.MX1基因编码的MxA蛋白对于H7N9感染的机理研究
MX1基因编码的MxA蛋白是一种受干扰素IFN调控的、可以抵御粘性病毒的蛋白,它同时也可以抵抗多种RNA和DNA病毒,包括IAV(如H7N9)。有研究表明,MxA可以抑制病毒的聚合酶功能,从而起到抗病毒功能。
该文首先考察了17种SNV的性质,其中15种是错义突变,一种无义突变,一种剪切点突变。然后,考察这17种SNV在MxA蛋白编码区中的分布,发现在MxA蛋白的三种功能区(G区域,Stalk区域和BSE区域)均有分布(如图2)。
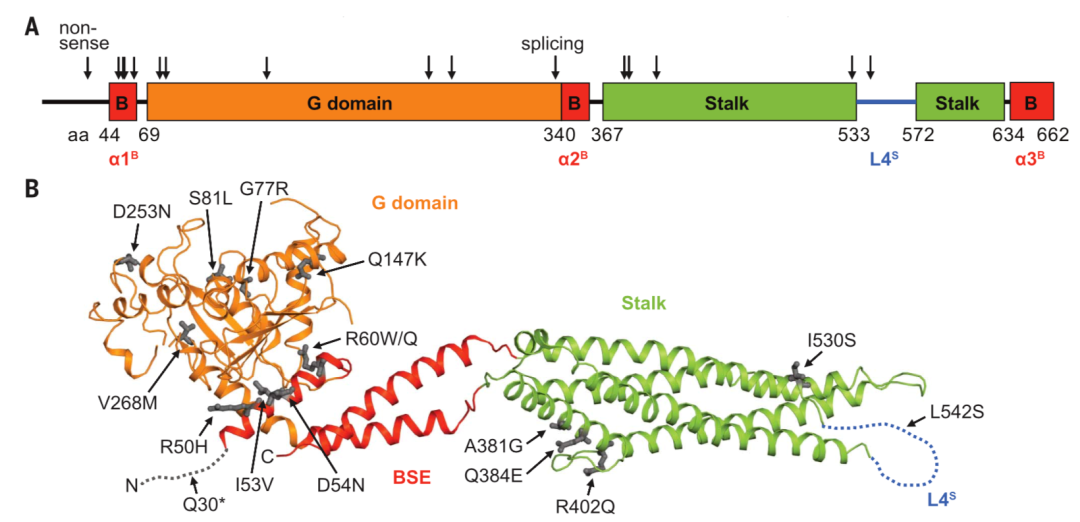
图2.H7N9禽流感病例中发现的17个MX1罕见变异示意图。
随后,作者直接通过病毒聚合酶功能测试和病毒感染测试,研究MxA在抵御H7N9方面的作用。实验设计在人胚胎肾脏293T细胞中共转染H7N9病毒的聚合酶亚基,H7N9的核蛋白编码蛋白和带有荧光素的H7N9基因组,旨在通过荧光强度表征H7N9聚合酶的活性。结果表明,在15个错义突变中,12个表现出抗病毒能力缺失,剩余3个保有一定的抗病毒能力;一个无义突变使抗病毒功能缺失;一个可变剪切位点突变相当于无义突变造成抗病毒功能缺失。聚合酶功能测试与病毒感染测试的结果相一致。综上,17个SNV中有14个突变是明显破坏了MxA的抗病毒功能,这种功能受损可同时见于抵抗H1N1、H5N1和H7N1流感病毒。
作者提到MxA会发生聚合,猜想MxA存在显性负性突变的效应,即一个失去功能的MxA蛋白会影响其他正常的MxA发挥作用。为了验证其猜想,作者在细胞中共转染了突变型的MxA和野生型的MxA。结果表明,12个错义突变的MxA会影响野生型MxA的抗病毒作用,而且随着突变型浓度越高,抗病毒能力被抑制得越强,而一个具有聚合能力缺陷的突变和另一个stalk截短突变并没有对野生型MxA产生影响。通过免疫共沉淀证明所有12个错义突变MxA与野生型的MxA有物理上的结合,而聚合能力缺陷的突变体并不会与其他野生型MxA结合,作为单聚体的这个突变MxA仍然具有抗病毒能力。
最后,作者表示,如果仅考虑这12个错义突变,MX1基因仍然与H7N9感染有显著相关。
与以前的相关研究相比,该研究依据科学分组,合理的入组人群,采用全基因组测序技术,充分利用华大领先的综合科技服务能力及独特的分析方法优势,最终发现MX1罕见遗传变异增加了人感染H7N9禽流感病毒风险,其影响的程度与单基因病遗传模式相当。研究结果为将来筛查和监测高危人群提供了科学依据,促进了传染病精准防控。
该研究得到国家重点研发计划和深圳市科技计划项目的支持。中山大学公共卫生学院(深圳)陈永坤博士、德国弗莱堡大学博士后Laura Graf、中国疾病预防控制中心病毒病预防控制所陈涛副研究员和中山大学公共卫生学院(深圳)博士研究生廖启军为论文共同第一作者,中山大学公共卫生学院(深圳)舒跃龙教授、德国弗莱堡大学 Martin Schwemmle 教授和中国疾病预防控制中心病毒病预防控制所王大燕研究员为共同通讯作者。华大基因科技服务陈颖和沈娟深度参与了该项目,主要负责生物信息分析。
作为全球领先的生命科学前沿机构,华大因“人类基因组计划”而成立,先后完成了多项具有国际先进水平的基因组科研工作,奠定了中国基因组科学在国际上的领先地位。近年来,华大基因更是助力了中国代谢解析计划ChinaMap和万例卒中患者队列项目,在人群大队列项目中积累了丰富经验。
华大基因提供针对全基因组重测序(WGS)的完整解决方案,包括可替代genotyping arrays的低深度全基因组测序(Low Pass WGS)、可解决大队列项目需求的常规全基因组测序(Standard WGS)、可实现完美基因组标准化的stLFR WGS(Long Fragment Read WGS)等。
· END ·
 热文推荐
热文推荐

喜欢就点个“在看”吧!



 个人中心
个人中心
 我是园区
我是园区




