Nature子刊发表!AI为快速开发抗AD药物提供全新策略
收藏
关键词:
新策略
资讯来源:医药观澜 + 订阅账号
发布时间:
2022-01-12
近日,德睿智药与奥斯陆大学、澳门大学、帝国理工等团队在《Nature Biomedical Engineering》发表一篇研究论文。该研究建立了一种基于人工智能(AI)融合多维分子信息的虚拟筛选算法,并结合细胞、线虫、小鼠多物种阿尔茨海默病(AD)模型验证,成功快速筛选获得具有AD治疗潜力的中药小分子化合物。该研究针对AD治疗,提出了一种高效可行的基于AI的药物发现方案,为快速开发抗AD药物提供全新策略。
国际阿尔茨海默病研究权威、美国麻省理工学院大脑与认知科学系教授蔡立慧(Li-HueiTsai,MIT)指出:“此研究使用前沿的机器学习算法成功发现新神经元线粒体自噬诱导剂,应用计算机筛选候选药物,再使用细胞、秀丽隐杆线虫和表达人类P301L Tau 蛋白的小鼠模型的多个系统中验证,最终发现2种小分子化合物山奈酚和丹叶大黄素。值得注意的是,这些线粒体自噬诱导剂能有效改善神经元功能,减少了AD相关病理变化,并在动物模型中增强了学习记忆能力。因此,该研究通过计算机药物筛选,并通过多系统验证,从而确定了有效的线粒体自噬诱导剂。此外,他们的研究说明了线粒体自噬在神经元的保护作用和改善记忆功能方面的治疗价值。”
阿尔茨海默病是一种渐进的神经系统疾病,损害思维,记忆和独立性,导致过早死亡。这种疾病是一种日益严重的全球健康危机,影响患者和他们的家人。根据《柳叶刀》2020年发布的一项报告,全球约有5000万人患有痴呆症,预计这一数字到2050年将增加到1.52亿。由于疾病具体机制不明,这一领域的药物研发异常艰难。因此,目前亟需发现新的AD治疗机制与更高效的AD药物研发方案。
研究表明,线粒体自噬在AD中扮演着重要角色。
线粒体自噬是细胞进化过程中产生的一种通过自噬选择性清除受损线粒体的机制,及时清除损伤的线粒体对维持细胞正常生理功能具有重要作用。AD患者的神经元中,当Aβ和Tau积累时,线粒体发生损伤,轻微损伤的线粒体通过分裂融合,保证部分子代线粒体内部环境的稳定,而严重损伤的子代线粒体则通过被自噬体包被,选择性线粒体自噬过程予以清除。当此功能受阻时,神经元中出现显著的线粒体运输、动力学异常等功能障碍,导致AD病理改变加重。
项目组前期发表于《Nature Neuroscience》的一项研究中发现:增强线粒体自噬可以抑制Aβ和Tau蛋白的聚集,并逆转AD模型中的认知缺陷。该研究证明线粒体清除机制受损在AD发病过程中扮演关键角色,对线粒体自噬的调控可能为AD的治疗提供新方法。但是目前线粒体自噬的激动剂较稀少,需要更高效的激动剂发现方案。
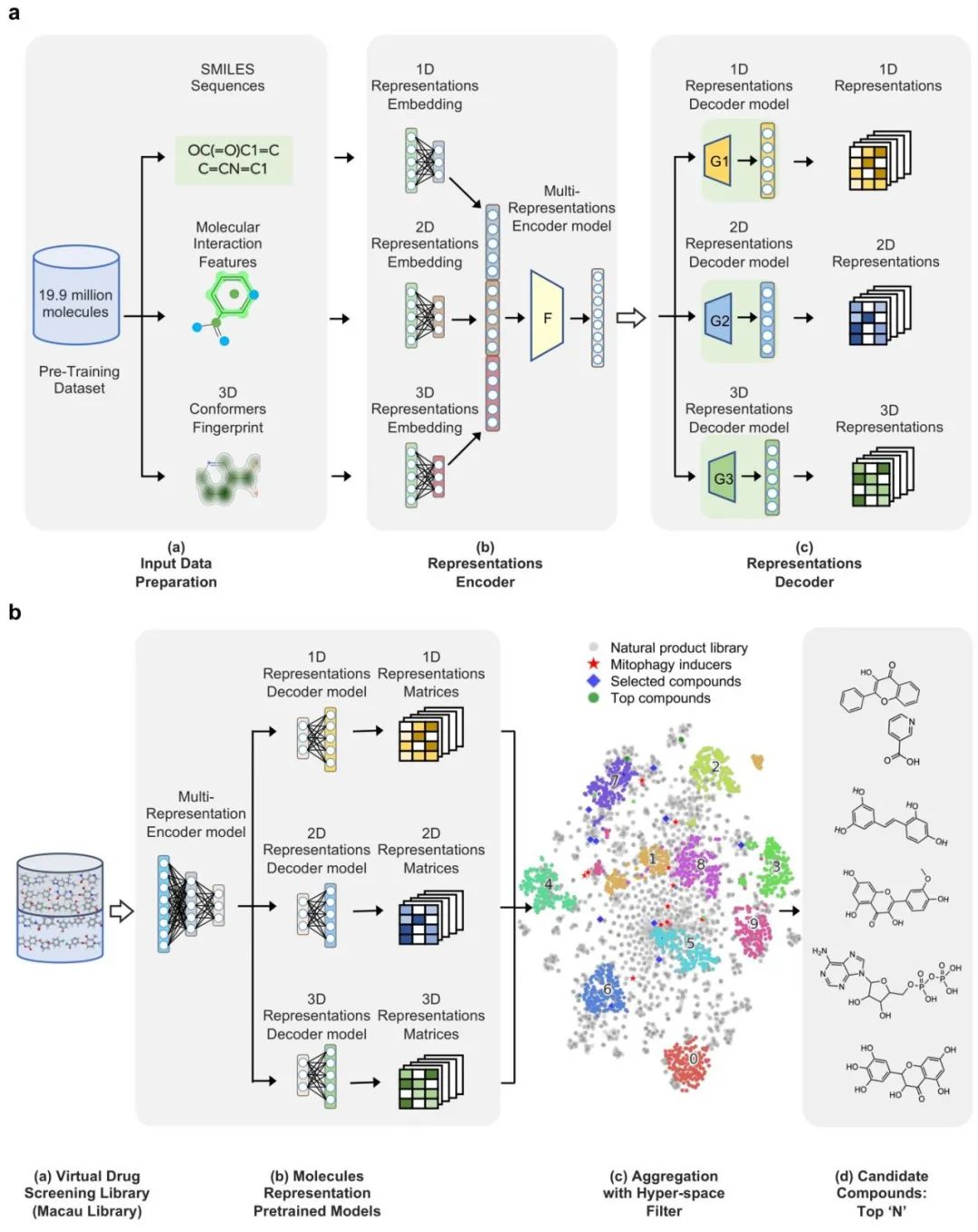
在这项研究中,研究团队引入了机器学习方案,为了获得全面的分子表征,对每个分子的一维、二维与三维信息进行了表征学习
(图一)。基于预训练模型所获得向量,研究团队对澳门大学天然分子数据库中共3724个天然小分子和14个已知的线粒体自噬诱导剂进行了聚类与过滤,共筛选出18个天然小分子进入湿实验验证阶段。
图一:AI筛选小分子流程
之后,研究团队使用人类赫拉细胞模型和线虫动物模型验证了这些小分子的自噬诱导作用
(图二)。
图二:AI筛选分子在细胞模型中的自噬诱导作用
随后,研究团队
通过AI模型,成功发现了两种有明显线粒体自噬诱导作用的天然小分子——山奈酚和丹叶大黄素(图三)。
图三:AI筛选分子在动物模型中的自噬诱导作用
在进一步试验中,研究人员继续使用山奈酚和丹叶大黄素对过表达Aβ和Tau的线虫动物模型进行治疗,发现治疗后线虫的学习行为得到明显改善
(图四)。具体机制方面,研究人员通过建立细胞模型,发现
山奈酚对自噬调通作用受到pdr-1和dct-1基因决定性影响,丹叶大黄素对自噬调控作用影响受到pink-1的影响。
图四:AI筛选分子在动物模型中的自噬诱导作用
除了线虫模型外,研究人员还在小鼠模型中发现,持续两个月的山奈酚和丹叶大黄素治疗后,AD小鼠空间学习和记忆能力、视觉识别记忆能力有了明显的提升(图五),并且小鼠大脑中自噬标志物由降转升,海马区域的Aβ产生和Tau的聚集明显降低。
图五:AI筛选分子对AD动物模型的治疗效果
另外,研究人员还将AI模型与其他机器学习方法进行比较,结果显示,研究中所使用的AI模型最为准确,且其他方法推介的化合物均无法在神经元中诱导线粒体自噬(图六)。
图六:AI虚拟筛选模型与其他筛选方法对比
本文建立了一种基于AI融合多维分子信息的虚拟筛选算法。基于该算法成功筛选出多个自噬诱导剂和生物学实验证明了筛选出的化合物具有治疗阿尔茨海默病的潜力。该研究证明了增强自噬机制在阿尔茨海默病治疗中的潜力,同时为快速开发阿尔茨海默病药物提出了一种基于AI的可行框架方案。
本文由药明康德内容团队根据公开资料整理编辑,欢迎个人转发至朋友圈。转发授权请在「医药观澜」微信公众号留言联系我们。其他合作需求,请联系wuxi_media@wuxiapptec.com。
免责声明:药明康德内容团队专注介绍全球生物医药健康研究进展。本文仅作信息交流之目的,文中观点不代表药明康德立场,亦不代表药明康德支持或反对文中观点。本文也不是治疗方案推荐。如需获得治疗方案指导,请前往正规医院就诊。











 个人中心
个人中心
 我是园区
我是园区




