「 本文共:16条资讯,阅读时长约:3分钟 」


北海康成GBM新药上II期临床。北海康成CAN008注射液在国内开展的用于治疗胶质母细胞瘤(GBM)的II期临床首例患者给药。该项研究将在标准治疗(放疗加替莫唑胺)的基础上,评估CAN008与安慰剂治疗的有效性与安全性,并探索临床相关生物标志物。CAN008是一款CD95靶向创新生物药,已分别获得FDA和EMA授予用于治疗胶质母细胞瘤的孤儿药资格;欧洲药品管理局已将CAN008纳入PRIME(优先药物)计划。




1.首个儿童弱视数字疗法获批上市。Luminopia公司数字疗法Luminopia One获FDA批准上市,作为处方疗法,用于改善4-7岁弱视儿童视力。Luminopia One通过虚拟现实 (VR) 设备以不同的方式向患儿呈现经专有算法修改过的电视和电影内容,旨在重新平衡患儿双眼,加强视觉处理,训练患者两只眼睛的协同使用。这是FDA批准的首个治疗儿童弱视的数字疗法,也是神经视觉障碍领域首个获批的数字疗法。
2.礼来长效降糖药在欧美报产。礼来宣布已分别向FDA和欧盟EMA提交了糖尿病新药tirzepatide的上市申请。该公司同时使用一张优先审评券,向FDA寻求加快批准tirzepatide上市。该新药是一种新型的每周1次皮下注射给药的GLP-1R/GIPR双重激动剂。在一项与司美格鲁肽“头对头“的III期临床SURPASS中,Tirzepatide的降糖减重效果优于司美格鲁肽。tirzepatide已在全部5项国际Ⅲ期临床中达到主要终点。
3.诺华CD19 CAR-T新适应症报sBLA。诺华宣布,FDA和欧洲药品管理局已分别受理CD19 CAR-T细胞疗法Kymriah(tisagenlecleucel)的补充生物制品许可申请(sBLA)和II类变更,用于治疗先前接受过至少2种疗法的复发或难治性滤泡性淋巴瘤成人患者。FDA同时授予该sBLA优先审查资格。Kymriah是FDA批准的首个CAR-T细胞疗法,目前已获批用于治疗复发或难治性急性淋巴细胞白血病,和复发或难治性弥漫性大B细胞淋巴瘤的治疗。
4.创新蛋白降解疗法早期临床积极。Kymera公司IRAK4蛋白降解疗法KT-474在Ⅰ期临床中获积极中期结果。在健康志愿者中,单剂KT-474剂量依赖性降低IRAK4水平,最高3种剂量的KT-474能将外周血单核细胞(PBMC)中的IRAK水平降低93-96%;最高两个剂量的KT-474在24-48小时后显著降低TLR受体激动剂激发的多种促炎症细胞因子水平,最大降幅可达到97%;而且KT-474表现出良好的安全性和耐受性。
5.BTK蛋白降解剂早期临床积极。Nurix公司开发的、具有双重活性的口服BTK蛋白降解剂NX-2127,在治疗复发性B细胞血液恶性肿瘤的Ⅰ期临床中获积极结果。不论患者初始BTK水平如何,NX-2127(100 mg或200 mg)均显著降低外周血中的BTK水平,降幅分别超过80%和90%。其中,有1例患者在最近一次的评估中显示出部分缓解,多项临床指标也持续改善。NX-2127安全性可控,无剂量限制性毒性。
6.武田宣布收购γδT细胞疗法平台。武田行使收购GammaDelta Therapeutics公司的选择权,将获得GammaDelta的γδT细胞疗法平台,包括基于血液和组织来源的γδT细胞亚群Vδ1+细胞的同种异体细胞免疫疗法项目。γδT细胞不需要借助主要组织相容性复合体(MHC)呈递抗原就可以识别肿瘤细胞,因此肿瘤细胞无法通过下调MHC蛋白的表达来逃避它的攻击。这一独特的机制让肿瘤细胞“无处可逃”。


1.浙江将动态调整医疗服务价格。浙江省印发《关于建立医疗服务价格动态调整机制的实施意见》提出,建立灵敏有度的医疗服务价格动态调整机制,开展医疗服务价格动态调整工作。《意见》还对医疗服务价格动态调整设置了约束标准,其中规定,如果出现“上年地区医疗收入增幅高于10%,或上年地区门诊(或住院)均次费用增幅高于5%”等情况,不得启动医疗服务价格动态调整。
2.湖北商保“一站式”结算平台上线。10月26日,湖北省首家商保“一站式”结算平台在湖北省人民医院(武汉大学人民医院)正式上线。该平台上线后,商保患者就诊结束后,保险公司即可实时完成智能理算,并将赔付资金直接转到医院,患者出院结算时,只需补齐扣除医保和商保报销后的差额即可。平台目前已接通平安人寿、富德生命、太平洋寿险等多家保险公司。
3.军人配偶将获免费医疗。中央军委办公厅日前印发《军人及军队相关人员医疗待遇保障暂行规定》,自2022年1月1日起施行。《规定》明确军人及军队相关人员在军队医疗机构就医的医疗待遇,界定军人跨军地就医的具体情形,打通远离军队医疗机构单位军人及其家属就近就便到驻地医疗机构就医渠道,实现军人配偶免费医疗、军官军士父母和配偶父母优惠医疗,继续实行军人、军人未成年子女免费医疗,充分体现军人职业尊崇。
4.美国拟针对免疫低下者接种第四针新冠疫苗。美国疾控中心(CDC)日前发布最新防疫指南,宣布中重度免疫功能低下人群(包括正在治疗白血病或肿瘤的患者、器官移植接受者、晚期或未经治疗的艾滋病毒感染者)在打完第三针新冠疫苗的6个月后,可以接种第四针。今年8月CDC正式批准18岁及以上免疫功能低下者接种第三针新冠疫苗,因此最早打完第三针的接种者最快明年2月才能接种第四针。


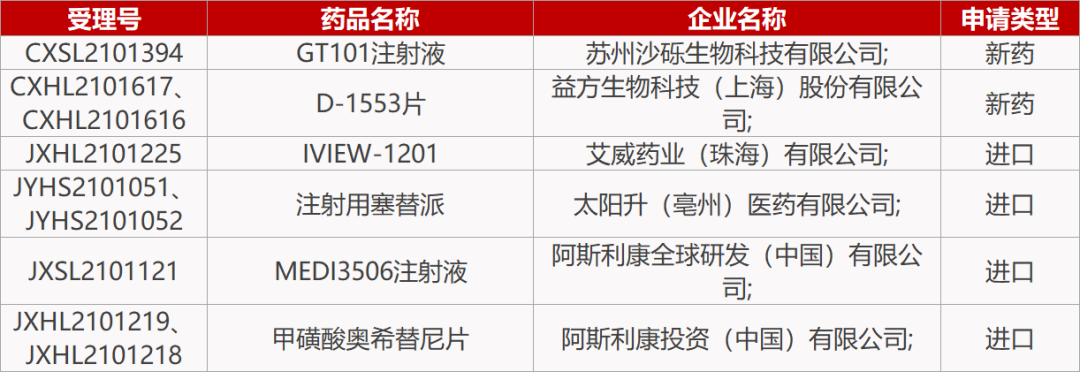
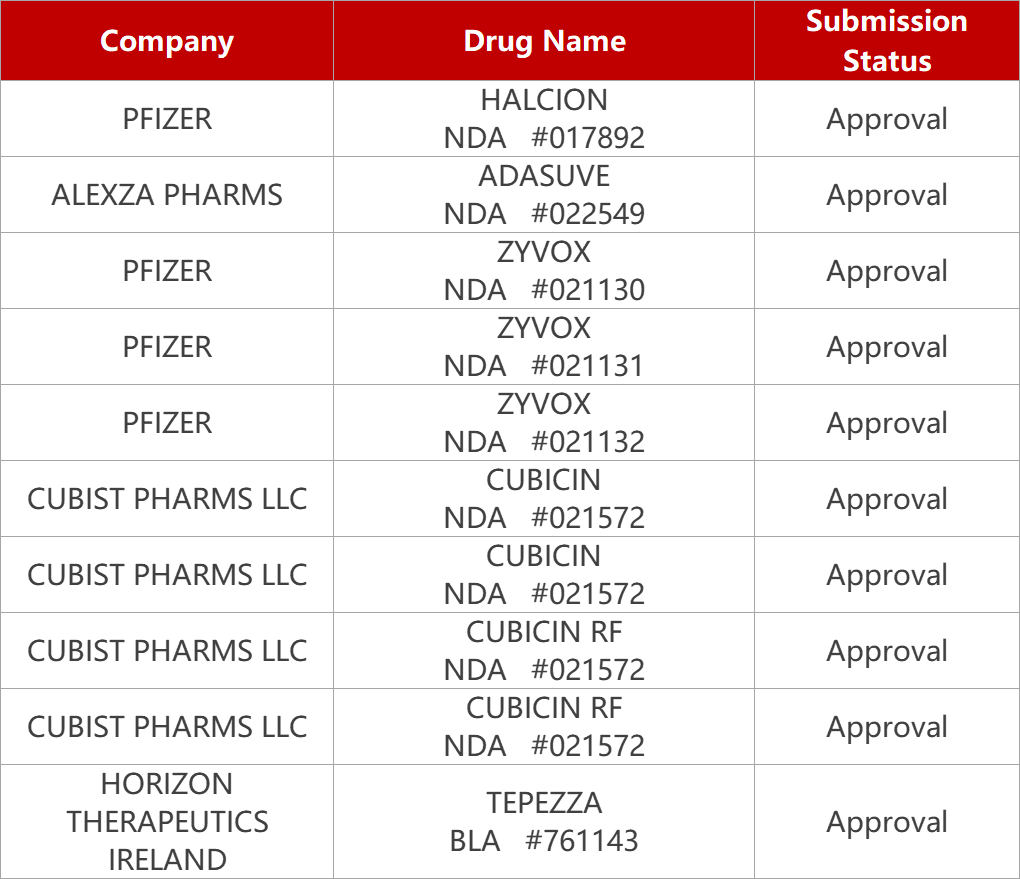


【恒瑞医药】公司收到国家药品监督管理局核准签发关于 SHR0410 注射液、SHR8554注射液的《药物临床试验批准通知书》,将于近期开展临床试验。
【佰仁医疗】公司在研产品限位可扩张人工生物心脏瓣膜注册申请获国家药品监督管理局正式受理。
【长江健康】公司旗下二级子公司海南海灵化学制药有限公司主要产品注射用拉氧头孢钠已通过仿制药质量和疗效一致性评价。
- The End -




 个人中心
个人中心
 我是园区
我是园区




