▎药明康德内容团队报道
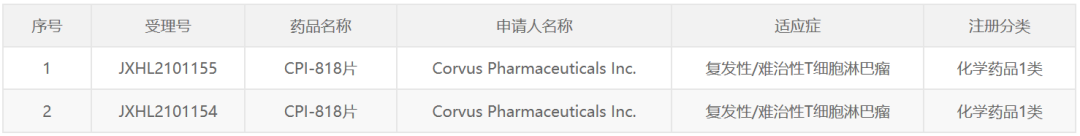
10月26日,和剂药业宣布,其ITK抑制剂口服用CPI-818的临床试验申请已获得中国国家药监局药品审评中心(CDE)临床试验批件,拟用于复发/难治性T细胞淋巴瘤。根据新闻稿,这也是和剂药业获得的首个临床试验批件,和剂药业拥有CPI-818 大中华区权限。
白细胞介素-2(IL-2)诱导酪氨酸激酶(ITK),于1992年首次被发现,分子量为72kDa,其在Th2细胞的激活、分化和增殖中发挥必不可少的作用。T细胞淋巴瘤属于非霍奇金淋巴瘤的罕见亚型,具有侵袭性的、异质性等特点。目前已证实,ITK在T细胞的信号传导、分化、发育和细胞因子生成中发挥关键作用。因此ITK成为治疗T淋巴细胞增生性疾病中极具潜力的靶点。
CPI-818正是一种ITK抑制剂。它能够强效抑制ITK激酶并具有高度选择性,同时不影响正常T细胞的增殖以及免疫反应。
此前,CPI-818已在美国、韩国、澳大利亚进行的首次人体临床试验中,显示出了一定疗效和良好的安全性及耐受性。
截至2021年2月17日,全球共有25例患者(剂量递增阶段16例,扩展阶段9例)接受了CPI-818的治疗。在剂量递增期间未观察到剂量限制性毒性(DLT)。在原发性皮肤T细胞淋巴瘤(CTCL)患者中,1例CTCL-Sezary综合症患者的靶淋巴结出现缩小,且无正子造影(FDG)活性病灶,淋巴结达到完全缓解(CR)。在剂量递增阶段,接受了CPI-818 ≥ 200mg BID(每日两次)治疗的7例外周T细胞淋巴瘤非特指型(PTCL-NOS)患者中,有2例患者达到了缓解。其中1例PTCL-NOS患者达到持续15个月的完全缓解,1例患者出现持续5个月的经确认的部分缓解(PR)并在PR期间成功接受同种异体移植。

和剂药业共同创始人,董事长Richard Miller博士表示:“很高兴CPI-818在中国获批临床,中国以外的临床数据初步证明了其在多个T细胞淋巴瘤亚种患者带来临床获益的潜力,我们将与中国淋巴瘤领域专家一起,全力推进CPI-818临床试验的进展,争取尽早在中国获批上市,为复发/难治性T细胞淋巴瘤患者带来革命性的解决方案,满足亟待解决的临床需求。”
中国临床肿瘤学会(CSCO)理事,CSCO抗淋巴瘤联盟秘书长,北京大学肿瘤医院淋巴瘤科宋玉琴教授表示:“复发/难治性T细胞淋巴瘤是非霍奇金淋巴瘤临床工作中的一大难题,目前多数患者的五年生存率仅在10-30%。我们非常高兴看到和剂药业将全新靶点的ITK抑制剂带到中国,希望产品在国内的临床开发进展顺利,期待能够早日上市,给众多复发/难治性T细胞淋巴瘤患者带来福音。”
根据新闻稿,和剂药业是一家致力于肿瘤和自身免疫性疾病的创新药公司。该公司于2020年10月完成2.8亿人民币A轮融资,由贝达基金、海正药业、檏盛投资等共同投资。目前,和剂药业拥有针对ITK靶点的抑制剂CPI-818,针对CD73的人源化单克隆抗体CPI-006,针对腺苷A2A靶点的拮抗剂CPI-444的三个临床阶段管线药品的大中华区权限,以及新一代BTK抑制剂的全球商业权限及专利权。
[1]和剂药业-全球首个进入临床阶段的ITK抑制剂IND获临床试验批件. Retrieved Oct 26,2021, from https://www.prnasia.com/story/337828-1.shtml
本文由药明康德内容团队根据公开资料整理编辑,欢迎个人转发至朋友圈。转发授权请在「医药观澜」微信公众号留言联系我们。其他合作需求,请联系wuxi_media@wuxiapptec.com。
免责声明:药明康德内容团队专注介绍全球生物医药健康研究进展。本文仅作信息交流之目的,文中观点不代表药明康德立场,亦不代表药明康德支持或反对文中观点。本文也不是治疗方案推荐。如需获得治疗方案指导,请前往正规医院就诊。







 个人中心
个人中心
 我是园区
我是园区




