「 本文共:15条资讯,阅读时长约:3分钟 」




1.礼来两款1类新药在华获批临床。礼来申报的两款1类新药获CDE临床许可,分别是PD-1激动剂peresolimab注射液(LY3462817),拟开发用于中重度活动性类风湿关节炎;PI3Kα H1047R抑制剂LOXO-783片,拟开发用于治疗PIK3CA H1047R突变的晚期乳腺癌和其它实体瘤。LY3462817是一款具“first-in-class”潜力的单抗药物,可与人类PD-1结合并作为其激动剂,抑制淋巴细胞的激活和扩增。目前LY3462817用于治疗类风湿性关节炎正处于Ⅱ期临床开发。
2.蓝盾MSLN靶向CAR-T获批卵巢癌IND。南京蓝盾生物申报的1类生物制品“LD013自体T细胞注射液”获国家药监局临床许可,拟用于治疗复发性卵巢癌。LD013是一款靶向间皮素(MSLN)的自体CAR-T细胞治疗产品,已在研究者发起的临床研究(IIT)中显示出良好的疗效和安全性,用药后卵巢癌患者肿瘤显著消退,且未观察到2级以上的细胞因子风暴、神经毒性和CAR-T相关的输液反应。
3.天泽云泰眼科基因疗法获批BCD临床。天泽云泰生物自主研发的1类生物制品VGR-R01获国家药监局临床默示许可。VGR-R01是一款针对CYP4V2基因突变导致的结晶样视网膜变性(BCD)患者的基因替代疗法,通过回补正确拷贝的CYP4V2基因,介导RPE细胞表达CYP4V2蛋白,旨在恢复患者视网膜内的脂肪酸代谢障碍,保护视力。VGR-R01也是该公司第二款获批临床的基因治疗产品。今年4月,天泽云泰血友病B基因疗法VGB-R04注射液已获得CDE的临床批件。
4.康方PD-1/LAG-3双抗获批临床。康方生物1类生物药AK129获国家药监局临床试验默示许可,拟开发用于治疗晚期恶性肿瘤。AK129是一款PD-1/LAG-3双特异性抗体,可阻断PD-1与其配体PD-L1和PD-L2的结合,以及阻断LAG-3与其配体MHCII等的结合,解除肿瘤微环境中的免疫抑制。临床前研究显示,与PD-1抗体和LAG-3抗体联合疗法相比,AK129可介导更强的免疫激活,具有更好的抗肿瘤活性。
5.歌礼新冠口服药在美报IND。歌礼制药宣布已向FDA递交口服小分子3CLpro抑制剂ASC11的新药临床试验(IND)申请。抗新冠病毒细胞实验显示,ASC11的抗病毒活性(EC90)为奈玛特韦的31倍 (155/5),S-217622的120倍(600/5),PBI-0451的16倍(78/5)以及EDP-235的7倍 (33/5);而且,ASC11对奥密克戎变异株如BA.1和BA.5均保持活性。目前,歌礼已在全球范围内递交多项ASC11和相关化合物及其治疗病毒性疾病用途的专利申请。


1.辉瑞RSV母体疫苗Ⅲ期临床积极。辉瑞双价RSV候选疫苗PF-06928316(RSVpreF)用于产妇主动免疫来预防婴儿出生后感染RSV相关下呼吸道疾病(MA-LRTI)的Ⅲ期临床MATISSE结果积极。中期分析显示,PF-06928316避免婴儿出生后90天内以及出生后6个月内感染MA-LRTI的保护力分别为57.1%(CI:14.7-79.8%)和51.3%(CI:29.4-66.8%),不具显著性;但该疫苗避免婴儿出生后90天内以及出生后6个月期间感染严重性MA-LRTI的保护力分别达到81.8%(CI:40.6-96.3%)和69.4%(CI:44.3-84.1%)。辉瑞预计年底向FDA递交生物制品许可申请。
2.CD45靶向放射疗法Ⅲ期临床积极。Actinium公司CD45靶向性放射疗法Iomab-B用于急性髓系白血病(AML)的关键Ⅲ期临床SIERRA中达到主要终点。Iomab-B是由单克隆抗体apamistama和放射性同位素碘-131组成,旨在通过快速耗尽血癌患者体内的癌细胞、免疫细胞和骨髓干细胞来改善患者获得骨髓移植治疗的机会。该项试验结果显示,Iomab-B治疗组与对照组相比,有更多患者获得长达6个月的持久完全缓解(P<0.0001)。Actinium公司计划尽快向FDA递交BLA申请。
3.Bcl-xL抑制剂眼科Ⅱ期临床积极。UNITY Biotechnology公司细胞凋亡抑制蛋白Bcl-xL抑制剂UBX1325用于治疗糖尿病性黄斑水肿的Ⅱ期临床BEHOLD达到主要终点。单次注射24周后,UBX1325组患者的平均最佳校正视力较基线增加6.2个ETDRS视力表字母(假性注射组则减少1.4个字母,p=0.0084),患者黄斑中心凹视网膜厚度(CST)的改善持续24周(假性注射组患者则呈现恶化情形),患者6个月期间无需接受标准治疗的比例达到59.4%(vs37.5%)。UBX1325总体耐受性良好。
4.CD20靶向CAR-T血液瘤早期临床积极。Mustang Bio公司CD20靶向CAR-T疗法MB-106用于治疗多种血液瘤的最新Ⅰ/Ⅱ期临床结果积极。在包括B细胞非霍奇金淋巴瘤(B-NHL)、滤泡性淋巴瘤(FL)、弥漫性大B细胞淋巴瘤(DLBCL)、慢性淋巴细胞白血病等血液瘤中,MB-106总缓解率(ORR)达到 96%(27/28),完全缓解率 (CR) 为 75%(21/28);两例WM患者的ORR和CR均为100%;MB-106具有良好的耐受性。
5.Hi-Bio公司融资推进两款免疫疾病精准疗法。Human Immunology Biosciences(Hi-Bio)公司宣布完成1.2亿美元融资,以加速推进CD38抗体felzartamab和C5aR1抗体HIB210的临床开发。Felzartamab通过与CD38结合,可清除浆细胞和浆母细胞,消除导致疾病的自身抗体的来源;目前它正在临床中评估治疗膜性肾病和IgA肾病的潜力。天境生物拥有felzartamab在大中华区的开发权益,以及HIB210在大中华区和韩国的开发权益。
6.强生近166亿美元收购Abiomed公司。强生宣布将以约166亿美元收购Abiomed。Abiomed开发了用于治疗冠状动脉疾病和心力衰竭的Impella心脏泵产品组合。此次收购,提升了强生在医疗器械(Johnson & Johnson MedTech)心血管创新者地位,为推动心血管疾病突破性治疗提供一个战略平台,帮助全球更多的患者。这项交易将加速实现心脏康复的全球护理标准。


1.兰大预测猴痘疫情年底将蔓延全球。兰州大学疫情预测团队近日在medRxiv预印本平台发表《猴痘疫情全球预测》,结果表明猴痘疫情将于2022年底蔓延到全球各国,届时全球累计猴痘感染病例总数将达到10万例。排名前五的国家分别是美国、巴西、西班牙、法国和英国,病例数分别超过2.8万、2.0万、0.75万、0.45万和0.4万例。如果30%的人口接种疫苗,猴痘感染人数将会下降35%。
2.上海启动医疗行业专项整治工作。上海市卫健委日前印发《上海市2022年纠正医药购销领域和医疗服务中不正之风工作要点》,明确深入开展医疗领域乱象治理、严厉打击医药购销领域非法利益链条等五大工作任务。《工作要点》强调,从“标本兼治”两个维度坚决惩治“红包”、回扣等行风问题;严肃查处医疗机构工作人员利用职务、身份之便直播带货。
3.郑州卫健委:新冠是自限性疾病。郑州市卫健委官方微信公众号10月31日发布《新冠肺炎不可怕,可防可治,郑州权威专家来解答》一文介绍,郑州市卫健委邀请郑州市第一人民医院、郑州市疾病预防控制中心以及郑州市中医院专家,就新冠肺炎疫情防控有关问题进行解答。专家表示,新冠病毒感染是自限性疾病,大家不用过于惊慌。感染后根据病情、症状等情况,在专科医生指导下进行治疗。同时保证充足睡眠,多饮开水,保持心情舒畅,规律饮食,有助于疾病的快速恢复。


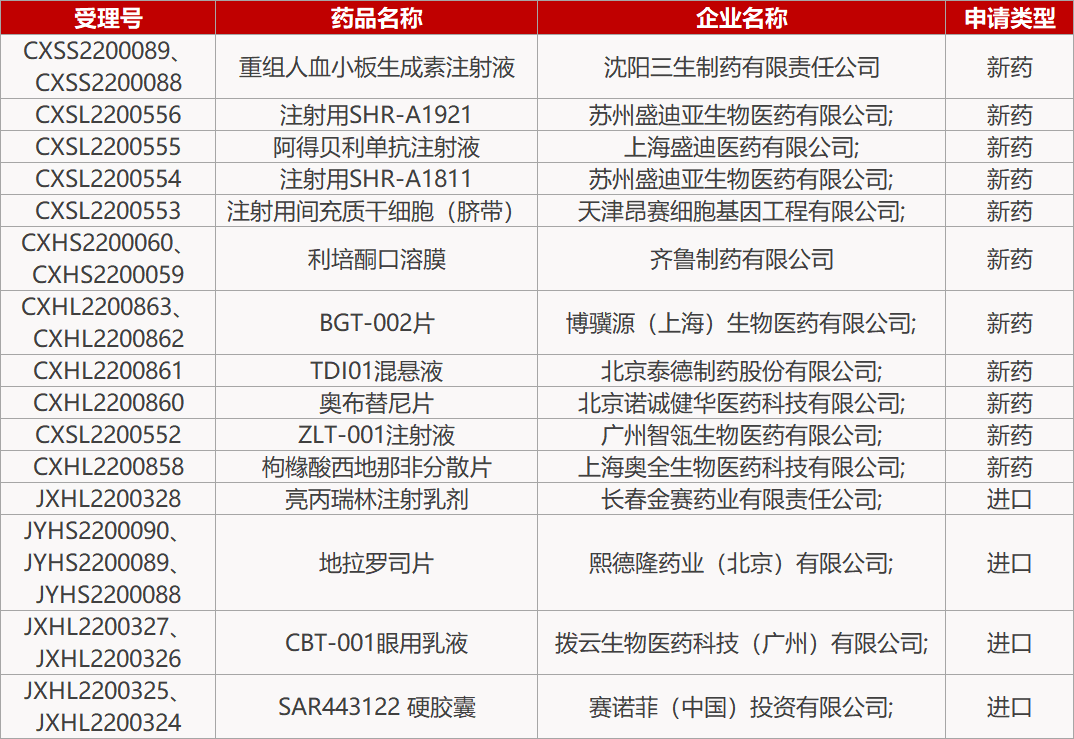


【安科生物】公司与控股子公司合肥瀚科迈博共同申报的PD-L1/4-1BB双特异性抗体“HK010注射液”获批临床,拟定适应症为晚期恶性肿瘤。
【上海医药】控股子公司上海上药中西制药“甲磺酸雷沙吉兰舌下膜”获批药物临床试验,拟用于原发性帕金森病患者的单药治疗,以及伴有剂末波动患者的联合治疗(与左旋多巴合用)。
【人福医药】控股子公司宜昌人福药业产品氯巴占口服混悬液获批药物临床试验,用于2岁及以上Lennox-Gastaut综合征(LGS)患者癫痫发作的联合治疗。
- The End -




 个人中心
个人中心
 我是园区
我是园区




