
“一位品学兼优的七岁小女孩,已经为自己安排好了身后事”,这部有关白血病的公益电影令上亿观众潸然泪下,同时也引发了科学、医学界人士的深思。 图|《天堂的张望》中白血病患者(来源:影片截图)
图|《天堂的张望》中白血病患者(来源:影片截图)
该部名为《天堂的张望》的影片于 2020 年 11 月上映,讲述了一位患急性白血病小女孩在化疗期间的痛苦经历,当她得知需要 30 万天价花费时,毅然决定放弃治疗。“白血病”,给患者的身心都造成了严重的打击。
白血病就像 “恶魔” 一样严重威胁着人类的健康,无论是成人还是儿童。截至目前,化疗仍然是临床上治疗白血病的主要方式,这种治疗方式中所用的药物,包括抗代谢类、烷化剂、生物碱类等,在杀灭白血病细胞的同时也会对正常细造胞造成明显的伤害。
以三氧化二砷为例,该药物是治疗急性早幼粒细胞白血病的一线药物,三价砷(trivalent arsenic,AsIII)主要通过诱导细胞分化和凋亡来发挥抗白血病作用。
然而,临床使用的三氧化二砷,病人注射后会在体内广泛分布,给心脏和肝脏等带来毒副作用,并且难以用于其他白血病的治疗。
为了突破三氧化二砷在临床中的诸多局限,在白血病细胞上寻找新的靶点,并构建相应的靶向递送载体可能成为一种行之有效的方法。中国科学院联合国内多家单位基于可靠的新靶点创建出一种仿生的砷递送载体,可以为多种类型的白血病提供高效治疗方案。
10 月 25 日,相关论文以《基于铁蛋白靶向递送砷至多种类型白血病细胞并显著增强白血病治疗效果》(Ferritin-based targeted delivery of arsenic to diverse leukaemia types confers strong anti-leukaemia therapeutic effects)为题发表在 Nature Nanotechnology 上[1]。 图|相关论文(来源:Nature Nanotechnology)
图|相关论文(来源:Nature Nanotechnology)
由中国科学院过程工程研究所生化工程国家重点实验室研究员马光辉和魏炜、北京大学化学与分子工程学院教授马丁、广州南方医科大学珠江医院血液科教授李玉华担任共同通讯作者。 图|马光辉(来源:中国科学院大学官网)
图|马光辉(来源:中国科学院大学官网)
该研究成果揭示了来自多种白血病类型和病程患者的白血病细胞高表达转铁蛋白受体(transferrin receptor,CD71)靶点,通过 CD71 配体铁蛋白高效装载三氧化二砷,以此靶向递送到不同类型白血病细胞内部,提高三氧化二砷的靶向性和治疗白血病的广谱性。
CD71 有望成为白血病精确疗法的稳定治疗靶点

以往的白血病靶点及递送载体的相关行业消息曾提及,科研人员已在白血病细胞上鉴定出 CD19、CD20 等一系列靶点,但它们的表达特征随白血病类型和病程不同,而有很大差异。
在载体构建方面,基于外源性材料合成载体通常需要长期的安全性论证后才有望进入临床,而复杂的配体偶联过程又为放大生产和质量控制带来了进一步的障碍。
基于上述痛点,找寻更加可靠的新靶点以及创建更加安全和简单的新载体,用于对多种白血病类型的有效治疗,成为业界不得不解决的问题。
针对新靶点,马光辉、魏炜研究团队与南方医科大学珠江医院李玉华团队进行了合作研究,发现 CD71 靶点在急/慢性髓系、急性淋系等白血病中均出现高表达,且在不同进程的白血病中表达也比较稳定。
为了探究白血病细胞是否具有 CD71 高表达性,该团队筛选了健康人体外周血样本和白血病患者骨髓样本中细胞的 CD71 表达水平。 图|采集和流式细胞术分析示意图(来源:Nature Nanotechnology)
图|采集和流式细胞术分析示意图(来源:Nature Nanotechnology)
通过对健康人体样本的初步流式细胞技术分析证实,CD71 在各种细胞类型中的表达非常低。将细胞分布比例和 CD71 表达结合分析,可以发现健康捐献者不同细胞类型 CD71 表达丰都没有差异。
 图|健康人体和患者之间不同 CD71 表达的对比(来源:Nature Nanotechnology)
图|健康人体和患者之间不同 CD71 表达的对比(来源:Nature Nanotechnology)
在临床急性髓系白血病(Acute Myeloid Leukaemia,AML)患者骨髓中,与有核红细胞、淋巴细胞和粒细胞相比,白血病细胞 CD71 阳性表达率高达 90%, CD71 丰度在白血病细胞中也有非常显著的提升。其他类型白血病和不同进程的白血病也表现出相同的规律。
魏炜表示:“我们对白血病患者临床资料的综合分析,证实了 CD71 在急/慢性髓系、急性淋系等白血病中均为高表达,且在不同进程白血病中表达也比较稳定,可以作为白血病治疗药物精准递送的稳定靶点。”
成功制备仿生递送载体,为后续白血病治疗铺平了道路

药物装载方面,由于铁蛋白(Fn)的内腔只有 8 纳米,这对小分子三氧化二砷的高效装载和可控释放方面提出了新的挑战。
马光辉、魏炜课题组和北京大学化学与分子工程学院马丁团队合作,利用铁蛋白一系列独特的性质以及砷与铁之间的相互作用,设计出一种铁预成核的策略,并高效锚定了三价砷,这有助于高细胞毒性 AsIII 离子能够稳定留在铁蛋白的空腔内,进入白血病细胞中的酸性溶酶体后,再特异性释放。
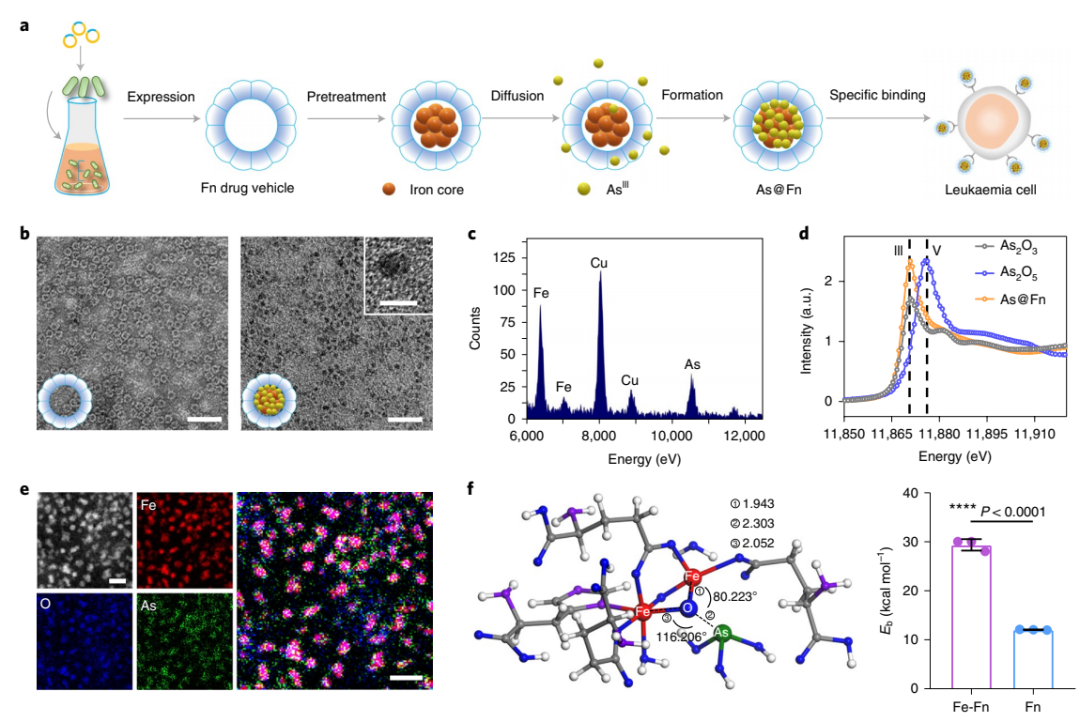 图|As @ Fn 的构建及体外评价部分示意图(来源:Nature Nanotechnology)
图|As @ Fn 的构建及体外评价部分示意图(来源:Nature Nanotechnology)
为了更深入地了解三价砷和氧化铁的结合,该团队与北京化工大学合作,进行了量子力学计算。结果表明,H3AsO3 分子中的As 原子与 Fe-O-Fe 结构的桥氧原子紧密结合,显著高于未添加 Fe 的结合能力,表明形成的 Fe-O-As 纳米配合物具有更高的稳定性。
成功加载 AsIII 后,该团队开始对 HL-60 白血病细胞进行评估。结果显示,Fn 能够通过网格蛋白介导的途径有效地将 As 运送到 HL-60 细胞。 与商业三氧化二砷注射剂相比,As 的摄取可提高 4.5 倍。
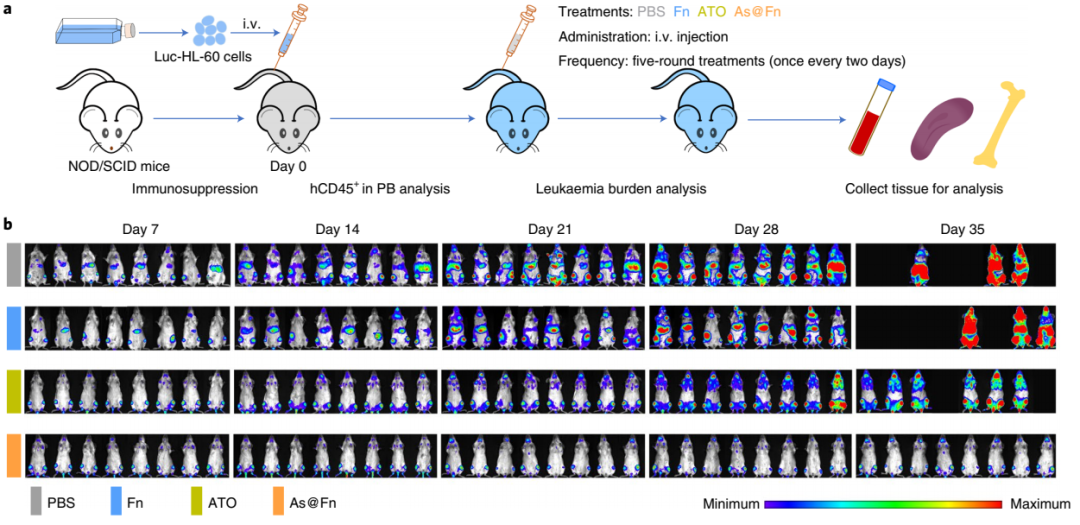 图|HL-60(AML)移植异种移植模型中的抗白血病疗效(来源:Nature Nanotechnology)
图|HL-60(AML)移植异种移植模型中的抗白血病疗效(来源:Nature Nanotechnology)
在此基础上,该团队在小鼠上构建了不同种类的白血病模型。体内分布的结果显示,注射后三氧化二砷静脉在血液中白血病细胞的分布为 12%;装砷铁蛋白在血液中白血病细胞的分布为 65%。体内疗效结果进一步证明,装砷铁蛋白可以有效治疗急/慢性髓系、急性淋系等白血病,并且效果显著优于临床的标准治疗方法。
就该研究而言,还有进一步的提升空间。魏炜表示:“利用本研究发现白血病细胞稳定表达 CD71 的特点,可以进一步在铁蛋白空腔中联合装载化疗药物,通过不同的作用机制克服白血病化疗耐药,这也是我们下一步的研究规划。”
 图|魏炜(来源:魏炜)
图|魏炜(来源:魏炜)下一步,该团队希望进一步考察多发性骨髓瘤、淋巴瘤等其他肿瘤中的 CD71 表达水平,分析铁蛋白装载不同药物在这些肿瘤中的治疗效果。
鉴于铁蛋白为人体内源组分并且三氧化二砷为已批准用药,该试剂在临床转化方面具有很大的发展潜力。据悉,该团队也正在与相关机构进行合作,深度推进该制剂的相关转化。
用工程学理念和技术手段,直面医药领域的挑战

研究生期间,他主要从事多糖药物载体的应用基础研究。博士毕业后留在中国科学院过程工程所工作至今,先后破格晋升为副研究员和研究员。
 图|魏炜(来源:魏炜)
图|魏炜(来源:魏炜)
针对高端创新剂型成药性低的重大挑战,魏炜工作之后进一步提出了仿生剂型工程的策略,将体内组分(如蛋白、外泌体等)的结构和功能巧妙地融入药物载体设计中,使其遵循固有的转运途径在体内实现精准递送。
该策略一方面可以避免使用难以批准的外源性材料,另一方面克服了体内的复杂环境和递送屏障,因而获得了最佳使用效果,而且提高了成药性。
今年以来,马光辉、魏炜课题组的多篇研究成果相继发表在 Nature Nanotechnology、Science Translational Medicine、Nature Biomedical Engineering 等期刊上 [2 ] 。
 图|部分交叉合作成果展示(来源:Nature Biomedical Engineering)
图|部分交叉合作成果展示(来源:Nature Biomedical Engineering)
一系列研究成果的共同点都是紧密围绕临床转化需求,与临床背景的团队深度合作以及优势互补,用工程化技术来解决实际问题。同时,采用临床可转化的材料,通过简单且巧妙的设计,制备安全高效的剂型,以解决药物和疫苗递送过程中的关键科学问题[3]。
马光辉表示:“这几篇文章的发表历时 4 到 11 年不等,中间经历过很多困难,但是团队毅然保持着科研热情,从未放弃。”
魏炜所在的生化工程国家重点实验室以及马光辉团队,给年轻人提供了非常好的发展平台,鼓励青年科研人员提出自己的学术思想进行自由探索。
魏炜表示:“科研之路的困难在所难免,如载体的可控制备、临床样本的收集和分析、患者来源异种移植模型的构建等难题,需要进行科技转化的研究还涉及到更多的人力和经费的问题。面对这些挑战,我们既要有坐冷板凳的精神,也要与多方合作共同解决科研难题。”
未来,魏炜希望用工程学理念和技术手段,解决医药领域的难题,直面挑战,早日造福患者。
-End-

参考:
1.Ding Ma, Guanghui Ma, Wei Wei, Yuhua Li, et al. Nature Nanotechnology,1748-3395 (2021)
https://www.nature.com/articles/s41565-021-00980-7
2.Yong Tao, Di Yu,Wei Wei, et al.Nature Biomedical Engineering 5, 968-982 (2021)
https://www.nature.com/articles/s41551-021-00764-3
3. Guanghui Ma, Wei Wei, Di Yu, Shuang Wang, et al. Science Translational Medicine, eabb6981 (2021)
https://www.science.org/doi/10.1126/scitranslmed.abb6981



 个人中心
个人中心
 我是园区
我是园区




