
一、药物概况
1 、药物介绍
通用名:磷酸奥司他韦胶囊
英文名:Oseltamivir Phosphate Capsules
(2)BCS分类
Ⅰ类

分子式:C16H28N2O4·H3PO4
分子量:410.4
(4)成份性状和理化性质
本品为灰色和淡黄色双色胶囊,内容为白色至黄白色粉末,可含有块状物。
溶解度:1.6×103 mg/L(25℃)
Log P:1;
pKa:7.7;
(5)药代动力学参数

(6)药代动力学特征
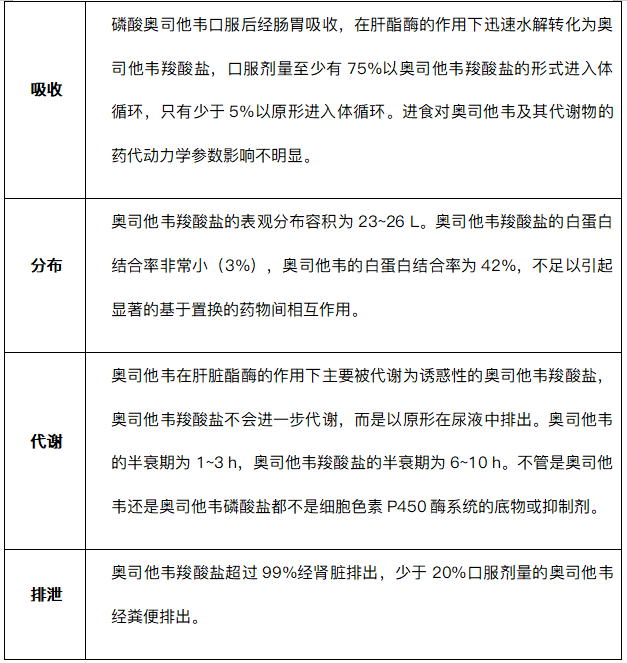
(7)药理作用
磷酸奥司他韦是一种乙酯类前体药物,需要经过水解作用转化成有活性的奥司他韦羧酸盐。奥司他韦羧酸盐是一种流感病毒神经氨酸苷酶的抑制剂,影响病毒颗粒的释放。
(8)转运体及代谢酶
转运体:MRP4(底物)、PEPT1(底物)、OAT3(底物);
代谢酶: 酯酶,非P450酶系的底物与抑制剂。
(9)药物相互作用
与流感疫苗的相互作用:尚无磷酸奥司他韦和减毒活流感疫苗相互作用的评估。但由于两者之间可能存在相互作用,除非临床需要,在使用减毒活流感疫苗两周内不应服用磷酸奥司他韦,在服用磷酸奥司他韦后48 小时内不应使用减毒活流感疫苗。因为磷酸奥司他韦作为抗病毒药物可能会抑制活疫苗病毒的复制。三价灭活流感疫苗可以在服用磷酸奥司他韦前后的任何时间使用。
与肾小管竞争分泌相关的药物相互作用不可能有重要的临床意义,因为大部分药物的安全范围较宽,磷酸奥司他韦活性代谢产物的排泄有肾小球滤过和肾小管分泌两个途径,而且这两个途径的清除能力是很大的。但与同样由肾脏分泌且安全范围窄的药物(如氯磺丙尿、甲氨喋呤、保泰松)合用要慎重。
药理和药代动力学研究数据表明,磷酸奥司他韦和其它药物之间基本上没有明显临床意义的相互作用。
(10)适应症
1.用于成人和1岁及1岁以上儿童的甲型和乙型流感治疗(磷酸奥司他韦能够有效治疗甲型和乙型流感,但是乙型流感的临床应用数据尚不多)。患者应在首次出现症状48小时以内使用。
2.用于成人和13岁及13岁以上青少年的甲型和乙型流感的预防。
(11) 不良反应
① 临床研究经验
偶见 (不良反应发生率在0.1%~5%):恶心,呕吐, 腹泻,支气管炎,腹痛,头晕,头痛,咳嗽,失眠,眩晕,疲乏。
全身:脸部或舌部肿胀、变态反应、过敏反应/过敏样反应、体温过低;
皮肤:皮疹、皮炎、荨麻疹、湿疹、中毒性表皮坏死松解症、Stevens-Johnson 综合症、多形性红斑;
消化系统:肝炎、肝功能检查异常;
心脏:心律失常;
胃肠道:胃肠道出血、出血性结肠炎;
神经:癫痫发作;
代谢:糖尿病恶化;
精神:行为异常、谵妄,包括以下症状,如幻觉、易激动、意识水平改变、意识模糊、梦魇、妄想。
二、 研发情况
奥司他韦是由吉利德研发,罗氏负责全球商业化的一款神经氨酸酶抑制剂,对甲型、乙型流感、H5N1、H9N2等亚型流感病毒引起的流行性感冒有治疗和预防的作用。该药于1999年获得美国FDA批准上市,商品名为达菲。奥司他韦是目前国际上预防和治疗流感的主选用药,主要适应症包括用于成人和1岁及1岁以上儿童的甲型和乙型流感治疗、用于成人和13岁及13岁以上青少年的甲型和乙型流感预防。同时,奥司他韦是FDA批准的唯一一个可用于超过14天新生儿流感治疗药物。
2002年奥司他韦进入中国,2005、2006年罗氏分别将奥司他韦的生产销售授权给上海医药和东阳光药,两家公司分别以商品名奥尔菲和可威上市销售,实现了奥司他韦的国产化。
自2016年至2020年8月6日,本品在国内已有13家药企提交临床试验登记,有8家已提交申报资料,国内获批生产奥司他韦胶囊剂的有原研罗氏、东阳光、上海药业。(具体详见BE研究信息)。
三、 销售价格与市场概况
1 、销售价格
列出两种常见产品的销售价格,详见下表。
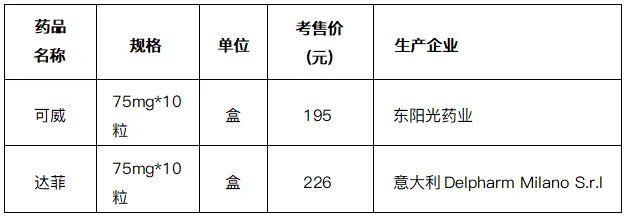
2 、市场概况

四、 备案信息
1) 中山万汉制药有限公司(进行中),空腹加餐后,118例;
2) 齐鲁制药(海南)有限公司(进行中), 空腹加餐后,96例;
3) 扬子江药业集团有限公司(进行中),空腹加餐后,90例;
4) 杭州澳赛诺生物科技有限公司(进行中),空腹加餐后,70例;
5) 广东中润药物研发有限公司(进行中),餐后,36例;
6) 广东中润药物研发有限公司(进行中),空腹,42例;
7) 中山万汉制药有限公司(进行中),空腹加餐后,24例;
8) 中山万汉制药有限公司(进行中),空腹加餐后,72-80例;
9) 中山万汉制药有限公司(进行中),空腹加餐后,24例;
10) 上海上药中西制药有限公司(已完成),空腹加餐后,80例;
11) 石药集团欧意药业有限公司(已完成),空腹加餐后,72例;
12) 四川科伦药业股份有限公司(已完成),空腹加餐后,96例;
13) 成都倍特药业有限公司(已完成),空腹加餐后,88例;
14) 安徽康瓴药业有限公司(已完成),餐后,48例;
15) 安徽康瓴药业有限公司(已完成),空腹,40例;
16) 信泰制药(苏州)有限公司(已完成),空腹加餐后,72例;
17) 博瑞生物医药(苏州)股份有限公司(已完成),空腹加餐后,72例;
18) 宜昌东阳光长江药业股份有限公司(已完成),空腹加餐后,96例。
五、 参考资料及文献
[1] Tamiflu®原研说明书.
文章来源:都正生物官网 www.duxact.com
点击文末“阅读原文”进入官网



长沙都正生物科技股份有限公司

长沙都正生物科技股份有限公司成立于2016年1月,坐落在长沙高新区,现有员工300余人。为全球生物医药企业提供药物、医疗器械和诊断试剂临床评价“一站式”服务。
分析实验室4800平方米,按照ISO 17025体系标准建设,仪器设备先进,包括光谱色谱分析检测、数据管理与生物信息分析、基因检测、免疫生化分析四大平台。
公司集“产、学、研”于一体,立志领跑药物临床评价、实验室信息化建设、医药大数据挖掘等新技术领域。
◆ 药物评价:为国内外200余家企业提供临床研究服务,以高水平的方案设计和高效率的临床管理,助力多家药企“全国首家”获批。
◆ 创新技术:全球首次发现并证实何首乌肝损伤特异性生物标志物,具有划时代意义;全国首家取得TMAO检测技术专利,并成功实现产业转化。
◆ 大数据挖掘:通过基因组学信息挖掘,成功为我国某企业创新药物上市提供支持。
◆ 信息化建设:围绕药学和临床,自主研发8款信息化系统,覆盖药物评价全过程,打破国际垄断,填补国内空白,建立行业标准。
目前,都正生物已成为“硬件先进、管理规范、分析能力强”的研发中心。都正人胸怀“立业报国、为国分忧”的理想,以“每天努力一点点”的精神,不断开拓进取,为我国生物医药产业做出贡献!
地址:长沙市高新区麓天路28号麓谷科技产业园C10栋
邮箱:bd@duxact.com
电话:0731-85681666-8006

创 新 ● 求 实

-- 每天努力一点点 --




 个人中心
个人中心
 我是园区
我是园区




