▎药明康德内容团队编辑
2021年6月1日,CTI BioPharma宣布,美国FDA已受理其为在研口服激酶抑制剂pacritinib递交的新药申请(NDA),用于治疗伴有严重血小板减少症的骨髓纤维化(myelofibrosis)患者。FDA还授予这一NDA优先审评资格,预计在今年11月30日前做出回复。

Pacritinib是一款特异性抑制JAK2、IRAK1和CSF1R的口服抑制剂。它的一个特点是并不抑制JAK1活性,因此避免了抑制JAK1带来的潜在副作用。
JAK家族蛋白是多种信号转导通路的中心组分,对正常的血细胞生长和发育、以及炎性细胞因子的表达和免疫应答都至关重要。这些激酶的突变已被证明与多种血液相关癌症的发生有直接关系,包括骨髓增殖性肿瘤(myeloproliferative neoplasms)、白血病(leukemia)和淋巴瘤(lymphoma)。除骨髓纤维化外,pacritinib在急性髓系白血病(AML)、骨髓增生异常综合征(MDS)、慢性粒单核细胞白血病(CMML)和慢性淋巴细胞白血病(CLL)等疾病中均具有潜在的治疗作用。
本次NDA申请是基于pacritinib的一个2期临床试验与两个3期临床试验的积极结果。研究结果表明,在接受pacritinib治疗的患者中,29%的患者脾脏体积缩小了至少35%,活性对照组仅缩小3%。此外,23%的患者总症状评分至少降低了50%,相比下,活性对照组仅降低了13%。安全性与耐药性方面,不良事件通常为低级别,可通过支持治疗进行控制,并且很少导致停药。患者的血小板计数和血红蛋白水平也保持稳定。
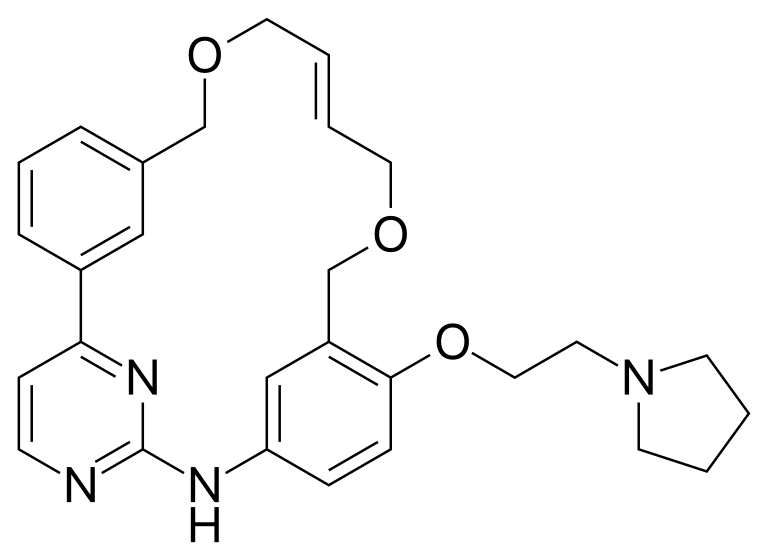
▲Pacritinib分子结构式(图片来源:Anypodetos, Public domain, via Wikimedia Commons)
骨髓纤维化是骨髓癌的一种类型,表现为形成纤维瘢痕组织,可导致严重的血小板减少和贫血、虚弱、疲乏、与脾脏和肝脏的肿大。据估计,重度血小板减少症患者占接受骨髓纤维化治疗患者的三分之一,总生存期仅为15个月。伴有重度血小板减少的骨髓纤维化患者的治疗选择有限,代表了一个未满足医疗需求的重要领域。
CTI Biopharma总裁兼首席执行官Adam R. Craig博士表示:“我们很高兴FDA接受我们的NDA,使我们离目标又近了一步,即为伴有严重血小板减少的骨髓纤维化患者提供一种新的治疗选择。我们期待在审评期间与FDA合作。”
参考资料:
[1] CTI BioPharma Announces Acceptance of NDA Granted with Priority Review of Pacritinib for Treatment of Patients with Myelofibrosis. Retrieved June 1, 2021, from https://investors.ctibiopharma.com/news-releases/news-release-details/cti-biopharma-announces-acceptance-nda-granted-priority-review
注:本文旨在介绍医药健康研究进展,不是治疗方案推荐。如需获得治疗方案指导,请前往正规医院就诊。
版权说明:本文来自药明康德内容团队,欢迎个人转发至朋友圈,谢绝媒体或机构未经授权以任何形式转载至其他平台。转载授权请在「药明康德」微信公众号回复“转载”,获取转载须知。







 个人中心
个人中心
 我是园区
我是园区




