▎药明康德内容团队编辑
2021年7月29日,Arrowhead Pharmaceuticals公司宣布,美国FDA已授予其潜在“first-in-class”在研RNAi疗法ARO-AAT(TAK-999)突破性疗法认定,用于治疗与α-1抗胰蛋白酶缺乏症(AATD)相关的罕见遗传性肝病。在2020年10月,该公司与武田(Takeda)达成一项可达10亿美元的
,共同开发这款药物。此前,ARO-AAT已获得了美国FDA授予的孤儿药资格和快速通道资格。

α-1抗胰蛋白酶蛋白缺陷(AATD)是一种罕见的遗传性疾病,与儿童和成人肝病以及成人肺部疾病相关。抗胰蛋白酶(AAT)蛋白主要由肝细胞合成和分泌,其功能是抑制能分解正常结缔组织的酶。最常见的致病变异体是Z突变体,由于一个氨基酸的变化导致蛋白的不正确折叠。突变蛋白不能有效分泌,在肝细胞内聚集成小球。从而引发持续的肝细胞损伤,导致纤维化、肝硬化,增加肝细胞癌的风险。对于这些患者来说,目前肝脏移植是唯一治疗方法,患者仍然存在显著未满足需求。
ARO-AAT旨在敲除导致进展性肝病的突变α-1抗胰蛋白酶(Z-AAT)蛋白的产生。减少炎症性Z-AAT蛋白的产生有望阻止肝病的进展,并可能允许肝脏再生和修复。
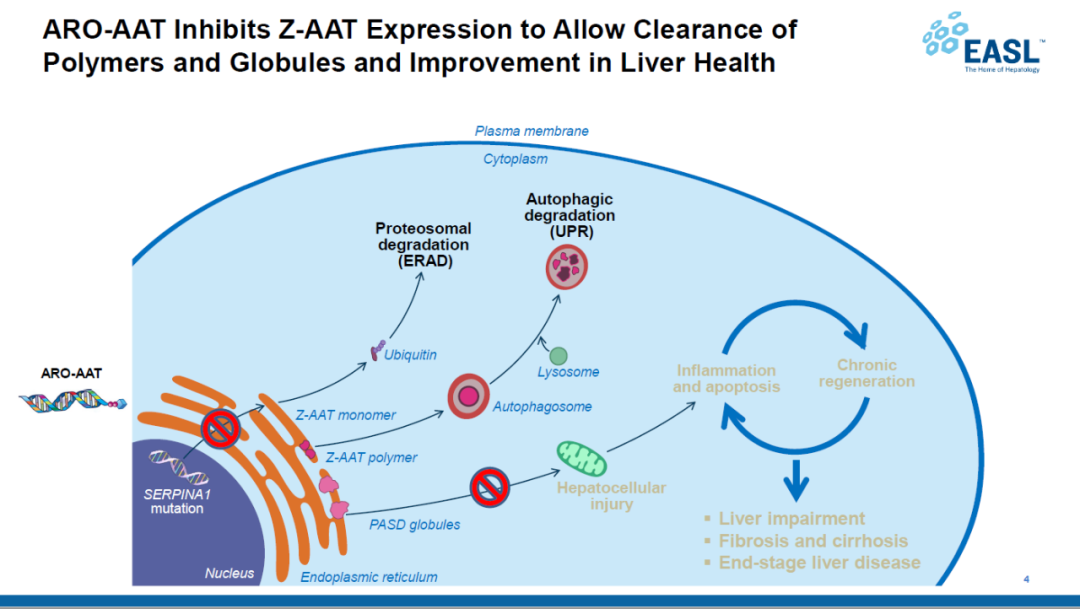
▲ARO-AAT的作用机制(图片来源:Arrowhead Pharmaceuticals公司官网)
“获得FDA授予的突破性疗法认定是ARO-AAT研究项目的一个重要里程碑,有望为AATD患者提供一种新的治疗选择。我们希望能通过与FDA继续合作,尽早为患者提供这款重要的在研药物。”Arrowhead的首席医学官Javier San Martin博士表示,“我也很高兴地宣布,ARO-AAT的2期临床试验SEQUOIA已完成40例患者的全部入组。此外,开放标签2期AROAAT2002试验获得的积极中期结果十分令人鼓舞。ARO-AAT能够持续减少导致进行性肝病的毒性突变Z-AAT蛋白的产生。而且持续6-12个月的Z-AAT蛋白水平降低导致多个与肝脏纤维化和肝脏健康有关的生物标志物的改善。”
参考资料:
[1] Arrowhead Pharmaceuticals Receives Breakthrough Therapy Designation from U.S. FDA for ARO-AAT for the Treatment of Alpha-1 Antitrypsin Deficiency Associated Liver Disease. Retrieved July 29, 2021, from https://www.businesswire.com/news/home/20210729005199/en
[2] ARO-AAT, an Investigational RNAi Therapeutic, Demonstrates Improvement in Liver Fibrosis with Reduction in Intrahepatic Z-AAT Burden. Retrieved July 29, 2021, from https://ir.arrowheadpharma.com/static-files/f3260420-51ad-4bc1-85d8-b45fd143d6fd
注:本文旨在介绍医药健康研究进展,不是治疗方案推荐。如需获得治疗方案指导,请前往正规医院就诊。
版权说明:本文来自药明康德内容团队,欢迎个人转发至朋友圈,谢绝媒体或机构未经授权以任何形式转载至其他平台。转载授权请在「药明康德」微信公众号回复“转载”,获取转载须知。







 个人中心
个人中心
 我是园区
我是园区




