
核孔复合物(nuclear pore comple, NPC)镶嵌在真核细胞的核膜中,是非分裂期细胞控制细胞核与细胞质之间物质交换的唯一通道,与细胞转录表达等一系列重要生命活动都与核孔运输息息相关【1,2】。核孔是由超过30种核孔蛋白(nucleoporins)组成的超大型的复合物,负责运输功能的中央通道部分更是由上百个富含“苯丙氨酸-甘氨酸”重复序列(FG-repeats)的天然无序蛋白(FG核孔蛋白)组成的选择性屏障【2,3】。或许正是由于核孔功能与结构的复杂性和特殊重要性,使得核孔本身在不同的细胞中具有结构高度动态化,组分成分异质化,和功能的冗余性等特点【4】。常规的实验技术手段,包括冷冻电镜,晶体学,常规的生化分析和物化表征,细胞内基因敲除或突变等,都无法清楚的解析核孔中央通道形成选择性屏障的分子机制。目前,核孔中央通道的组织结构仍是未知,如何实现选择性运输与调控仍然有很大的争论。
近日,美国耶鲁大学医学院林晨翔研究组与Patrick Lusk研究组以及沈琦研究员(第一作者)合作在JACS杂志发文,题为DNA-Origami NanoTrap for Studying the Selective Barriers Formed by Phenylalanine-Glycine-Rich Nucleoporins,采用DNA折纸技术,冲破核孔运输研究的技术壁垒,揭示了FG核孔蛋白组装形成选择性屏障的机制。

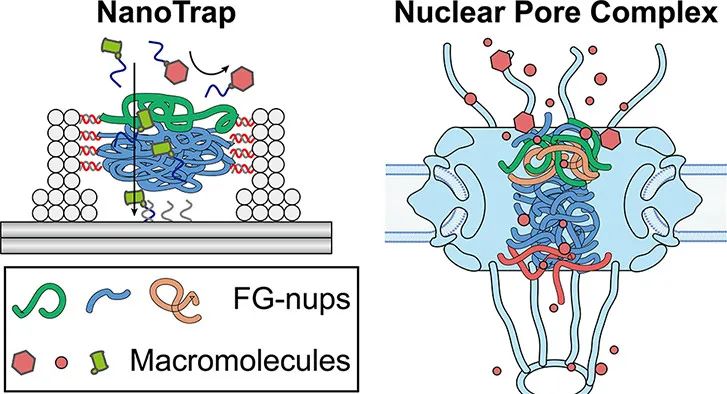
在体外研究核孔选择性屏障形成机理的关键与挑战在于创造一个类似于天然核孔的拥挤微环境,将几十拷贝的天然无序蛋白有序的组织在一个约40纳米直径的狭窄空间。DNA折纸技术在纳米尺度上三维空间的可设计性和精确的控制能力,并且与其他生物材料(如蛋白质和脂类)的兼容性在攻克这个技术难题上发挥了无可替代的作用。为了研究富含苯丙氨酸-甘氨酸重复序列的核孔蛋白如何形成选择性屏障和影响核孔运输的因素,本文作者们使用DNA为骨架材料,构建了一个直径为45纳米,高22.5纳米的“纳米陷阱”。这个“陷阱”能精确的控制0到48个拷贝的FG核孔蛋白组装在通道上部,形成一个由FG核孔蛋白交织而成的蛋白网格屏障。当有蛋白大分子通过这个蛋白屏障就会被位于陷阱底部的捕获装置捕获并通过荧光信号检测到。利用这个仿生的纳米陷阱,作者精确的调整并测试了通道内不同数量,不同种类和不同位置的FG核孔蛋白对大分子通过性的影响,确定了核孔蛋白FG重复序列的类型、嫁接密度和空间排列是形成有效扩散屏障的关键因素。
此外,作者们还观察到,在混合了多种FG核孔蛋白情景中, 拥有更强内聚力的核孔蛋白在形成有效扩散屏障时仍占主导地位。最后,该课题组研究人员证明了核转运受体Ntf2可以选择性地通过由富含FxFG重复序列核孔蛋白组成的蛋白网格屏障,而由富含GLFG重复序列组成的蛋白屏障则不能,显示人工组装的核孔蛋白屏障实现了天然核孔对蛋白大分子的转运受体依赖的选择透过性。
总的来说,该工作采用了DNA折纸技术,构建核孔研究仿生平台,重现了类似天然核孔对小分子自由扩散,大分子选择性运输的核心生物学功能。该研究还揭示了核孔蛋白FG重复序列的类型、嫁接密度和空间排列是形成有效扩散屏障的关键因素。面对目前核孔研究的困难和争论,该仿生平台将为清晰描绘核孔运输的机制提供了有价值的工具。
原文:
https://doi.org/10.1021/jacs.1c05550
参考文献
1. Strambio-De-Castillia, C.; Niepel, M.; Rout, M. P., The nuclear pore complex: bridging nuclear transport and gene regulation. Nat Rev Mol Cell Bio 2010, 11, (7), 490-501.
2. Beck, M.; Hurt, E., The nuclear pore complex: understanding its function through structural insight. Nat Rev Mol Cell Bio 2017, 18, (2), 73-89.
3. Lin, D. H.; Hoelz, A., The Structure of the Nuclear Pore Complex (An Update). Annu Rev Biochem 2019, 88, 725-783.
4. Hurt, E.; Beck, M., Towards understanding nuclear pore complex architecture and dynamics in the age of integrative structural analysis. Curr Opin Cell Biol 2015, 34, 31-38.
转载须知
【非原创文章】本文著作权归文章作者所有,欢迎个人转发分享,未经允许禁止转载,作者拥有所有法定权利,违者必究。




 个人中心
个人中心
 我是园区
我是园区




