▎药明康德内容团队报道
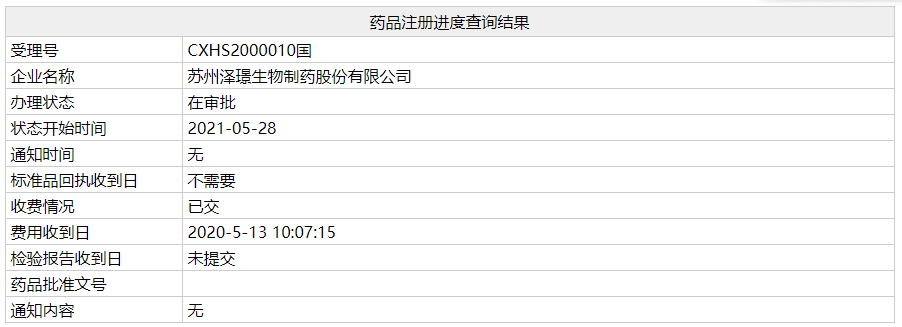
根据中国国家药监局(NMPA)药品注册进度最新查询结果,由泽璟制药提交的一项甲苯磺酸多纳非尼片的新药上市申请的审评状态已更新为:在审批,这意味着这款新药有望于近期在中国获批上市。根据NMPA药品审评中心(CDE)优先审评公示,该上市申请的适应症为:治疗晚期(无法手术或转移性)肝细胞癌。该药本次进入“在审批”意味着,泽璟制药将有望迎来首款获批上市的药品。
甲苯磺酸多纳非尼是一款口服、多靶点小分子抗肿瘤药物。临床前研究证实,该药物既可抑制VEGFR、PDGFR等多种受体酪氨酸激酶的活性,也可直接抑制各种Raf激酶,并抑制下游的Raf/MEK/ERK信号传导通路,抑制肿瘤细胞增殖和肿瘤血管的形成,从而发挥多重抑制、多靶点阻断的抗肿瘤作用。
2020年5月,泽璟制药提交了甲苯磺酸多纳非尼的新药上市申请,并于同年10月被纳入优先审评。据悉,该上市申请主要是基于一项名为ZGDH3的临床研究结果。
ZGDH3是一项开放、随机、平行对照、多中心的2/3期临床研究,由中国临床肿瘤学会(CSCO)副理事长秦叔逵教授主导,旨在探索多纳非尼片在晚期肝细胞癌患者一线治疗中的有效性与安全性。研究主要终点为总生存期(OS),次要终点包括无进展生存时间(PFS)、客观缓解率(ORR)、疾病控制率(DCR)、安全性及耐受性等指标。
试验结果显示,ZGDH3研究达到了预设的主要终点和统计学要求。在未接受过系统治疗的不可手术或转移性晚期肝细胞癌患者中,多纳非尼治疗组的中位总生存期(mOS)显著优于对照药物索拉非尼治疗组,达到统计学上差异显著性且具有临床意义的延长。此外,多纳非尼组在3级及以上不良事件发生率、与药物相关的导致停药或减量的不良事件发生率等方面显示出更优的安全性。
除了肝癌之外,目前泽璟制药还在开展多纳非尼治疗晚期结直肠癌和甲状腺癌的关键性临床研究,同时也在积极推进多纳非尼联合PD-1/PD-L1单抗治疗多种肿瘤的新型研究。
注:本文旨在介绍医药健康研究进展,不是治疗方案推荐。如需获得治疗方案指导,请前往正规医院就诊。
[1]泽璟制药杰克替尼片治疗中、高危骨髓纤维化的II期临床研究结果入选EHA 2021. Retrieved Apr 25,2021, from http://www.zelgen.com/xinwenzhongxin/2021/04-25/214.html
[2]中国国家药监局(NMPA)官网. From https://www.nmpa.gov.cn/zwfw/zwfwzhcx/index.html
声明:本文由药明康德内容团队根据公开资料整理编辑,欢迎个人转发至朋友圈,谢绝媒体或机构未经授权以任何形式转发/复制至其他平台。转发授权请在「医药观澜」微信公众号留言联系我们。







 个人中心
个人中心
 我是园区
我是园区




