Cancer Cell | 方兰/王平团队揭示甲硫氨酸限制促进cGAS染色体解离和激活增强抗肿瘤免疫的重要机制
收藏
关键词:
免疫揭示Cell瘤肿瘤
资讯来源:BioArt + 订阅账号
发布时间:
2023-06-02
虽然免疫检查点单抗治疗在临床抗肿瘤应用中取得了可喜成果,但在不同肿瘤中的响应率仍存在较大差异。肿瘤免疫微环境的复杂性和多样性对免疫治疗具有深远影响。因此,深入解析肿瘤免疫微环境的调节机制对于评估患者对免疫疗法的反应能力,并揭示新的治疗靶点具有重要临床价值。cGAS感应胞质双链DNA,产生第二信使cGAMP,激活STING-TBK1-干扰素信号通路,在先天免疫反应和肿瘤免疫中发挥关键作用。通过各种途径激活cGAS-STING通路,已被视为与免疫检查点抑制剂联合治疗的有效策略。cGAS最初被认为定位于细胞质,后续研究发现大量内源性cGAS在细胞核中富集,其活性抑制受到染色质栓系和细胞周期依赖性磷酸化的调控。生化和结构研究表明,核小体束缚cGAS在组蛋白的酸性斑块上,阻断其与染色质DNA结合导致活性抑制。然而,染色质栓系的cGAS如何从染色质解离并重新激活的分子机理并不清楚。解决这些基本问题可以为重塑肿瘤免疫微环境提供新的治疗靶点和新策略。
2023年6月1日,同济大学医学院/癌症中心和同济大学附属第十人民医院方兰/王平团队在Cancer Cell杂志在线发表了题为
Methionine Restriction Promotes cGAS Activation and Chromatin Untethering through Demethylation to Enhance Antitumor Immunity
的研究论文。该研究
揭示了甲硫氨酸饮食限制促进cGAS激活,并增强放疗(IR)和免疫检查点抑制剂(ICIs)的抗肿瘤免疫表型。
其原因是肿瘤细胞竞争摄取甲硫氨酸促进甲基转移酶SUV39H1催化cGAS发生甲基化修饰,甲基化促进cGAS染色质栓系和活性抑制。对肿瘤细胞进行短时甲硫氨酸剥夺或靶向干预SUV39H1,降低cGAS甲基化修饰促进其染色质解离进入细胞质,增强抗肿瘤免疫。该工作深入解析了
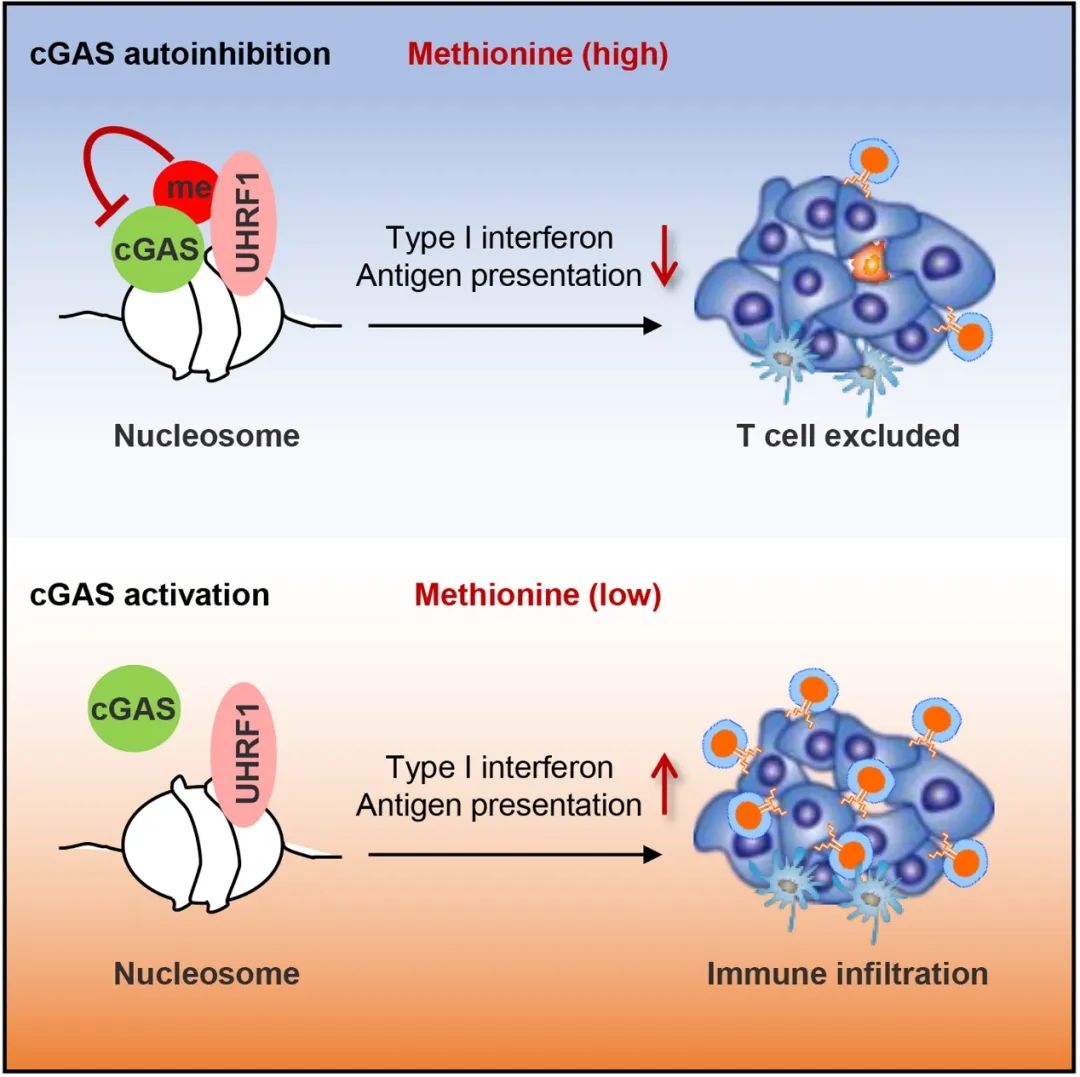
甲硫氨酸介导甲基化修饰招募UHRF1调节cGAS染色质栓系,发现去甲基化促进cGAS从染色体解离的重要机制,为激活cGAS-STING通路重塑肿瘤免疫微环境提供了新的干预策略
(图1)
。
营养饮食调节,特别是氨基酸限制,已成为肿瘤微环境重编程的新方法,并有望用于癌症治疗。肿瘤细胞的高代谢需求,促进其与免疫细胞竞争氨基酸资源。肿瘤微环境中的肿瘤内在机制和代谢调节也可能有助于免疫逃逸或降低免疫反应。但尚不清楚氨基酸代谢是否对肿瘤cGAS-STING信号通路有影响,以及它是否可以与电离辐射和免疫检查点抑制剂结合用于癌症治疗。团队首先通过氨基酸剥夺的筛选实验,发现甲硫氨酸剥夺特异性促进cGAS-STING-干扰素信号通路,并且这个过程依赖cGAS。敲除内源cGAS,甲硫氨酸限制对干扰素信号通路和抗肿瘤免疫的增强作用消失。紧接着,研究人员通过对甲硫氨酸代谢通路
(Met-SAM-SAH代谢流)
和甲基化修饰质谱分析发现,cGAS发生多个位点甲基化修饰,其中K362位点
(对应鼠源K350位点)
甲基化修饰依赖甲硫氨酸
(Met)
和S-腺苷甲硫氨酸
(SAM)
。
接下来,通过一系列的生化细胞实验发现甲基化缺失减弱cGAS与双链DNA结合,抑制其二聚化和相变过程,降低cGAS活性。而甲基化修饰促进cGAS的细胞核聚集和染色质栓系,并且这一过程依赖甲基化识别蛋白UHRF1。染色质结合蛋白UHRF1招募甲基化修饰状态的cGAS,促进其与染色体结合。甲硫氨酸短时限制或者靶向干预SUV39H1-UHRF1轴降低cGAS甲基化修饰,促进其染色体解离和进入细胞质,再次被胞质双链DNA激活。这些数据共同表明肿瘤微环境或者肿瘤细胞内甲硫氨酸水平通过甲基化和去甲基化的动态平衡精细调控cGAS染色质栓系和活性状态。
团队接下来通过大量的转基因小鼠和动物模型实验证明了肿瘤细胞和宿主甲基化缺失亦或是甲基化模拟修饰均抑制内源cGAS活性,促进肿瘤免疫逃逸。而甲基转移酶Suv39h1敲除小鼠的抗肿瘤免疫增强。并且甲硫氨酸限制饮食和SUV39H1的抑制剂联合治疗重塑肿瘤免疫微环境,抑制肿瘤生长。通过临床样本的分析也进一步cGAS甲基化水平与结直肠癌肿瘤病人预后呈明显负相关。而且通过深入分析临床样本突变类型,发现cGAS甲基化与KRAS/NRAS G12/13突变密切相关,而与BRAF V600E突变及P53表达无明显相关性。并且在微卫星不稳定的一类免疫治疗敏感的肿瘤病人组织中,cGAS甲基化修饰水平偏低。这些发现为临床肿瘤治疗手段的选择提供了重要的理论依据。
图1 甲硫氨酸介导甲基化修饰招募UHRF1调节cGAS染色质栓系,干预cGAS甲基化修饰促进其染色质解离在肿瘤免疫微环境重塑中的作用机制及功能
综上所述,该研究揭示了甲硫氨酸-SUV39H1-UHRF1通过甲基化修饰调节cGAS染色质栓系和活性,并阐明了cGAS染色质解离的生化基础,为激活cGAS-STING通路促进抗肿瘤免疫提供了重要的潜在靶向干预策略。
鉴于cGAS在抗病毒感染、自身免疫性疾病和肿瘤免疫中的关键作用,该研究提示甲基化修饰抑制cGAS活性可能作为免疫应答调节的关键开关,值得深入探索。
据悉,同济大学医学院/癌症中心王平教授和同济大学附属第十人民医院方兰教授为本论文的共同通讯作者。同济大学医学院博士研究生郝运,博士研究生余海红和硕士研究生谷雪妹为该论文共同第一作者。该研究同时得到了同济大学附属第十人民医院秦环龙教授等团队的合作和支持。
方兰教授近年来主要关注肿瘤免疫微环境重塑,聚焦甲基化和泛素化等蛋白质翻译后修饰,解析表观和代谢调控调节肿瘤免疫微环境的作用机制及功能,以共同通讯/第一作者发表Cancer Cell (2023,2018),Molecular Cell,Cell Death and Differentiation, Cell Discovery等代表性论著。课题组招聘博士后和技术员(支持攻读博士学位),欢迎志同道合者加盟!
王平教授长期致力于肿瘤微环境基础与转化研究,围绕肿瘤代谢和免疫微环境的调控机制寻找新靶点,开发肿瘤干预新策略,以通讯作者在Cancer Cell(2023,2018),Immunity,Molecular Cell,Cell Research,Developmental Cell,J Clin Invest等国际主流杂志发表论著50余篇。课题组长期招聘博士后、副/助理研究员等各类工作人员,欢迎有志者加盟!
https://jinshuju.net/f/ZqXwZt
或扫描二维码
投递简历
https://doi.org/10.1016/j.ccell.2023.05.005

【非原创文章】本文著作权归文章作者所有,欢迎个人转发分享,未经作者的允许禁止转载,作者拥有所有法定权利,违者必究。









 药选址
药选址








