
2月3日,强生宣布与Mersana Therapeutics达成合作协议,共同开发3款新一代ADC药物。因此,笔者重新仔细审视了Mersana的整个技术平台,留意到其中的Dolasynthen。

该技术就是利用高分子linker实现毒素分子偶联数目的更丰富的变化,从而满足不同的靶点和适应症的技术需求。DAR最高可达24。
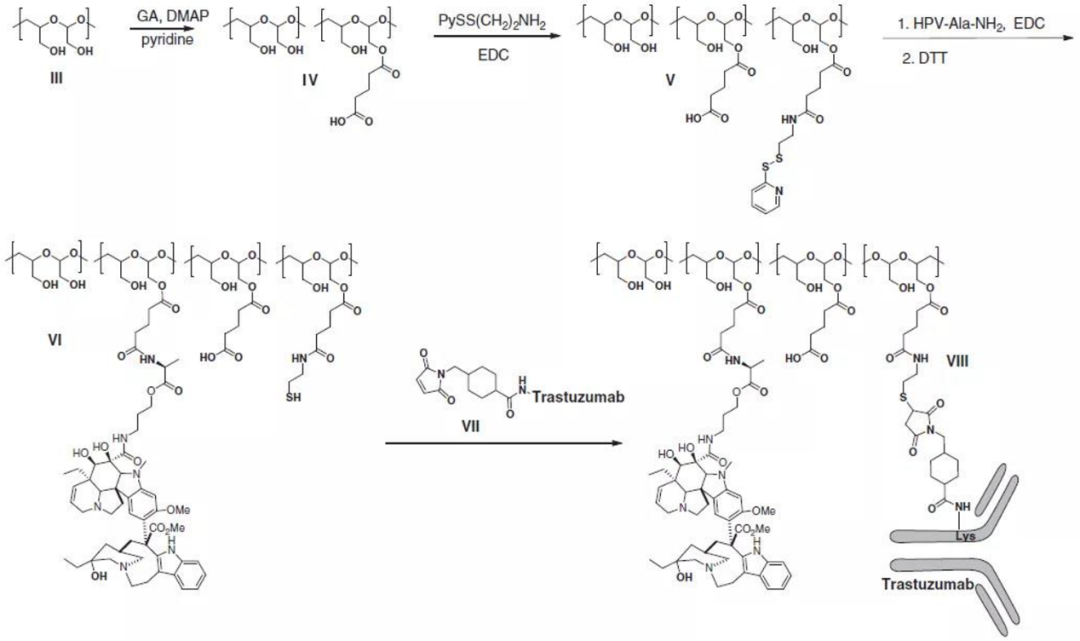
不过,联想到ADC的最大局限性之一——毒素分子的体内毒性,笔者觉得,DAR的提高搭配毒素分子的毒性的适当降低,倒不失为一个可以探索的改进方向。
ADC药物的毒性主要来源于2个方面,即抗体分子产生的毒性和毒素分子产生的毒性,其中抗体分子产生的毒性随着靶点、适应症等因素的不同有较大差异,而毒素分子产生的毒性主要体现在对快速增殖的健康细胞的损伤,如淋巴细胞的减少、脱发、胃肠道反应等。笔者统计了FDA批准的ADC药物的主要副反应(以说明书为准),总结如下:
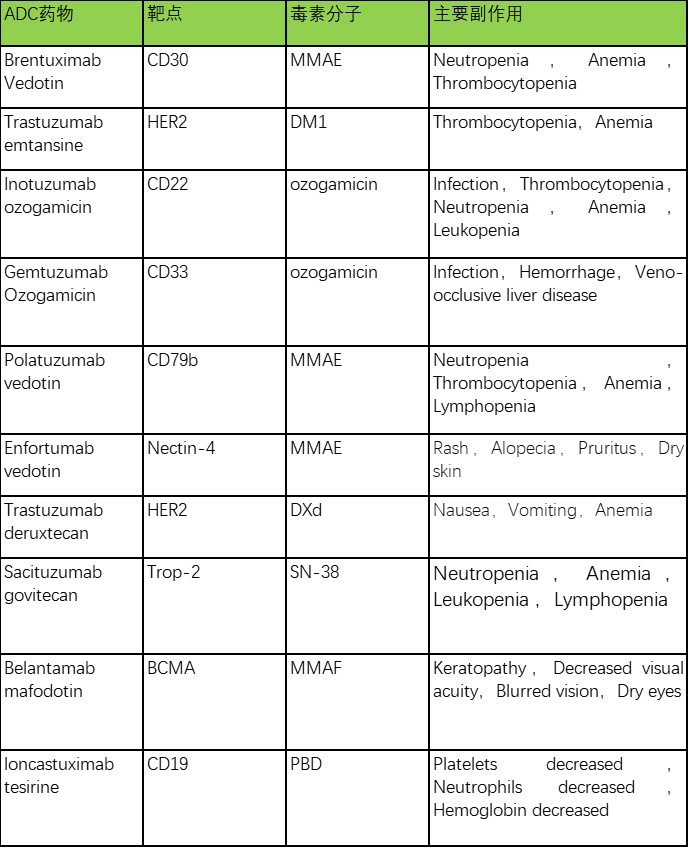
另外,在临床阶段,很多ADC药物也是由于血液毒性等化疗类似毒性而终止开发的,如SGN-CD33A等。
Bicycle Therapeutics的“low blood-to-tumor ratio”的实际效果
英国的Bicycle Therapeutics公司以环肽分子的筛选和开发为其核心技术平台,在此基础上,他们探索了多种应用场景,包括多肽-药物偶联物(即PDC),目前已有部分项目进入临床试验阶段。
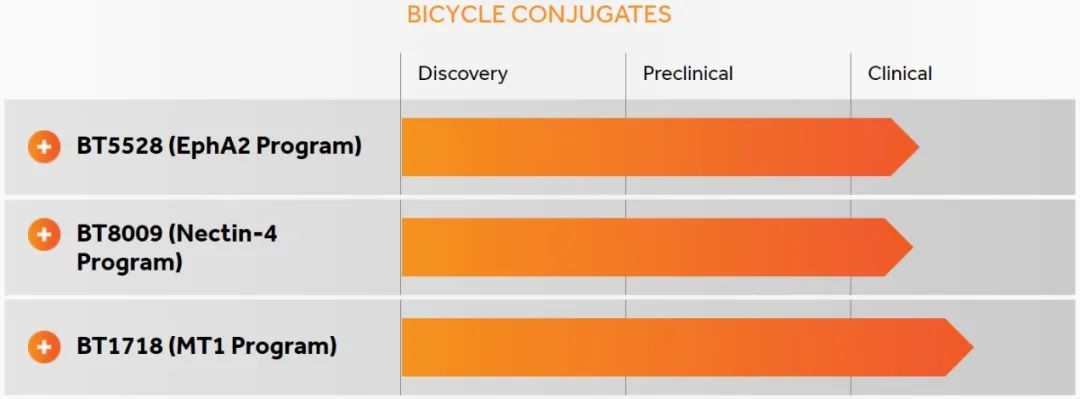
关于PDC方向的应用,Bicycle强调其优势在于低“blood-to-tumor ratio”:由于PDC药物分子量小,组织穿透性好,因此可以帮助毒素分子迅速富集到肿瘤部位,快速行使杀伤癌细胞的功能;同时,血液中的药物分子被迅速清除,半衰期很短,有利于系统性的毒副作用。这一理论得到了BT8009体内PK试验的验证。基于这一特点,PDC给药的剂量调整可以有一个很大的空间。

另外,正因为PDC摩尔剂量可以有一个很大的调节范围,DAR较低(等于1)的理论缺陷也可以得到弥补。以BT8009和同靶点的ADC药物Enfortumab vedotin的比较为例:BT8009的剂量假设为爬坡剂量之一的13 mg/m2(成人皮肤的表面积设为2 m2),Enfortumab vedotin目前的标准剂量为1.25 mg/kg(假设成人体重为80 kg);BT8009的分子量约4 kDa,Enfortumab vedotin的分子量约160 kDa。则:

可以看出,BT8009的摩尔剂量是Enfortumab vedotin的10倍,毒素的载量相对足够。
然而,之前公布的初步的临床试验数据并不理想。
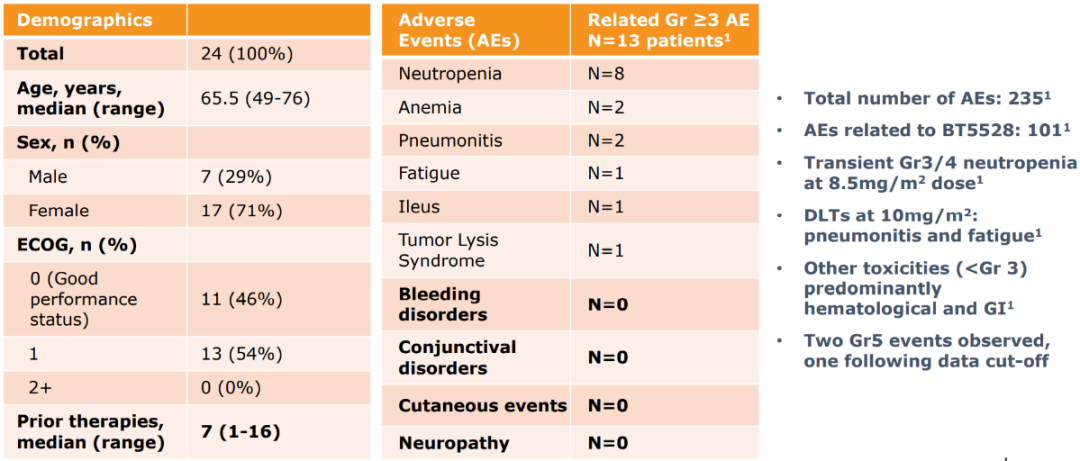
同样,BT8009的早期数据显示,虽然未发现1-2级眼毒性和DLT(略好于对标的ADC药物Enfortumab),但出现3级以上血液毒性的患者的比例并不低(>10%)。

因此,公司强调的PDC理念并未得到很好的体现。由于公司的PDC采用的毒素分子都是ADC常用的毒素(MMAE或DM1),毒素分子本身的优化似乎更为重要。

早期的ADC使用的毒素分子都是传统的化疗药物,如阿霉素、丝裂霉素等,因为ADC这一概念的初衷就是“靶向化疗”。但由于抗体分子量较大,合适的ADC剂量窗口内,化疗药物无法达到有效浓度。因此,后期人们才尝试开发毒性更强的小分子作为ADC的payload。但这样一来,新的毒性问题也随之而来,因为毒素分子难免会有非特异性的释放,这其中的原因很多,包括linker的提前断裂、ADC分子被细胞非特异性地内吞(通过pinocytosis等方式)等等。
因此,毒素的毒性是ADC药物开发的核心问题之一。笔者认为,适当减弱毒素的毒性,同时提高DAR值,是优化的趋势之一。Immunomedics的Sacituzumab govitecan使用的毒素分子是SN-38,即伊立替康的活性代谢物,而DAR为7~8,事实上有这种改良趋势,但效果还是不够理想。这一领域的研发人员仍需努力,类似Dolasynthen的技术或许能够实现这一目标。




 个人中心
个人中心
 我是园区
我是园区




