
饮食习惯是影响人体健康和肠道疾病的重要因素。高脂饮食大大提高了炎症性肠病和结直肠癌等肠道疾病的患病风险;相反,适当禁食可以减缓癌症的发展,被认为是预防癌症的有效策略。肠道干细胞是一类具有自我更新和多能性的细胞群,在肠道稳态维持、肠上皮损伤修复和肠道疾病发生等生物学过程中均发挥着关键作用。肠道干细胞的命运及功能主要受到来自间充质微环境信号的调控。然而,肠道间充质微环境能否响应饮食状态变化参与调控肠道稳态和疾病发生尚未揭示清楚。因此,深度解析饮食状态-肠道间充质微环境-肠道干细胞轴的调控机制不仅是阐明肠道稳态调控规律的关键所在,同时也有助于揭示不良饮食习惯诱发炎症性肠病等肠道疾病的致病机理。
2022年3月16日,中国农业大学营养与健康系吕聪课题组与生物学院于政权课题组在Cell Research期刊在线发表了题为 Lepr+ mesenchymal cells sense diet to modulate intestinal stem/progenitor cells via Leptin–Igf1 axis 的研究论文,发现了一种特殊的能够响应饮食状态变化的肠道干细胞间充质微环境,其在肠道稳态维持和损伤修复过程中具有重要作用。

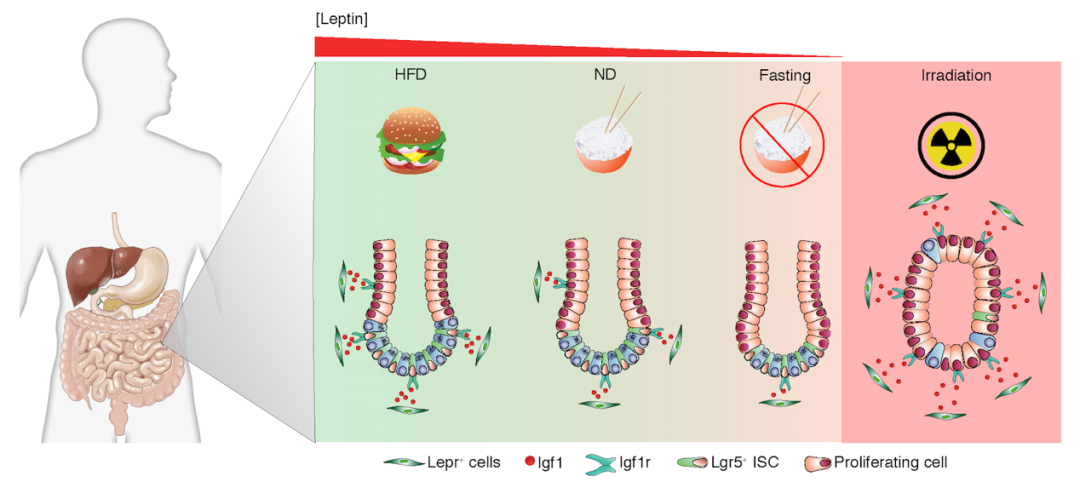
该研究首先利用单细胞测序分析发现了一群特殊的瘦素受体阳性(Lepr+)间充质细胞,鉴定为新型的肠道干细胞微环境。在生理情况下,Lepr+间充质微环境维持着肠道干细胞的快速增殖能力;在肠道辐射损伤后,Lepr+间充质细胞显著增加,起到促进肠上皮再生的作用。进一步,该研究发现Lepr+间充质细胞受到瘦素(Leptin)介导的STAT3信号通路调控,特异地高表达并分泌胰岛素样生长因子-1(Igf1),进而Igf1通过与其肠道干细胞的受体(Igf1r)相互作用来维持干细胞的快速增殖。有趣的是,Lepr+间充质细胞能够响应饮食状态的变化,在高脂饮食情况下,其数量显著增加;相反在禁食时,其数量急剧减少。这意味着饮食状态(高脂或者禁食)可以通过Lepr+间充质微环境来调控肠道干细胞的功能,从而影响肠道稳态。这一发现表明Lepr+间充质细胞是连接系统性饮食与局部肠道上皮功能的重要介质。
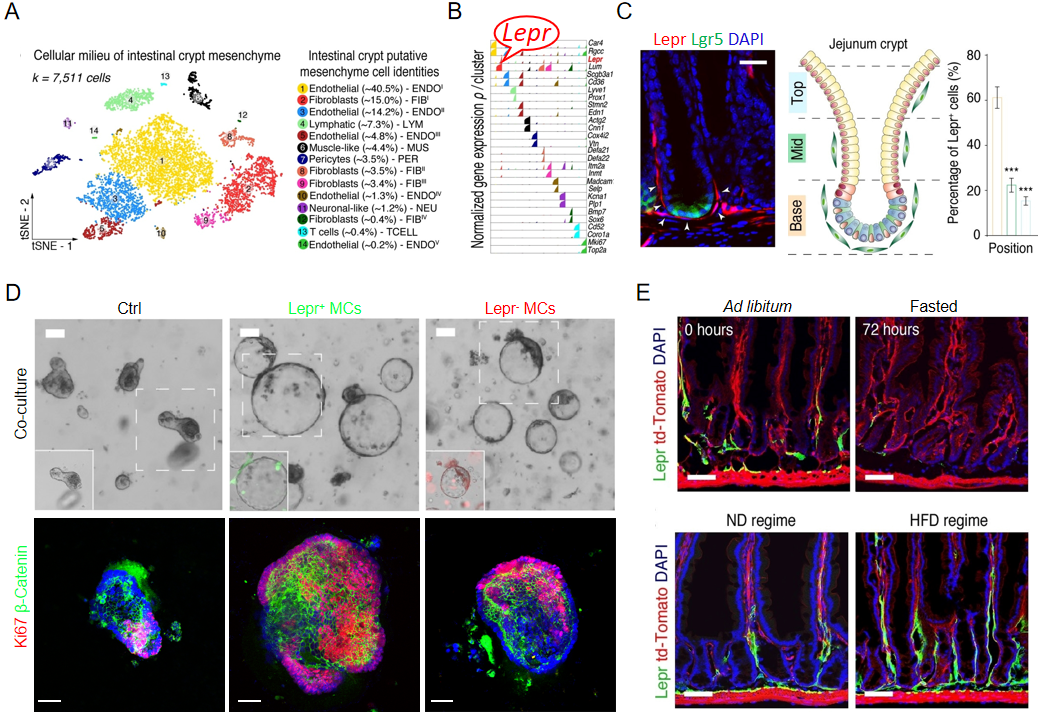
这项研究鉴定了一类新型的响应饮食状态的肠道干细胞间充质微环境。就生理意义而言,这一发现揭示了机体在营养充裕时加快营养吸收的机制:即在营养充裕时,肠道通过增加Lepr+间充质细胞数量来促进干细胞的增殖,以增加肠上皮吸收面积,促进了机体的营养吸收和能量储存。就病理而言,Lepr+间充质细胞有可能是介导高脂饮食诱发炎症性肠病和肠癌的重要因素。在未来的研究中,Lepr+间充质细胞是否在这些肠道相关疾病中发挥着重要作用以及其调控机制值得深入探究。
原文链接:
https://www.nature.com/articles/s41422-022-00643-9.
转载须知
【非原创文章】本文著作权归文章作者所有,欢迎个人转发分享,未经允许禁止转载,作者拥有所有法定权利,违者必究。




 个人中心
个人中心
 我是园区
我是园区




