
2022年4月,国际权威消化病学术杂志《胃肠病学》(Gastroenterology,IF:22.682)发表了来自天津医科大学肿瘤医院胰腺肿瘤中心的郝继辉课题组题为“BZW1通过增强eIF2α磷酸化促进胰腺导管腺癌的糖酵解和肿瘤生长(BZW1 Facilitates Glycolysis and Promotes Tumor Growth in Pancreatic Ductal Adenocarcinoma Through Potentiating eIF2α Phosphorylation)”的研究论文。
研究人员通过临床及实验数据,发现BZW1分子对维持胰腺癌实体肿瘤细胞在低糖乏氧微环境(Glucose-Oxygen deprivation microenvironment)中存活、生长起到关键作用。BZW1分子通过促进eIF2α与其激酶PERK的结合,促进eIF2α的磷酸化从而促进糖酵解关键蛋白HIF1α及c-MYC的翻译,进而显著地促进了胰腺癌细胞的糖酵解能力。该研究揭示了胰腺癌代谢重编程的关键调控基因,阐明了胰腺癌应答低糖乏氧环境的新机制,提出了胰腺癌的治疗新靶点。

本项工作主要完成单位为天津医科大学肿瘤医院,博士生李增勋、葛懿为共同第一作者,郝继辉教授和黄崇标教授为共同通讯作者。美国俄克拉荷马大学(The University of Oklahoma)医学部胃肠道癌症研究中心主任Li Min教授发表同期评述文章,高度评价了该发现,认为此研究加深了对胰腺癌生物学行为的理解,为开发胰腺癌靶向治疗提供了新的方向。


低糖乏氧微环境是胰腺癌的特征性微环境,影响着肿瘤细胞发生转移、耐药等多种恶性行为。乏氧诱导因子1(HIF1)、MYC等信号通路是肿瘤应答低糖乏氧微环境中的重要调控信号,实体肿瘤细胞通过复杂的调控网络来调控这些信号通路,从而应答低糖乏氧微环境,阐明这些调控网络有助于阐明胰腺癌生长的分子机制从而开发治疗靶点。
近20年来,郝继辉教授团队针对胰腺癌乏氧微环境开展了一系列深入探索,揭示了其中的部分关键调控机理,发现乏氧环境上调乏氧诱导因子HIF-1,从而激活胰腺癌细胞中Fascin、LASP1、IGFBP2及LIMS1等关键分子的转录水平表达,进而影响胰腺癌细胞凋亡、侵袭转移、无氧糖酵解及肿瘤血管新生等生物学行为,最终促进胰腺癌进展。

在此研究中,郝继辉团队通过一系列的生物信息学的筛选,发现了一个新的促进胰腺癌生长的关键基因——BZW1。研究者发现BZW1在胰腺癌肿瘤组织及细胞内呈高表达,其表达水平与肿瘤的大小及TNM分期呈显著正相关,是胰腺癌的独立预后因子。在低糖乏氧微环境下,BZW1的表达水平对维持肿瘤的存活、生长起到了决定性的作用(图1A-1B)。BZW1通过促进HIF1α和c-MYC的翻译促进了肿瘤细胞的糖酵解;后续发现BZW1蛋白可以促进eIF2α和其激酶PERK的结合,从而促进eIF2α的磷酸化,而磷酸化的eIF2α对于HIF1α和c-MYC的内部核糖体进入位点(IRES)依赖的特殊翻译起到关键作用。
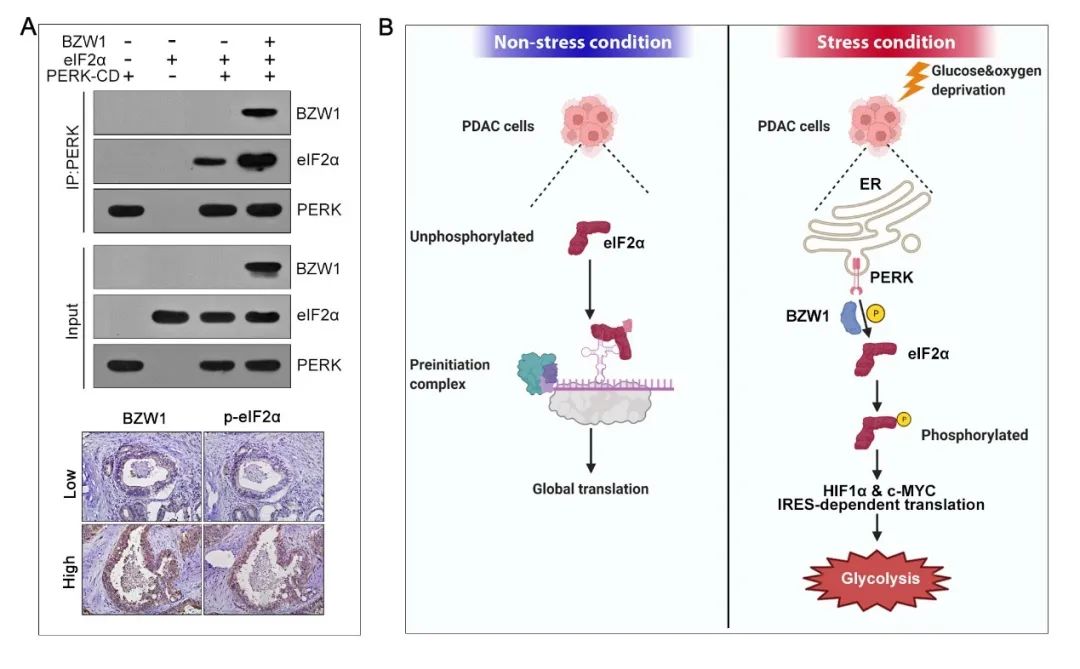
图1 BZW1促进肿瘤细胞适应低糖乏氧微环境
研究者通过临床资料分析及动物实验研究,探索性研究了BZW1分子相关的临床转化应用前景。小鼠移植瘤模型及类器官模型研究发现,BZW1分子能显著地促进了肿瘤细胞的生长及抗凋亡。回顾性分析胰腺癌患者临床病理切片发现BZW1表达强度与患者癌细胞增殖水平呈显著地正相关性。这些结果提示BZW1表达强度可作为胰腺癌患者预后判断指标。
另外,研究者应用eIF2α磷酸化抑制剂后,小鼠肿瘤生长显著受到抑制,肿瘤组织细胞凋亡率显著升高,而BZW1高表达的肿瘤则更为明显。这些结果揭示BZW1是一个非常有潜力的抗胰腺癌治疗靶点。
总的来说,本项研究工作揭示了胰腺癌应答低糖乏氧微环境的新机制,阐明了BZW1蛋白在胰腺癌生长中发挥的关键作用;为实体肿瘤治疗提供了新的靶点。

通讯员 天津医科大学肿瘤医院 朱芸
中国医学论坛报 刘佳玲整理
中国医学论坛报将每周定期推送肿瘤领域最新进展,传递专家观点,分享学术共识,一起来看吧!









 个人中心
个人中心
 我是园区
我是园区




