基于“QBD”的理念,ANDA的分析方法并非单纯的仿标准,而是基于API的性质和制剂处方、工艺进行方法的合理开发,验证与转移。虽然不像IND中的方法需要从无到有,但是有标准可参考的前提下,ANDA的分析方法中仍然存在一些痛点,在方法开发、方法验证和方法转移、稳定性检验的全生命周期中均会出现,基于这些“痛点”在方法建立之初进行充分设计显得尤为重要。本文以注射液A的有关物质和含量分析的HPLC方法为例,将其分析方法全生命周期中的痛点案例逐一暴露,与广大同行分享与探讨。
基于ANDA的分析相关调研,结合参比制剂的进口信息等,会对相关的进口注册标准,各国药典标准进行收集。本例中存在进口注册标准,因此在有关物质方法开发之初,选择重现标准中方法,得到图1的色谱分离情况。
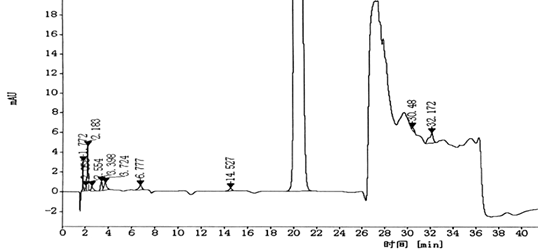
可以得到本例的方法开发痛点:①基线波动较大;②部分杂质在溶剂峰处;③杂质未达到基线分离;④梯度峰后的色谱峰需要验证是否为杂质峰;
根据以上痛点,可以进行原因分析,逐一攻克,改善措施:①更换色谱柱,考虑色谱柱性能差异影响分离效果;②优化流动相梯度,结合强制降解试验及加标供试品等系统溶液优化出最佳分离条件的流动相梯度;③基于末端吸收的检测波长,增加鬼峰捕集小柱,消除基线中的鬼峰干扰;④未注明柱温的方法,可以通过较大温度差比较柱温对各杂质色谱峰的保留时间的影响。
以痛点分析,对应方法优化的思路,可以较为效率的得到理想拟定方法。
方法经过开发拟定,预验证,看似不会存在很大问题了,然而方法验证中的“痛点”依然存在,比如,回收率未在可接受标准范围内,连续进样的供试品溶液的保留时间一直不稳定等,除了一些超出可接受标准的问题,还存在压力瞬间升高造成漏液等一些异常问题等。本例中有关物质的方法验证专属性中的痛点:随着进样次数的增加,供试品溶液的保留时间前移并趋于稳定,但是因为专属性之初强制降解试验的样品较多,需要统计降解程度和物料平衡,因为保留时间不同(可能存在压力的变化),主峰的峰面积存在一定的差异,在比较主峰降解程度方面就存在了问题:
问题描述:在供试品未破坏进针后,根据预验证中的强制降解条件逐一安排强制降解试验,并分别排样进针,但是中间存在个别酸破坏降解程度不够(与预试验存在差异),需要重新进行酸破坏,于是酸破坏样品排在最后,这时的保留时间与供试品未破坏时的保留时间差了1分多,较第一次稍微剧烈一点的破坏条件,降解程度居然达到了近10倍的降解?
供试品未破坏主峰峰面积:19024;第一次酸破坏主峰峰面积:19017(降解约0%);第二次酸破坏主峰峰面积:17122(降解约10%);
可以得到本例的方法验证痛点:①大浓度供试品溶液存在保留时间波动;②因出峰时间不同,出现的峰面积不同;
根据以上痛点的原因分析:①进样分析之前,流动相需要进行充分的平衡,最好进行一次梯度平衡,并且在破坏试验之前,进样分析加标供试品溶液,使色谱柱充分饱和;②在第二次破坏试验中增加未破坏供试品溶液的进样,考察主峰降解程度的真实性;
以痛点分析,方法验证前的预验证充分设计,对保证验证质量至关重要。
经过转出方的方法学验证的分析方法也未必能一帆风顺的在接收方完成转移,分析方法转移可以采取共同验证、部分验证和对比检验的方式进行,一般转移豁免很少出现。以相对简单的对比检验为例,痛点大概就是QC实验室的偏差了,一批样品,双样中的第二个样品中54min左右出现了一未知色谱峰,如下图2。
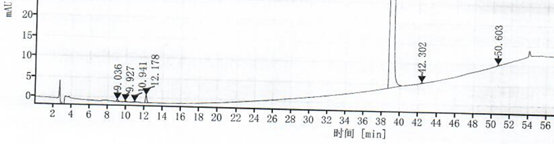
根据以上痛点的原因分析:展开偏差调查,结果是进样小瓶污染。
以痛点分析,结合分析方法本身的耐用性和特殊性(比如末端吸收),需要重点关注并规避常规容易造成偏差的风险因素,比如玻璃仪器的洁净度、塑料滴管和滤膜的浸出物质等。
方法经过了验证和转移应该是相对成熟了,可是因为顶层设计的bug也会带来痛点。比如常规的含量分析,影响因素的样品,检验某个条件时突然在线信号中发现运行时间快结束的时候还有峰未洗脱完,造成连续的第二针进样的初始位置非0点开始运行。
分析本例稳定性检样中的痛点:运行时间内个别稳定性考察条件下存在杂质峰未洗脱完全。
根据以上痛点的原因分析:如果制剂在某个条件下异常不稳定,需要评估拟定方法下的强制降解试验色谱峰洗脱情况。
以痛点分析,制定个性化的含量分析方法,而非经验主义的认为含量的供试品浓度下一定不会发生杂质峰干扰等情况,通过缜密的方法开发设计,能有效的降低稳定性检验中带来的偏差。
综上所述,分析贯穿与ANDA的全生命周期,分析方法与质量标准的拟定关乎产品的质量可控性,在项目开启之初,有序的调研、详细的计划和试验结果的及时分析是保证分析方法的全生命周期高效、高质运行的关键。
药事纵横投稿须知:稿费已上调,欢迎投稿

↓↓点击海报了解药融圈2022年度会议计划↓↓

各位朋友好,觉得本文对您有帮助,请随手点一下下方的在看,以便让你的朋友也能看到哦。



 药选址
药选址