一、药物概况
1 、药物介绍
英文名:Esomeprazole Magnesium Enteric-Coated Capsules
(2)BCS分类
(3)药品成分
化学名称:双-S-5-甲氧基-2-{[(4-甲氧基-3,5-二甲基-2-吡啶基)甲基]亚磺酰-1H-苯并咪唑镁三水合物
分子式:C34H36MgN6O6S2·3H2O
分子量:767.2 g/mol
艾司奥美拉唑镁是一种白色到略带颜色的结晶粉末。它含有3mol溶剂化的水,微溶于水。艾司奥美拉唑镁的稳定性与pH相关,在酸性介质中迅速降解,但在碱性条件下具有可接受的稳定性。在pH 6.8(缓冲液)下,镁盐的半衰期在25℃约为19小时,在37℃约为8小时。
(5)药代动力学参数
(6)药代动力学特征

(7)药理作用
艾司奥美拉唑是奥美拉唑的S-异构体,通过特异性的靶向作用机制减少胃酸分泌,为壁细胞中质子泵的的特异性抑制剂。作用部位和机理:埃索美拉唑为一弱碱,在壁细胞泌酸微管的高酸环境中浓集并转化为活性形式,从而抑制该部位的H+/K+-ATP酶(质子泵),对基础胃酸分泌和刺激的胃酸分泌均产生抑制。[1,7]
转运体:MDR1(底物、抑制剂);OAT3(抑制剂)
代谢酶: CYP2C19(底物、抑制剂);CYP3A4(底物)
不建议联合使用质子泵抑制剂和阿扎那韦和奈非那韦。预期与质子泵抑制剂合用,可导致阿扎那韦血药浓度大幅下降,并且可能失去疗效,产生耐药性。预期与质子泵抑制剂合用后,可能使沙奎那韦(常与阿扎那韦合用)浓度升高,导致其毒性增加,因此,需要减少用药剂量。
已有报告,奥美拉唑(艾司奥美拉唑为其对映异构体)可与一些逆转录抗病毒药物发生相互作用,但这些相互作用所具有的临床意义和作用机制并不完全清楚。在奥美拉唑治疗期间,胃pH值升高,可改变逆转录抗病毒药物的吸收。其它可能的相互作用机制为通过CYP2C19发挥作用。
艾司奥美拉唑可抑制胃酸分泌,因此,对于生物利用度会受到胃pH值重大影响的药物(如酮康唑、伊曲康唑、阿扎那韦、铁盐和地高辛),艾司奥美拉唑可影响其吸收。
艾司奥美拉唑广泛地在肝脏中经CYP2C19和CYP3A4代谢。体外和体内研究显示,艾司奥美拉唑不太可能抑制CYP1A2、2A6、2C9、2D6、2E1和3A4,预期本品与经这些CYP酶代谢药物间的相互作用不具有临床相关性。
上市后的报告显示,对于接受华法林和艾司奥美拉唑联合治疗的患者,其凝血酶原检测结果有变化。凝血酶原国际标准化比值(INR)和凝血酶原时间增加可导致患者出现异常出血,甚至发生死亡。因此,对于接受质子泵抑制剂和华法林联合治疗的患者,需要对其INR和凝血酶原时间增加的情况进行监测。
艾司奥美拉唑抑制CYP2C19,后者为本品的主要代谢酶。因此,当艾司奥美拉唑与经CYP2C19代谢的药物(如地西泮、西酞普兰、丙米嗪、氯米帕明、苯妥英等)合用时,这些药物的血浆浓度可被升高,可能需要降低剂量。特别是本品用于按需治疗时,更应考虑这一点。合用本品30mg可使经CYP2C19代谢的地西泮的清除下降45%。
合用本品40mg,可使癫痫患者的血浆苯妥英的谷浓度上升13%。因此,苯妥英治疗期间,当合用或停用本品时,建议监测苯妥英的血药浓度。奥美拉唑40mg每日一次分别增加了voriconazole(伏立康唑:一种CYP2C19的底物)Cmax和AUCτ15%和41%。艾司奥美拉唑经CYP2C19和CYP3A4代谢。艾司奥美拉唑与CYP3A4抑制剂克拉霉素(500mg,每日二次)合用,可使机体对艾司奥美拉唑的暴露(AUC)加倍。艾司奥美拉唑与CYP2C19,CYP3A4共同抑制剂合用可使艾司奥美拉唑的暴露增加两倍以上。CYP2C19和CYP3A4的抑制剂voriconazole(伏立康唑)增加奥美拉唑AUCτ280%。以上两种情形艾司奥美拉唑的剂量不必作常规调整。然而对于严重肝损和需要长期治疗的患者应该考虑调整本品的剂量。
氯吡格雷部分经由CYP2C19酶代谢为其活性代谢产物。合并使用艾司奥美拉唑40mg可降低氯吡格雷活性代谢产物的血浆浓度,进而降低血小板抑制作用。因此,应避免将本品与氯吡格雷合并使用。在使用本品时应考虑其他抗血小板治疗。
药物引起的胃酸降低可导致肠嗜铬样细胞增生和嗜铬粒蛋白A水平增加,对神经内分泌瘤的检查造成干扰。
本品与他克莫司合并用药可导致他克莫司血药浓度增加。
艾司奥美拉唑、克拉霉素与阿莫西林联合用药治疗后,可导致艾司奥美拉唑和14-羟基克拉霉素的血药浓度升高。禁止联合使用克拉霉素与西沙必利、匹莫齐特、阿司咪唑、特非那定、麦角胺或二氢麦角胺等药物进行治疗。
病例报告、已发表的群体药代动力学研究和回顾性分析提示,PPIs和甲氨蝶呤(主要是高剂量;参见甲氨蝶呤处方信息)合并使用可能会增加甲氨蝶呤和/或其代谢产物的血清浓度,延长高血清浓度的持续时间。然而,尚未开展任何关于甲氨蝶呤和PPIs的正式药物相互作用研究。
在一些患者中有报道,当与PPI联合给药时,甲氨蝶呤水平会升高。当使用高剂量甲氨蝶呤治疗时,可考虑艾司奥美拉唑的暂时撤药。
(10)适应症
胃食管反流性疾病(GERD)-糜烂性反流性食管炎的治疗,已经治愈的食管炎患者防止复发的长期维持治疗,胃食管反流性疾病(GERD)的症状控制与适当的抗菌疗法联合用药根除幽门螺杆菌,并且愈合与幽门螺杆感染相关的十二指肠溃疡,防止与幽门螺杆菌相关的消化性溃疡复发。
在艾司奥美拉唑镁的临床试验中已确定或怀疑有下列不良反应,这些反应均没有剂量相关性。
常见反应:(>1>100,<1/10),头痛、腹痛、腹泻、腹胀、恶心/呕吐、便秘。少见反应:(>1>1000,<1/100,皮炎、瘙痒、荨麻疹、头昏、口干。)
二、研发情况
艾司奥美拉唑是质子泵抑制剂药物,最先由瑞典AstraZeneca AB公司研制,2007年获批进入中国,2019年阿斯利康(AstraZeneca)获得本地化生产资格。
东阳光药业是国内首个按照新注册分类3类申报艾司奥美拉唑镁肠溶胶囊上市申请的企业,并成功拿下国内艾司奥美拉唑镁肠溶胶囊制剂批文,且视同通过一致性评价。目前国内按照新注册分类申报艾司奥美拉唑肠溶胶囊的企业还有正大天晴、石药集团;自2017年至2020年9月,艾司奥美拉唑镁肠溶胶囊在国内已有8家药企提交临床试验登记。
1、销售价格
目前,质子泵抑制剂是治疗消化性溃疡最先进的一类药物,它通过高效快速抑制胃酸分泌和清除幽门螺旋杆菌而达到快速治愈溃疡的目的,是近十几年来临床用于治疗酸相关性疾病最广泛、疗效最好的药物。
奥美拉唑是第一个用于临床的质子泵抑制剂,由阿斯利康开发,于1989年在美国上市,2006年全球奥美拉唑年最高销售额超过60亿美元,继奥美拉唑之后,全球相继开发了兰索拉唑、泮托拉唑、埃索美拉唑和雷贝拉唑等多个质子泵抑制剂,2007年全球整体市场销售额峰值超过170亿美元。由于专利到期,在仿制药冲击下,全球市场逐渐呈现下坡态势。
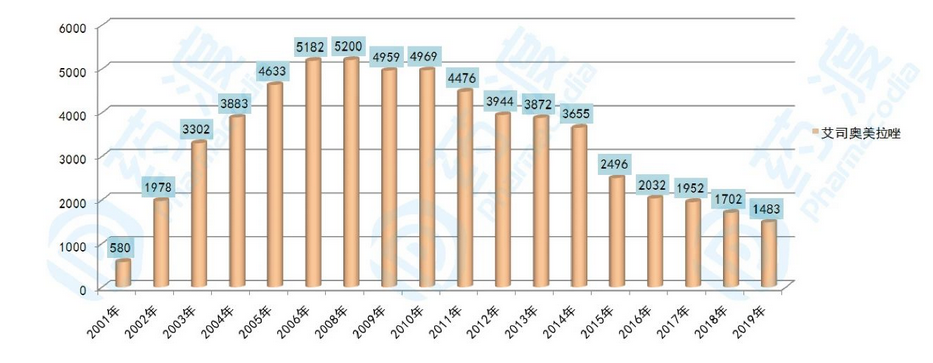
艾司奥美拉唑由阿斯利康研制开发,商品名为Nexium®,2000年,埃索美拉唑镁口服制剂在瑞典上市,2003年该公司又开发了注射用埃索美拉唑钠。艾司奥美拉唑为奥美拉唑的S-异构体,主要通过特异性的靶向作用机制减少胃酸分泌,为质子泵特异性抑制剂。埃索美拉唑上市后,很快替代专利到期的奥美拉唑市场,是最成功的异构体开发先例。阿斯利康的埃索美拉唑2001年销售额为5.8亿美元,2001年销售额达到峰值52亿美元,2019年销售额为14.83亿美元,自2001-2019年总销售额已超过600亿美元。
图1:1999-2019年全球艾司奥美拉唑市场情况(单位:百万美元)
艾司奥美拉唑于2003年由阿斯利康在国内上市,剂型为口服肠溶片。2013年重庆莱美药业艾司奥美拉唑肠溶胶囊获得生产批文,打破外企垄断的局面。该产品是目前市场上唯一的异构体质子泵抑制剂。
阿斯利康在国内逐步实现了从奥美拉唑到艾司奥美拉唑的更新换代。2012年之前由进口企业阿斯利康一家独占国内市场。2013年,重庆莱美药业肠溶胶囊获得生产批文,打破外企垄断局面。近二年来,国内众多实力较强的企业进入艾司奥美拉唑市场,竞争尤其激烈。
据国内样本医院数据统计,2015-2019年,艾司奥美拉唑销售额实现了快速增长。2017年用药金额为12.15亿元,2018年用药金额为13.86亿元,2019年用药金额为16.61亿元,较同期增长19.86%。其中,2019年,阿斯利康的产品用药金额为10.20亿元,占61.39的份额;正大天晴药业的产品用药金额为3.38亿元,占20.30的份额;江苏奥赛康药业的产品用药金额为1.49亿元,占8.96的份额;重庆莱美药业/朗天药业的产品用药金额为1.55万元,占9.33的份额。进口企业的产品占据绝对优势,正大天晴药业增长较快。
截止目前,国内已上市埃索美拉唑注射剂、片剂和胶囊剂已有20多家,不过埃索美拉唑申报依然高涨,一大波堵在路上。据CDE数据检索,国内正在申请类型新药、仿制和已有国家标准的艾司奥美拉唑,受理号近300个,其中177个制剂。
我国质子泵抑制剂市场多年处于高速增长期以来,近二年也逐年呈下降态势。其中兰索拉唑、泮托拉唑、奥美拉唑主力产品市场增长略显乏力,新一代质子泵抑制剂埃索美拉唑在市场上十分活跃。
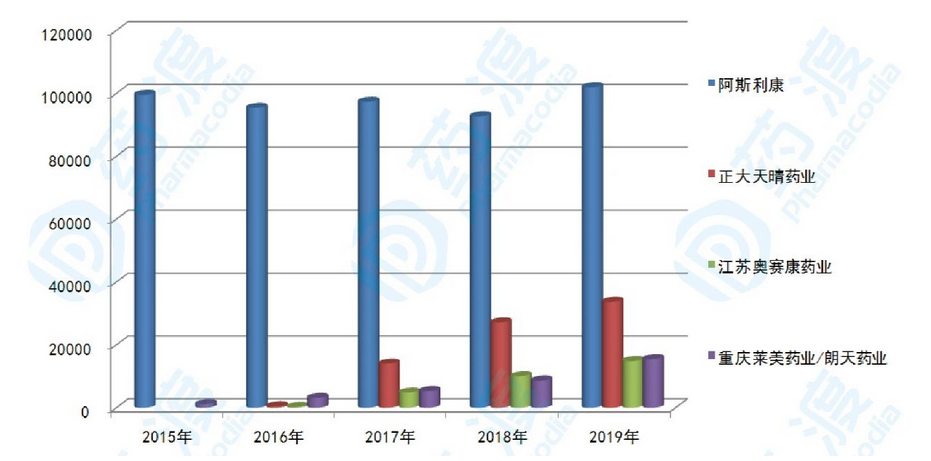
图2:2015-2019年国内样本医院艾司奥美拉唑竞争情况(单位:万元)
据国内样本医院数据统计,2015-2019年,艾司奥美拉唑销售额实现了快速增长。2017年用药金额为12.15亿元,2018年用药金额为13.86亿元,2019年用药金额为16.61亿元,较同期增长19.86%。其中,2019年,阿斯利康的产品用药金额为10.20亿元,占61.39的份额;正大天晴药业的产品用药金额为3.38亿元,占20.30的份额;江苏奥赛康药业的产品用药金额为1.49亿元,占8.96的份额;重庆莱美药业/朗天药业的产品用药金额为1.55万元,占9.33的份额。进口企业的产品占据绝对优势,正大天晴药业增长较快。
截止目前,国内已上市埃索美拉唑注射剂、片剂和胶囊剂已有20多家,不过埃索美拉唑申报依然高涨,一大波堵在路上。据CDE数据检索,国内正在申请类型新药、仿制和已有国家标准的艾司奥美拉唑,受理号近300个,其中177个制剂。
我国质子泵抑制剂市场多年处于高速增长期以来,近二年也逐年呈下降态势。其中兰索拉唑、泮托拉唑、奥美拉唑主力产品市场增长略显乏力,新一代质子泵抑制剂埃索美拉唑在市场上十分活跃。
国内已上市的PPI抑制剂有6个,艾司奥美拉唑、奥美拉唑、兰索拉唑、雷贝拉唑、泮托拉唑、艾普拉唑,相关制剂批文300多个,涉及医药企业近200家。在国内样本医院市场中,PPI抑制剂一直是医院用药金额排名较为靠前品种,2018年整体市场销售额超过70亿元。2018年,注射剂PPI抑制剂销售额为45.87亿元,占据64.6%的份额,口服PPI抑制剂销售额为24.24亿元,占据35.4%的份额,注射剂多年来一直占据主导地位。
面对PPI抑制剂的巨大市场,各大医药企业为了尽快抢占市场,在PPI抑制剂领域都已做了全面布局,已有众多企业切换到一致性性评价赛道。从受理号来看,注射剂28个,口服的制剂11个,注射剂申报占据71.8%,口服申报占据28.2%,在抢占PPI抑制剂一致性评价中,各厂家还是更注重注射剂一致性评价。
艾司奥美拉唑是质子泵抑制剂药物,原研是由阿斯利康开发的奥美拉唑的 S-异构体,目前国内口服制剂肠溶胶囊只有莱美药业、片剂只有原研阿斯利康。国内首个国产艾司奥美拉唑口服制剂来自莱美药业研发的艾司奥美拉唑肠溶胶囊,于2013年8月23日获批上市,目前尚未通过一致性评价,该企业独家销售该产品。
东阳光药业是国内首个按照新注册分类3类申报艾司奥美拉唑镁肠溶胶囊上市申请的企业,2018年6月,以同一生产线生产并于2017年在欧盟上市,申请国内上市的仿制药被纳入优先审评程序。
本次东阳光药业成功拿下国内艾司奥美拉唑镁肠溶胶囊制剂批文,且视同通过一致性评价,有望搅动国内重磅产品艾司奥美拉唑大市场。目前国内按照新注册分类申报艾司奥美拉唑肠溶胶囊的企业还有正大天晴、石药集团;肠溶片剂目前报上市的企业有苏州特瑞药业、江西山香药业等。
全部的CDE临床备案信息(截止至2020年09月09日):
1) 江苏海岸药业有限公司,空腹加餐后,空腹-12 h,餐后-24 h,108例;
2) 重庆莱美药业股份有限公司,餐后,54例,-14 h;
3) 江苏正大清江制药有限公司,空腹,24例,-12 h;
4) 青岛百洋制药有限公司,空腹,66例,-24 h;
5) 青岛百洋制药有限公司,餐后,66例,-24 h;
6) 青岛百洋制药有限公司,空腹,66例,-24 h;
7) 天方药业有限公司,空腹加餐后,96例,-12 h;
8) 江苏正大清江制药有限公司,空腹加餐后,64例,-12 h;
9) 江苏中邦制药有限公司,空腹加餐后,20例,-24 h。
五、参考文献及资料
[1] Draft Guidance on Esomeprazole Magnesium(Delayed release capsule; oral).
[4] Wang-Smith Laurene, Fort John, Zhang Ying et al. Pharmacokinetics and relative bioavailability of a fixed-dose combination of enteric-coated naproxen and non-enteric-coated esomeprazole magnesium.[J] .J Clin Pharmacol, 2012, 52: 670-80.
[5] Sostek M B, Chen Y, Skammer W et al. Esomeprazole administered through a nasogastric tube provides bioavailability similar to oral dosing.[J] .Aliment. Pharmacol. Ther., 2003, 18: 581-6.
[6] 侯贻平. 埃索美拉唑肠溶胶囊人体生物等效性分析[J]. 中外女性健康研究,2018(10):53+93.
[7] Esomeprazole Public Assessment Report(欧盟).
[8] Sostek Mark B, Chen Yusong, Andersson Tommy, Effect of timing of dosing in relation to food intake on the pharmacokinetics of esomeprazole.[J] .Br J Clin Pharmacol, 2007, 64: 386-90.
[9] Antoniou T, Macdonald EM, Hollands S, et al. Proton pump inhibitors and the risk of acute kidney injury in older patients: a population-based cohort study [J]. CMAJ Open, 2015, 3(2): E166-171. DOI: 10.9778/cmajo.20140074.
[10] Qiu T, Zhou J, Zhang C. Acid-suppressive drugs and risk of kidney disease: a systematic review and meta-analysis [J]. J Gastroenterol Hepatol, 2018. DOI:10.1111/jgh.14157.
[11] Kamal F, Khan MA, Molnar MZ, et al. The association between proton pump inhibitor use with acute kidney injury and chronic kidney disease [J]. J Clin Gastroenterol, 2018, 52(6): 468-476. DOI: 10.1097/MCG.0000000000001035.
[12] 钱悦, 倪兆慧. 质子泵抑制剂相关性肾损伤新认识 [J]. 中国血液净化, 2018, 17(03): 197-200. DOI: 10.3969/j.issn.1671-4091.2018.03.012.
[13] Xie Y, Bowe B, Li T, et al. Proton pump inhibitors and risk of incident ckd and progression to ESRD [J]. J Am Soc Nephrol, 2016, 27(10): 3153-3163. DOI: 10.1681/ASN.2015121377.
[14] 高飞萌,宋智慧. 艾司奥美拉唑镁肠溶片致肾损伤[J]. 药物不良反应杂志, 2020, 22(6): 381-382. DOI: 10.3760/cma.j.cn114015-20200305-00219.
[15] Wijarnpreecha K, Thongprayoon C, Chesdachai S, et al. Associations of proton-pump inhibitors and H2 receptor antagonists with chronic kidney disease: a meta-analysis [J]. Dig Dis Sci, 2017, 62(10): 2821-2827. DOI: 10.1007/s10620-017-4725-5.
文章来源:都正生物官网 www.duxact.com
点击文末“阅读原文”进入官网
长沙都正生物科技股份有限公司

长沙都正生物科技股份有限公司成立于2016年1月,坐落在长沙高新区,现有员工300余人。为全球生物医药企业提供药物、医疗器械和诊断试剂临床评价“一站式”服务。
分析实验室4800平方米,按照ISO 17025体系标准建设,仪器设备先进,包括光谱色谱分析检测、数据管理与生物信息分析、基因检测、免疫生化分析四大平台。
公司集“产、学、研”于一体,立志领跑药物临床评价、实验室信息化建设、医药大数据挖掘等新技术领域。
◆ 药物评价:为国内外200余家企业提供临床研究服务,以高水平的方案设计和高效率的临床管理,助力多家药企“全国首家”获批。
◆ 创新技术:全球首次发现并证实何首乌肝损伤特异性生物标志物,具有划时代意义;全国首家取得TMAO检测技术专利,并成功实现产业转化。
◆ 大数据挖掘:通过基因组学信息挖掘,成功为我国某企业创新药物上市提供支持。
◆ 信息化建设:围绕药学和临床,自主研发8款信息化系统,覆盖药物评价全过程,打破国际垄断,填补国内空白,建立行业标准。
目前,都正生物已成为“硬件先进、管理规范、分析能力强”的研发中心。都正人胸怀“立业报国、为国分忧”的理想,以“每天努力一点点”的精神,不断开拓进取,为我国生物医药产业做出贡献!
地址:长沙市高新区麓天路28号麓谷科技产业园C10栋
邮箱:bd@duxact.com
电话:0731-85681666-8006
创 新 ● 求 实

-- 每天努力一点点 --














 个人中心
个人中心
 我是园区
我是园区




