2020年7月30日,默沙东(MSD)宣布抗PD-1单抗帕博利珠单抗(K药)两项新的补充生物制品许可申请(sBLA)已获得美国FDA受理。一项sBLA是关于加速批准K药联合化疗用于治疗肿瘤表达PD-L1(联合阳性评分[CPS]≥10)的局部复发不可切除或转移性三阴性乳腺癌(TNBC)患者的申请。另一项sBLA关于K药联合化疗作为高危早期TNBC患者的新辅助治疗,单药作为手术后的辅助治疗。这是继阿替利珠单抗在乳癌获批后的久违突破,也掀起了免疫在乳癌早期和晚期免疫应用的全面爆发。一起看一下目前乳癌免疫的研究数据。
三阴乳癌作为乳腺癌中TMB较高的亚型,是乳癌中较为适合免疫治疗的。基于18年阿替利珠单抗的Impassion130研究以及此次K药优先审批依托的KEYNOTE-355研究,确立了化免联合在晚期三阴乳癌的一线地位。看一下具体数据。
阿替利珠单抗+白蛋白紫杉醇的Impassion130研究是首个获批的三阴乳癌化免方案。采用阿替利珠单抗联合白蛋白紫杉醇一线治疗晚期初治三阴乳癌患者。结果显示,相对于白紫单药组(n=451),化免联合组(n=451)PFS显著延长,中位PFS分别为
7.2个月
和5.5个月(HR 0.8,95%CI:0.69-0.92,P=0.002);PD-L1阳性亚组:Atezolizumab联合组对比安慰剂组进展或死亡风险显著降低,中位PFS分别为
7.5个月
和5.0个月(HR 0.62,95%CI:0.49-0.78),1年的PFS率,Atezolizumab组高于安慰剂组,分别为
29.1%
和16.4%。
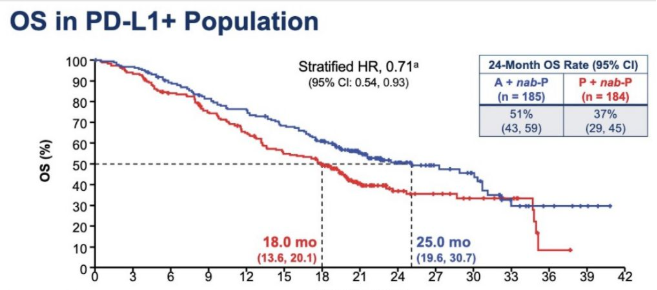
OS未观察到显著统计学差异,但在PD-L1阳性患者中,Atezolizumab +白蛋白紫杉醇组对比安慰剂+白蛋白紫杉醇组,中位OS分别为25个月 和18个月(HR 0.71,95% CI: 0.54-0.93),有7个月 的显著改善。
2019年3月11日, FDA加速获批,打破了乳癌免疫的零突破。
KEYNOTE-355是一项随机、双盲的Ⅲ期研究,旨在评估帕博利珠单抗联合化疗对比安慰剂联合化疗用于既往未接受过治疗的局部复发不可手术或转移性三阴性乳腺癌的疗效。
研究入组了未接受过治疗的局部复发不可手术或转移性三阴性乳腺癌,DFI≥6个月,2:1随机至接受
帕博利珠单抗+化疗(白蛋白紫杉醇或紫杉醇或吉西他滨+卡铂)
或安慰剂+化疗。在研究人群中CPS≥1的患者占75%,CPS≥10的患者占38.9%。研究用的化疗方案紫衫占50%,吉西他滨和卡铂占50%。患者中30%为出诊IV期,无病间期≥12月的患者占50%,无病间期≤12个月的患者22.3%和17.8%。帕博利珠单抗联合化疗组(n= 565)以及化疗组(n= 281)分别中位随访17.5和15.5个月。主要终点包括PD-L1阳性(CPS≥10和CPS≥1)及ITT人群的PFS和OS。2020ASCO 年会公布了KEYNOTE-355的PFS数据。
K药+化疗 PFS为9.7个月,6个月PFS率65.0%,12个月PFS率46.9%;
安慰剂+化疗 PFS 为5.6个月,6个月PFS率46.9%,12个月PFS率23.0%;
K药组降低疾病进展风险35%(p=0.0012)。
(2)但是在PD-L1 CPS≥1和全体患者中,PFS又延长趋势但无统计学差异。
K药+化疗 PFS为7.6个月,6个月PFS率56.4%,12个月PFS率31.7%;
安慰剂+化疗 PFS 为5.6个月,6个月PFS率46.6%,12个月PFS率19.4%;
K药组降低疾病进展风险26%(p=0.0014)。
K药+化疗 PFS为7.5个月,6个月PFS率55.4%,12个月PFS率29.8%;
安慰剂+化疗 PFS 为5.6个月,6个月PFS率7.846.9%,12个月PFS率20.9%;
基于KEYNOTE-355研究,K药获得了优先审批。
表1:晚期三阴乳癌化免研究
对于新辅助盛行的乳癌治疗,免疫已经开展了多项临床研究。集中于高危乳癌,喜忧参半。
KEYNOTE-522是一项加入安慰剂进行对照,评价帕博利珠单抗联合化疗序贯帕博利珠单抗辅助治疗方案对早期三阴性乳腺癌(TNBC)的治疗疗效的Ⅲ期临床研究。KEYNOTE-522研究入组新诊断的T1c N1-2或T2-4 N0-2TNBC患者。1174例入组患者2:1随机入组治疗组和对照组。治疗组(n=784)患者选择
卡铂+紫杉序贯多柔比星/表柔比星+环磷酰胺,同时全程联合帕博利珠单抗新辅助治疗,术后予以帕博利珠单抗辅助治疗。
而对照组(n=390)则选择卡铂+紫杉序贯多柔比星/表柔比星+环磷酰胺,术后也仅选择安慰剂进行辅助治疗。
主要研究终点是pCR和EFS。pCR定义为ypT0/Tis ypN0,在ITT人群中进行评估,EFS通过研究者在ITT人群中进行评估。次要研究终点是ypT0 ypNO和ypT0/Tis替代定义的pCR,OS,PD-L1阳性人群的pCR、EFS、OS以及所有接受治疗的患者中的安全性。2019ESMO大会上公布了该研究的结果。
(1)对比化疗+安慰剂组,帕博利珠单抗+化疗组显现出了显著的
pCR(ypT0/Tis ypN0)获益,两组对比为 64.8% (95% CI 59.9-69.5) vs 51.2% (95% CI 44.1-58.3),P=0.00055 ;次要研究终点中,帕博利珠单抗+化疗组依然优势明显:pCR(ypT0 ypN0 )59.9% vs 45.3%,pCR(ypT0/Tis )68.6% vs 53.7%。这一优势在PDL1阳性人群中更为明显, pCR (ypT0/Tis ypN0) 为
68.9%
vs 54.9%,而在PD-L1- 人群中
pCR (ypT0/Tis ypN0) 为 45.3% vs 30.3%。
(2)帕博利珠单抗联合化疗序贯帕博利珠单抗在EFS方面呈现除了良好的趋势(HR0.63,95% CI 0.43-0.93),18个月EFS率91.3% vs 85.3%。
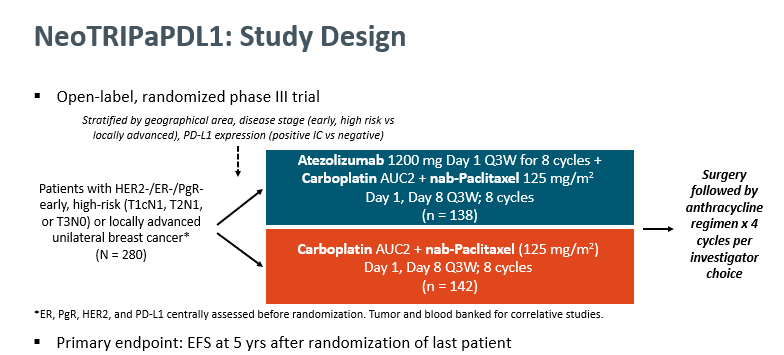
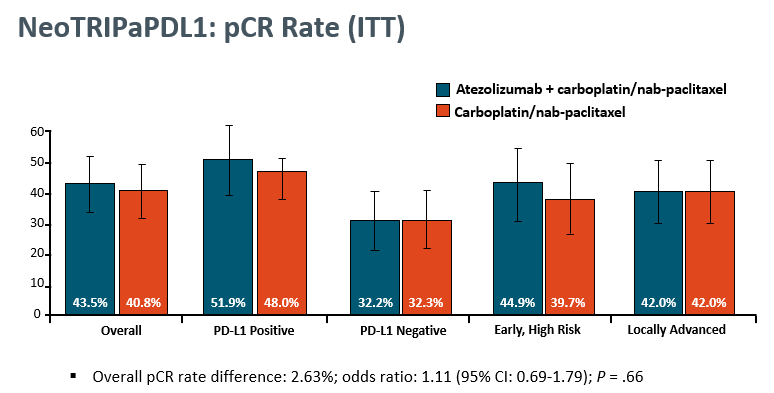
III期临床研究NeoTRIPaPDL1试验,纳入了三阴高危的早期乳腺癌患者(T1cN1、T2N1、T3N0),随机分组至试验组(阿替利珠单抗+白紫+卡铂8周期治疗+手术+术后采用蒽环类方案4周期辅助)或无阿替利珠单抗的对照组。主要研究终点是5年的EFS。
但据目前的病理缓解率数据显示,加入免疫并未提升pCR率。
因此,专家们也在比较分析522研究和NeoTRIPaPDL1的阴阳结果的差异性,筛选人群?方案设计?为早期乳癌的免疫新辅助的加入提出了要求。
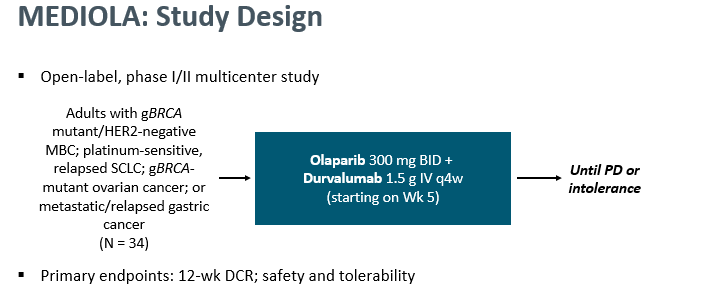
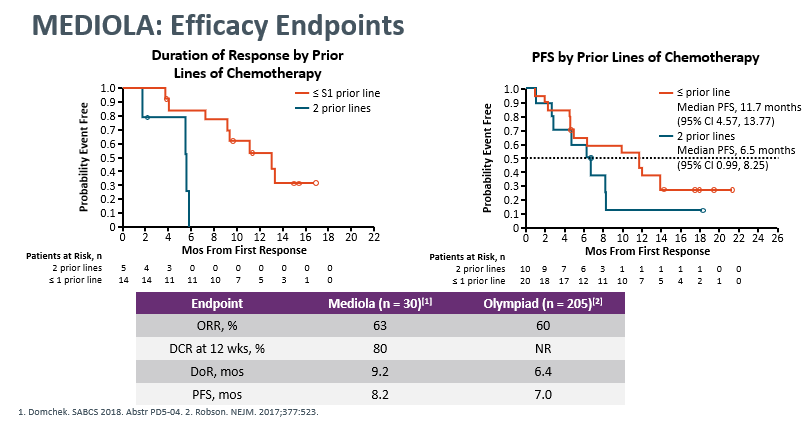
BRCA突变在HER1阴性的三阴乳癌中有近15%的突变率,在MEDIOLA研究中,采用度伐利尤单抗联合奥拉帕利治疗gBRCA突变的铂类敏感复发的三阴乳癌患者,
有效率可以达到63%,与单用PARP抑制剂相比,能延长PFS,8.2:7.0月,期待更成熟的研究结果。
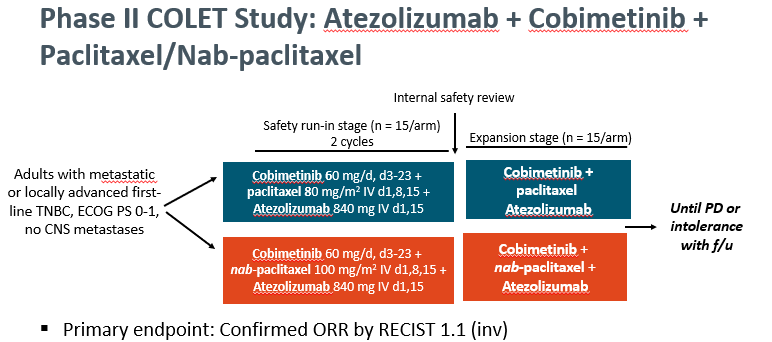
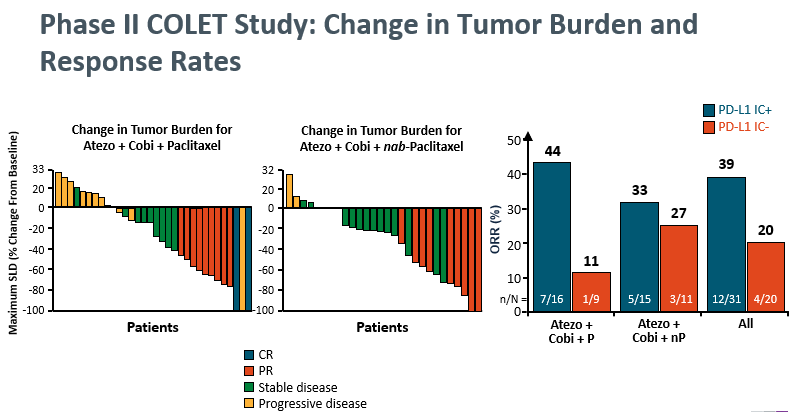
在II期COLET研究中,采用阿替利珠单抗联合考比替尼联合白紫一线治疗晚期初治的三阴乳癌,获得了44%的有效率。
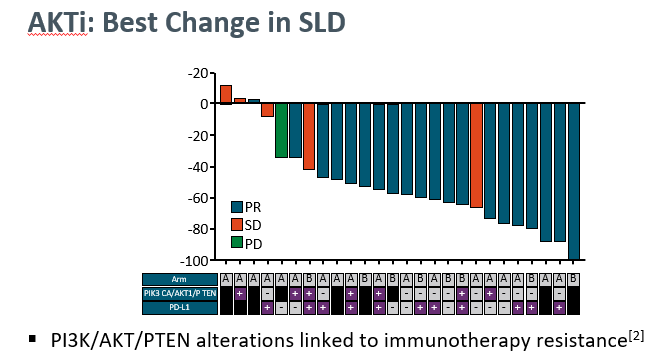
AKT通路在研究中显示与免疫耐药相关,因此开展AKTi的Ib期临床研究,采用AKT抑制剂Ipatasertib联合阿特利珠单抗+紫杉醇或白紫治疗晚期初治的三阴乳癌患者。
在初期有效率统计中,获得了69%的PR率,非常可观。
阿帕替尼是一种新型口服小分子抗血管生成制剂。2019年的ASCO大会上,由中山大学孙逸仙纪念医院宋尔卫、刘强教授团队开展的PD-1抑制剂卡瑞利珠单抗(SHR1210)联合阿帕替尼治疗晚期三阴性乳腺癌的II期研究被收录作为壁报展示(摘要号1066)。研究一共入组了34例既往接受过三线以内系统治疗的晚期三阴性乳腺癌(TNBC)患者,并1:1随机接受阿帕替尼联合卡瑞利珠单抗治疗。在28例疗效可评估患者中,ORR为46.2%,卡瑞利珠单抗(SHR1210,200mg Q2W)与阿帕替尼(250 mg)的联用明显提高ORR,达到单用PD-L1抗体(18.5%有效率)的两倍多;疾病控制率(DCR)为65.4%。PFS和OS数据尚未成熟。
参考来源:
https://www.onclive.com/view/fda-approvals-sought-for-2-pembrolizumab-indications-in-tnbc
声明:本资料中涉及的信息仅供参考,请遵从医生或其他医疗卫生专业人士的意见或指导。
本文版权归汝爱一生所有,任何个人或机构转载需获得汝爱一生授权,在授权范围内使用,并标注来源“汝爱一生”。
点击在看 不迷路















 个人中心
个人中心
 我是园区
我是园区





