炎症性肠病(IBD),主要包括溃疡性结肠炎(UC)和克罗恩病(CD),是一组慢性、特发性、异质性肠道炎症性疾病,在世界范围内尤其欧美地区影响非常广泛。该领域近年来上市了多款重磅药物,并且大量在研产品也即将进入市场。IBD药物治疗格局正在迅速发生改变。那么究竟有哪些改变?变化的趋势是什么?biotech公司在立项上该如何应对?本文将根据我们收集的资料以及以往的项目经验尝试对这些问题进行回答。
中重度IBD治疗加速进入以生物制剂为核心的时代

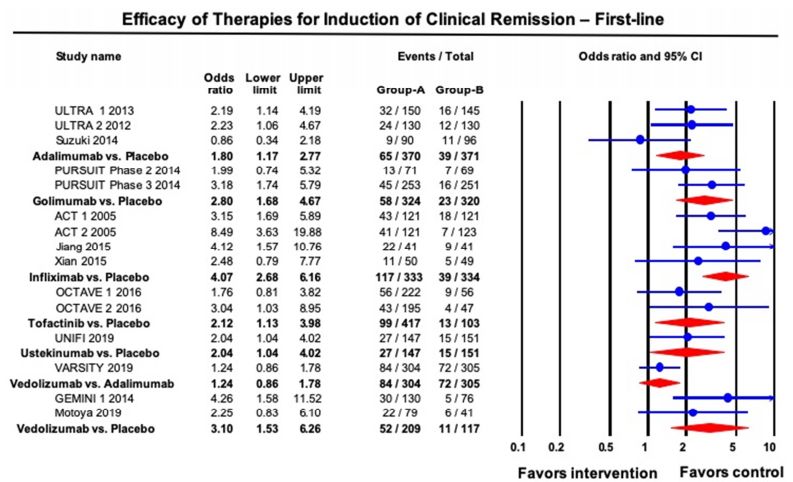
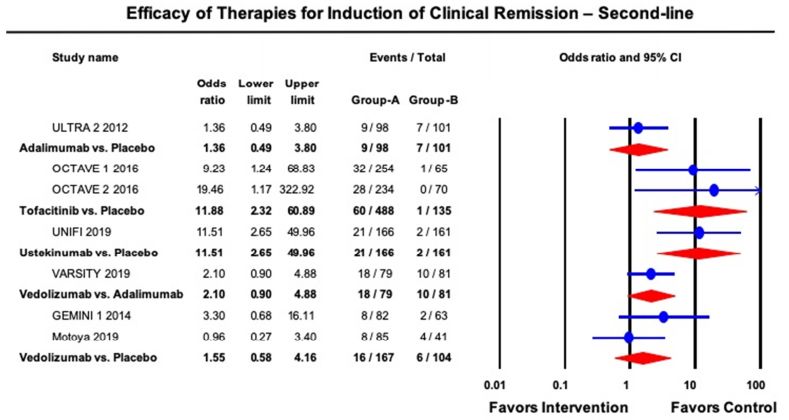
尽管有多个生物制剂上市,但仍然有较多未被满足的临床需求
在研新药百花齐放,缓解临床需求,但加剧竞争

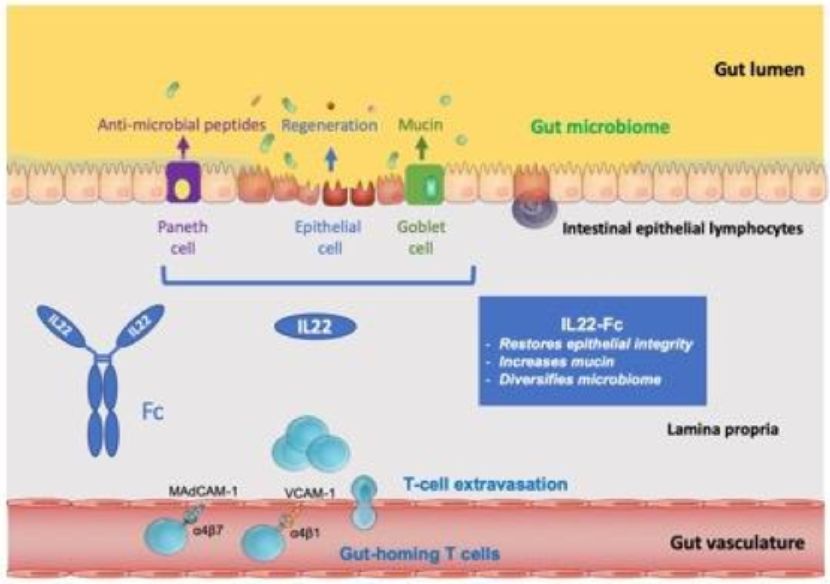
随着新药的不断研发,IBD未被满足的临床需求一定会得到一定程度地缓解,但同时也会带来竞争的加剧。以抗粘附(包括T细胞归巢)药物为例:除Natalizumab、Vedolizumab、Etrolizumab,在研的SHP647和口服的α4β7小分子抑制剂等之外,还包括在研的ozanimod、etrasimod等一众S1PRa类药物。选手众多且具有相似的作用机理,竞争关系非常复杂。S1PR小分子激动剂相对抗α4β7抗体最大的优势就是可以口服,但S1PRa存在理论上的进行性多灶性白质脑病(PML)风险(尽管诺华报道芬戈莫德没有明显的PML),除非具有肠道特异性,否则将有可能受限于治疗窗,影响对IBD的疗效。而且α4β7靶点也正在开发口服小分子抑制剂,对S1PRa类药物不利。Natalizumab受到PML的限制基本已经退出了IBD的竞争,Vedolizumab暂时取得领先,但罗氏的Etrolizumab (RG7413/rhuMAb Beta7) 靶向β7亚单位,同时拮抗T细胞的归巢和驻留,有望进一步提高疗效。最近,在抗TNFα难治性CD患者的3期临床试验BERGAMOT中显示了早在6周和持续14周的比Vedolizumab更高的症状和内镜缓解率。而且Etrolizumab也同时开发了SC版本。很难说长效的SC版本和PO版本那个更具有优势,这更加剧了该MOA药物的竞争。
新药预期市场份额缩水,开发难度加大
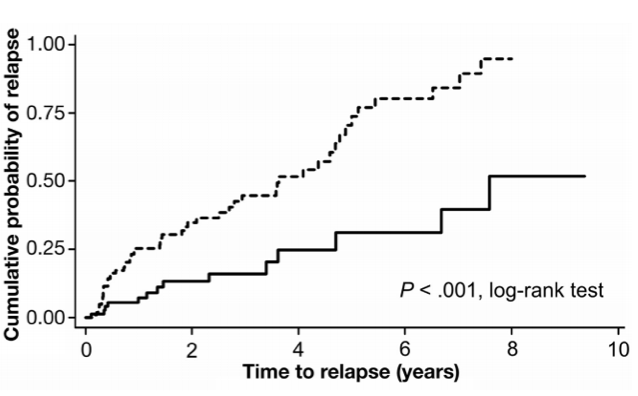
《clinical gastroenterology and hepatology》发表的一篇论文显示停用英夫利昔单抗会增加UC患者复发风险。目前,尚缺乏足够证据给出何时停用IFX的推荐意见。对IFX维持治疗达1年、保持临床无激素缓解、黏膜愈合、CRP正常者,可考虑停用IFX,继以免疫抑制剂维持。停药后复发患者重新给予IFX,80%患者可再次获得临床应答。
如下图所示,一项长期的随访研究告诉我们IFX单抗5年的复发风险约为25%,10年的复发风险约为50%,我们可以大致推出持续使用IFX5年的缓解率为75%,10年的缓解率为50%。
Ustekinumab有一项针对CD的3年随访研究。该试验入组患者近400人,临床缓解率从60%左右(由于0周时入组的患者是主要8w诱导缓解期结束时有响应的患者,因此缓解率起始就低于100%)下降至40%左右。表面上看Ustekinumab似乎维持缓解的效果没有IFX好,但实际上仔细剖析试验设计可以发现,该试验有近一半左右的入组患者(来自于UNITI-1研究)有anti-TNFα生物制剂难治性的历史。而从该试验结果中可以看出,这类患者在8周时诱导缓解率相对更低,44周时的维持缓解率也更低。因此,这部分患者是造成152周时缓解率下滑近三分之一的主要动力。如果剔除这部分患者,则剩下的入组患者(来自于UNITI2)44周时维持缓解率仅下降了6%左右,预期152w时下降不超过20%。这与IFX持续给药的维持缓解试验的结果近似。
其实,IFX复发的患者中还有一部分是因为产生了抗药抗体。但这部分患者可以通过优化药物剂量或者更换免疫原性更低的其它TNFα抗体,比如阿达木单抗重新获得缓解。
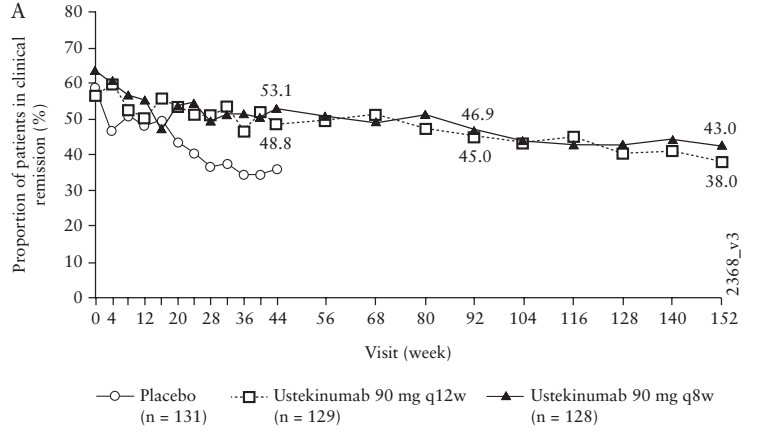
Ustekinumab治疗152周内CD患者诱导和维持临床缓解的患者比例
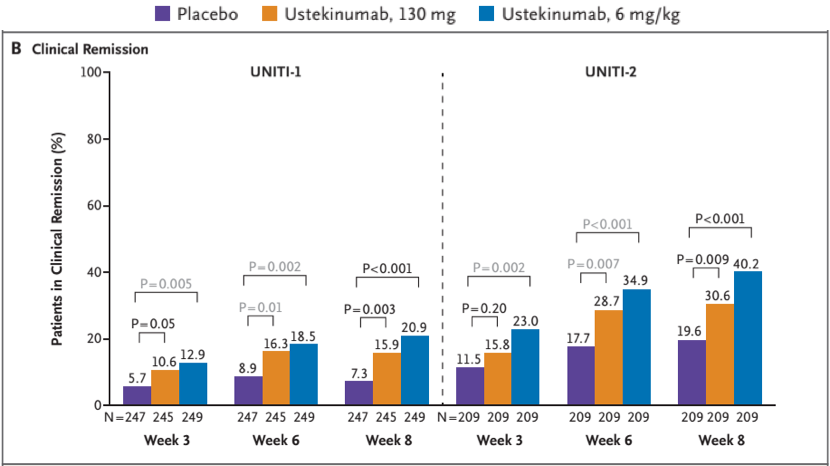
CD患者接受Ustekinumab治疗诱导临床缓解的比例
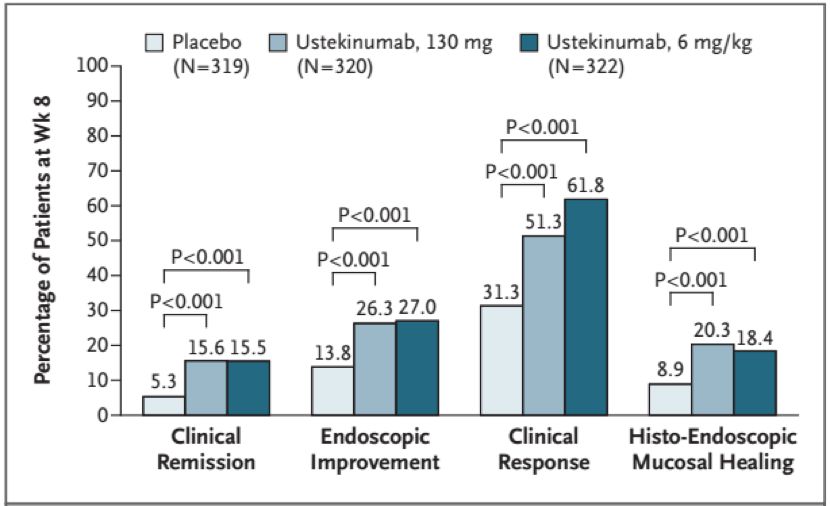

除了市场份额已经开始逐渐减少,新药开发需要跨过的barrier也越来越高。仅考虑新MOA的产品(非安全性或给药途径改良产品或联合治疗定位的产品),如果想进入后线治疗,其临床试验的入组人群将至少是anti-TNFα、Vedolizumab或Etrolizumab治疗过无效、耐药或无法耐受的患者甚至是Ustekinumab或Tofactinib治疗过无效、耐药或无法耐受的患者,难度可想而知。如果想进入一线治疗(biologic naive),则大概率需要做与现有一线主要生物制剂的头对头临床试验,以获得充分的数据,从而获得临床医生的支持,才能在一线激烈竞争中获得一席之地。
IBD的发病机制非常复杂,新的MOA治疗药物屡遭失败。IL17和IL13单克隆抗体治疗,以及有效地利用IL10来直接调节免疫反应均未能成功,尽管有令人信服的证据表明所有这些细胞因子是参与IBD的炎症反应的。
IBD异质性也非常大。很难有新的MOA可以覆盖大量患者群体。而且随着研究的深入,生物制剂和靶向药物增加,在IBD领域精准医疗的概念也已经提出。这意味着根据易感基因、治疗响应、动态监测等进一步对患者群体进行分层的时代即将来临。大“渔网”(适应人群广泛的药物)的出现将变得越来越困难。
临床试验终点目标和招募难度水涨船高
受到各种条件的限制,临床试验的设计和结果与最终的临床应用场景及预后之间总会存在或多或少的gap。弥补这一gap需要不断的优化试验设计或补充更多的临床试验。当前,IBD治疗正朝着更好的预后发展。这需要不断优化治疗的临床评价标准。相应地,药物临床试验的终点指标也水涨船高。
以UC为例,近些年的RCT临床试验设计中,内镜、组织学、生物标记物以及PROs(patient reported outcome,主要包括患者生存质量评分)作为关键疗效和安全性结果的比例正在提高。
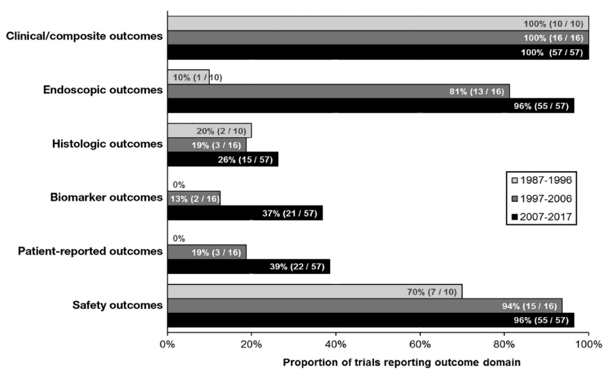
内镜和组织学检查容易因其介入性而在临床使用受限。因此,以非介入性生物标记物作为治疗目标受到了追捧。最近十年超过三分之一的RCTs报道了生物标记物的结果,主要集中在粪卫蛋白(FCP)和C反应蛋白。FCP是一种可靠的粘膜炎症生物标志物,并可预测维持治疗期间的响应丢失。然而,以生物标志物为终点的“达标治疗(treat-to-target)”方法是否能改善UC的深度缓解仍有待进一步确定。
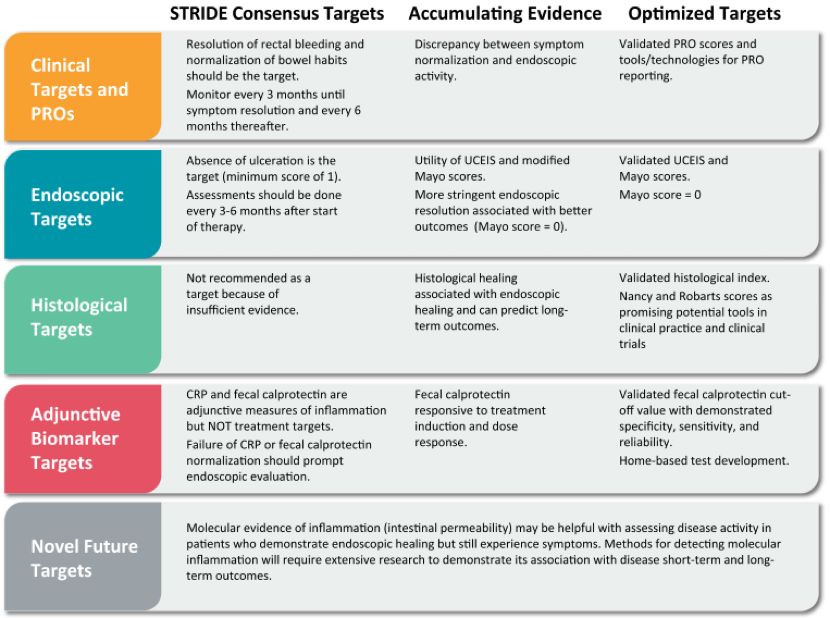
虽然目前内镜、组织学、生物标记物、无激素缓解等临床终点主要作为次要终点出现,而且其准确界定及对预后的意义仍需更大规模的前瞻性队列研究来证实,但“达标治疗”的趋势已不可逆转,2015年,STRIDE专家委员会确定了炎症性肠病(IBD)的“达标治疗”方案,将UC治疗的目标转变为预防长期疾病并发症(异形增生/癌变、住院治疗、结肠切除术),同时建议监测UC的客观疾病活动(如内镜炎症证据)。可以想象未来IBD治疗的临床终点中除了基本的临床缓解外,上述甚至更多的目标将日益被医生和FDA接受,成为预后和评价治疗药物的重要终点。
Informa的一项调查显示,自从IFX首次获批用于IBD适应症的20多年来(1998年以来),中重度UC每个临床中心的平均招募率为从0.32 降到0.13例/月,而中重度CD每个临床中心的平均招募率从0.65例降至0.0-0.10例/月(如下图所示)。1998年,总共有7次中重度IBD临床试验, 包括3个UC和4个CD;到2018年,已经增加到147个临床试验,包括84个UC和63个CD。这些趋势迫使制药公司不得不在全球范围内寻找可以参加IBD临床试验的中心。
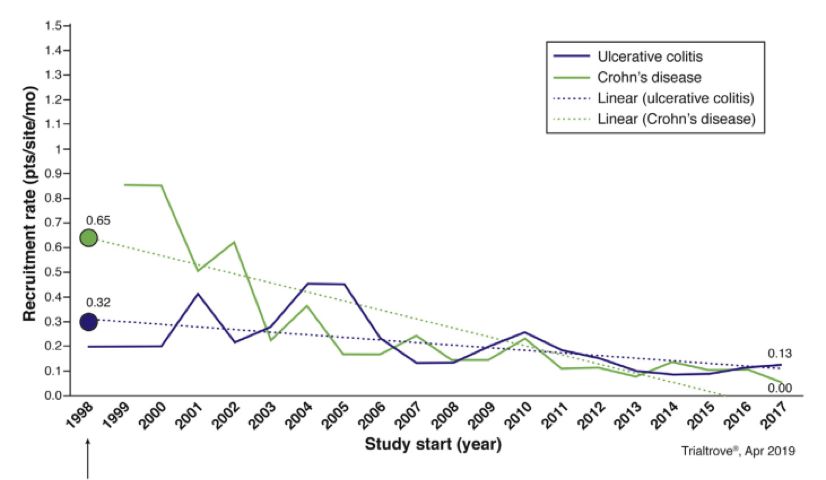
分析原因可能包括:在研药物数量的增加;相对于加入临床研究使用在研药物或安慰剂,其他的治疗选择明显增多;临床试验设计的复杂性增加;筛选患者失败率增加。
尤其第二点原因容易被忽略。新药的涌现增加了医生和患者的选择空间,但同时也降低了他们进入安慰剂对照研究的意愿,尤其是不提供长期扩展的二期试验。传统治疗失去响应的患者,一般会寻求新药,但在便宜、可及的生物类似药面前也有了更多的选择。生物制剂的大量应用也使得招募没有生物制剂治疗史的患者越来越困难。此外,试验流程中需要一定的洗脱期(通常5个半衰期),这对于超长半衰期的生物制剂来说,无疑会使患者长期暴露在无药控制或使用激素等其他药物的状态下,导致不少患者望而却步。
尽临床前评价模型转化效率低
动物模型是探索疾病发生机制,并为治疗效果提供概念验证的重要工具。然而,胃肠道系统中宿主遗传和环境因素独特的相互作用使建立IBD替代物种的模型非常具有挑战性。即使比较成熟的结肠炎模型也会受到重复性问题的困扰,这可能部分归因于不同实验室条件下微生物的差异。尽管如此,临床前动物模型仍然在为IBD病理生理机制及治疗评价研究“任劳任怨”地服务。
已经有多种IBD小鼠模型,从化学诱导的结肠炎模型到基因模型再到免疫改造或特殊菌群添加的模型。可是,至今没有一个模型能充分预测治疗的结果。每一种体内模型都有其适用性,稳健的科学研究关键仍然是谨慎地选择正确的模型来解决对应的科学问题,而不是将其直接转化为临床疗效。简单的右旋糖酐硫酸酯钠(DSS)诱导模型以及它所引起的损伤和炎症产生了大量科研论文,但却没有给患者带来直接的益处。例如,已经证明临床疗效的抗TNFα和抗IL-12/23p40抗体在化学诱导的结肠炎模型上是无效的。这可能是因为这些模型还只是短期的急性损伤而不是遗传易感人群发展多年的持续的疾病过程。而在其他模型,比如T细胞转移鼠(幼稚T细胞转移到Rag null或SCID突变小鼠),抗炎治疗却是非常有效的。
但是,即使小鼠对给定的治疗反应一致,但现实中却没有一种治疗方法能充分治疗所有IBD患者,这也表明需要多种模型来探索人类疾病的不同方面。理解哪些模型能充分代表人类疾病的不同方面是理解何时以及如何使用一种模型而不是另一种模型来解决与通路和治疗相关的适当机制问题的关键。
此外,具有显著且常常是严重免疫缺陷的遗传突变的小鼠让我们对IBD的免疫发病机制有了更深入的了解;然而,在这些小鼠身上的发现仅仅带来了少量的治疗方法,帮助了美国200多万以及全世界数百万IBD患者中的一小部分。最近的一个例子是IL -17抗体(Secukinumab)不仅不能对CD患者产生益处,而且还加重了一些患者的症状。动物模型研究发现,白细胞介素-23 (IL-23)促进肠道炎症的关键作用是通过IL-6和IL-17A等炎症介质实现的。与IL-17A在IBD中具有更为复杂的免疫调节作用相一致,其他动物模型的结果也提示IL-17A在IBD中具有保护作用。在活动性克罗恩病中发现12例粪便中IL-17A水平升高,同时克罗恩病患者固有层中分泌IL-23和IL-17A细胞数量增加。2006年,北美IBD遗传学协会在一项全基因组关联研究中首次报道IL-23R与克罗恩病易感性的强基因关联。后来,在独立地全基因组关联研究群组上这种联系的进一步证据被看到,提示IL-23-IL-17轴在疾病发病机制中的作用,并为IL-17A在克罗恩病中的作用提供间接证据。结果,在一项Secukinumab的2期临床试验中,第6周时,Secukinumab治疗未能将CDAI均值较安慰剂降低≥50分,错过了主要终点,并满足了IA中预先指定的无效标准。这项研究被提前终止,结果还表明,IL-17A的抑制可能对一组有炎症客观证据的患者产生不良结果。
另一个类似地例子,尽管对IL10 -/-小鼠发生的自发性结肠炎进行了大量研究,证明了这种抗炎性细胞因子在肠道炎症中的重要性,但21项针对IBD患者的IL-10治疗试验并没有显示出显著的有益效果。这可能是由于IL-10受体的多态性阻碍了这种治疗的有效性,或者是IL-10在体内的不稳定性和短半衰期。但无论如何,在人类IBD的阴性结果证实了动物数据外推到人类的不可预测性。
近来,在模型方面有两个最新进展,一是人源化小鼠模型的开发(人类免疫细胞嫁接到免疫缺陷小鼠),二是外植体的使用或直接从人类IBD患者肠道组织分离的固有层单核细胞(lamina propria mononuclear cells),他们可以让研究人员直接在人类细胞和/或组织上验证疗效,相信可以有效提高临床转化效率。
总结
结合上述IBD领域的趋势和我们对部分相关biotech公司的了解,我们认为biotech公司在IBD领域立项前应该思考如下几个问题:
一、IBD虽然有较多未满足的临床需求,但自己的产品定位是否属于真正的未满足的临床需求?如果是,这个需求有多大?比如:我们认为对于一个biotech公司,如果单纯改变给药途径面临的风险将较大,可能不足以支持其管线的商业价值。安全性和依从性甚至包括疗效的组合提升才是创业公司更好的选择。
二、IBD领域随着新药的涌现,市场放量会放缓甚至未被占据的市场份额都在萎缩,新产品尤其是发挥核心作用的新MOA产品的立项需要考虑这些变化,是否还有较大把握从现有“鱼塘”中捕获足够的“鱼”?相反,围绕核心地位产品的联合治疗(比如低毒的局部的粘膜或屏障修复或维持药物)或者围绕安全性或顺应性的深度挖掘是否可能另辟蹊径?
三、临床资源也在快速萎缩,是否有足够的能力、资金和时间来运作一个较大规模的临床研究?如何更巧妙的设计临床试验,以为上市后产品增加竞争力?
四、IBD领域临床前评价模型与临床结果之间关联性较弱,如何选择合适的临床前评价模型?对于新的MOA,如果能有临床上biomarker的指征,或全新的药物发现技术,将可能提高新产品的研发成功率。
未来最有价值的IBD新药将符合以下特征中的一个或几个:
1、全新机制,能够较大比例地解决现有药物无法诱导达到完全缓解的患者或者难治性/复发性患者。
2、解决现有药物的依从性和安全性等问题,扩大治疗窗。
3、诱导缓解并且能够达到“深度缓解”。
4、加速缓解或提高预后的辅助治疗或联合治疗。
参考
[1]AGA Clinical Practice Guidelines on the Management of Moderate to Severe Ulcerative Colitis. [Epub ahead of print] Gastroenterology. 2020 Jan 13. DOI: 10.1053/j.gastro.2020.01.006
[2]AGA Technical Review on the Management of Moderate to Severe Ulcerative Colitis. [Epub ahead of print]. Gastroenterology. 2020 Jan 13. doi: 10.1053/j.gastro.2020.01.007.
[3]The IBD Therapeutic Pipeline is Primed to Produce. PRACTICAL GASTROENTEROLOGY
[4]Genentech Research and Early Development (gRED).
https://www.roche.com/dam/jcr:46f31db2-73e5-4129-b1c4-e2d72233af5d/en/irp20200218.pdf
[5]Worldwide incidence and prevalence of inflammatory bowel disease in the 21st century: a systematic review of population-based studies. The Lancet, 390(10114), 2769–2778. doi:10.1016/s0140-6736(17)32448-0
[6]Discontinuation of Infliximab in Patients With Ulcerative Colitis Is Associated With Increased Risk of Relapse: A Multinational Retrospective Cohort Study. Clinical Gastroenterology and Hepatology, 14(10), 1426–1432.e1. doi:10.1016/j.cgh.2016.05.044
[7]IM-UNITI: 3 Year Efficacy, Safety, and Immunogenicity of Ustekinumab Treatment of Crohn's Disease. J Crohns Colitis 2019. doi:10.1093/ecco-jcc/jjz110
[8]The Present and Future of Inflammatory Bowel Disease Treatment.Gastroenterology & Hepatology Volume 12, Issue 7 July 2016
[9]Ustekinumab as Induction and Maintenance Therapy for CD. N Engl J Med 2016;375:1946-60. DOI: 10.1056/NEJMoa1602773.
[10]Ustekinumab as Induction and Maintenance Therapy for UC. N Engl J Med 2019;381:1201-14. DOI: 10.1056/NEJMoa1900750.
[11]Personalising medicine in inflammatory bowel disease—current and future perspectives. Transl Pediatr 2019;8(1):56-69. doi: 10.21037/tp.2018.12.03
[12]Heterogeneity in Definitions of Endpoints for Clinical Trials of Ulcerative Colitis: A Systematic Review for Development of a Core Outcome Set. Clinical Gastroenterology and Hepatology, 16(5), 637–647. doi:10.1016/j.cgh.2017.08.025
[13]Ulcerative Colitis: Clinical Trial Endpoints Guidance for Industry
[14]A Treat-to-Target Update in Ulcerative Colitis: A Systematic Review. Am J Gastroenterol 2019;114:874–883. https://doi.org/10.14309/ajg.0000000000000183
[15]Competition for clinical trails in IBD. Gastroenterology 2019;157:1457–1461. https://doi.org/10.1053/j.gastro.2019.08.020
[16]Challenges in IBD 2019. 2019 Crohn’s & Colitis Foundation

药事纵横是一个开放,由自愿者组成的团体,由以下成员组成:Voyager88,雷道安,Herman,梅希,文竹,duke,子炎,ZMJ和曾文亮。欢迎有志之士加入我们团队。投稿、合作、加专业群请加微信437180999,药事纵横二千人QQ群22711855



 个人中心
个人中心
 我是园区
我是园区




