▎药明康德内容团队报道
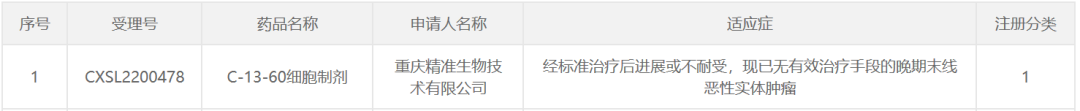
截图来源:CDE官网
精准生物成立于2016年,是由钱程教授为核心的技术团队与智飞生物联合创建的生物技术公司。该公司专注恶性肿瘤治疗,目前已建立10余项CAR-T产品研发管线,涵盖白血病、淋巴瘤、骨髓瘤、肠胃癌、肺癌、肝癌、乳腺癌、胰腺癌等适应症。
此次获批临床的C-13-60靶向一种名为CEA(carcinoembryonic antigen)的糖蛋白。该蛋白通常在癌胚胎的发展过程中表达,在非小细胞肺癌、结直肠癌、乳腺癌等癌细胞表面过度表达。值得注意的是,除低表达于肠上皮细胞外,CEA几乎不在其他正常细胞中表达。因此,它被认为是实体肿瘤极具治疗潜力的一个靶点。

根据精准生物早期发布的新闻稿,C-13-60来源于该公司研发的RESCAR和PHICAR技术平台,该平台可以促进CAR细胞向肿瘤部位聚集,克服肿瘤抑制免疫微环境以提高疗效,同时增强了在肿瘤环境中存活。临床前小鼠体内研究结果显示,C-13-60具有明显的有效性,有望帮助更多的直肠癌、胃癌和食管癌患者成功摆脱病痛。
参考资料:
[2]重庆精准生物申报的我国首个靶向CEA CAR-T产品获CDE受理. Retrieved Sep 23,2022,from https://mp.weixin.qq.com/s/hcN-O-8KPUmaDPMaXkDWjw

本文来自药明康德内容团队,欢迎个人转发至朋友圈,谢绝媒体或机构未经授权以任何形式转载至其他平台。转载授权请在「医药观澜」微信公众号留言联系我们。其他合作需求,请联系wuxi_media@wuxiapptec.com。
免责声明:药明康德内容团队专注介绍全球生物医药健康研究进展。本文仅作信息交流之目的,文中观点不代表药明康德立场,亦不代表药明康德支持或反对文中观点。本文也不是治疗方案推荐。如需获得治疗方案指导,请前往正规医院就诊。




 个人中心
个人中心
 我是园区
我是园区




