
责编 | 兮
2020年全球最新癌症数据指出,乳腺癌已超过肺癌,成为全球第一大癌症。三阴性乳腺癌 (TNBC) 因其表面雌激素受体、孕激素受体以及HER2均为阴性,故而对内分泌药物和HER2靶向药物不敏感。目前,手术和化疗是主要的治疗手段。同时,三阴性乳腺癌还具有侵袭性强、远程转移快和局部复发率高等特点,已经成为临床上最难以治疗的一种乳腺癌亚型。因此,深入探究三阴性乳腺癌的发生和发展过程,探寻新的治疗靶点和策略,提高三阴性乳腺癌患者生存率,改善生存质量,具有重要的临床应用价值和深远的社会意义。
表观遗传修饰已成为近年来肿瘤研究的前沿领域。目前,大量涉及表观遗传调控途径的小分子酶抑制剂或激活剂正被开发用于临床。然而,除了少数类型的实体瘤、T细胞淋巴瘤、上皮样肉瘤和难治性滤泡性淋巴瘤外,表观遗传学药物在晚期肿瘤中通常疗效不佳。越来越多的研究和临床数据表明,表观遗传药物和免疫治疗的联合疗法有望用于一系列实体癌患者。
2022年5月16日,中科院基础医学与肿瘤研究所吴芩团队与加拿大多伦多大学合作在Nature Chemical Biology上在线发表了题为PRMT inhibition triggers the viral mimicry response in Triple Negative Breast Cancer的研究论文,揭示了精氨酸甲基化转移酶调控内源免疫的新机制,为三阴性乳腺癌的免疫治疗提供了新的策略。

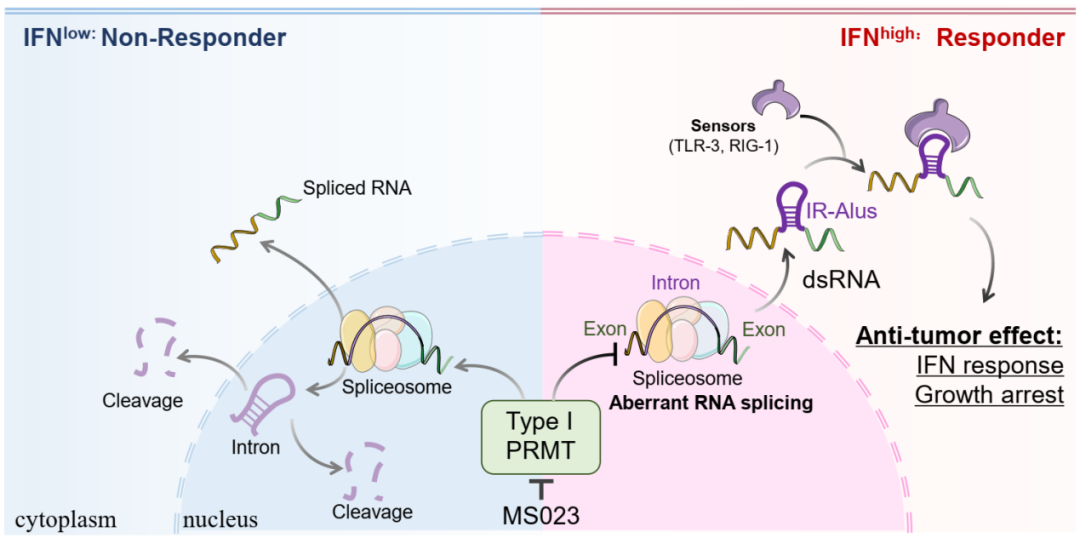
作者首先利用表观遗传小分子抑制剂对三阴性乳腺癌进行了系统筛选,鉴定出精氨酸甲基化转移酶可能是新的治疗靶点。并结合化学生物学、细胞生物学和生物信息学的方法对其作用机制进行了深入探讨,发现靶向精氨酸甲基化转移酶可调控细胞内的可变剪接,造成大量内含子滞留,滞留的内含子形成双链RNA激活下游的感受器,上调干扰素通路,从而引发内源性免疫反应,导致细胞死亡。该项研究揭示了揭示了精氨酸甲基化转移酶调控细胞内源性抗病毒免疫的新机制,为三阴性乳腺癌的治疗提供了新的靶点。
除此之外,该项研究还表明精氨酸甲基化转移酶的内源免疫调控功能仅限于部分三阴性乳腺癌细胞。这类细胞具有本底高表达干扰素通路的特征,抑制精氨酸甲基化转移酶通过激活上述的干扰素通路,使得此类本底干扰素通路上调的三阴性乳腺癌细胞超过承受阈值,导致细胞死亡。因此,本底干扰素通路的激活状态可作为生物标志物,预测精氨酸甲基化转移酶抑制剂的敏感性。总之,该项研究揭示了三阴性乳腺癌新的治疗靶点-精氨酸甲基化转移酶,并揭示了其调控细胞增殖和免疫的新机制,为三阴性乳腺癌的免疫治疗提供了新的策略。
值得一提的是,在同期Nature Chemical Biology还刊发了加拿大McGill University的Stéphane Richard的News & Views文章Putting introns on retainer对该篇文章进行了推介。
吴芩,中国科学院基础医学与肿瘤研究所谭蔚泓院士团队研究员。浙江省海外高层次人才,浙江省杰出青年基金获得者。主要从事化学分子探针与肿瘤精准治疗的研究。课题组致力于利用化学生物学、细胞生物学,分子生物学以及生物信息学等多学科交叉的方法鉴定乳腺癌治疗新靶点,绘制乳腺癌细胞的分子图谱,鉴定乳腺癌的免疫调控新机制,开发预测药物效果的生物标记物,实现乳腺癌的个性化精准治疗。研究成果以第一/通讯作者发表在Nature Chemical Biology、Nature Reviews Drug Discovery、Nature Communications、Chemical Science等期刊上。课题组长期招聘优秀博士后,待遇优厚。

原文链接:
https://www.nature.com/articles/s41589-022-01024-4
https://www.nature.com/articles/s41589-022-01025-3

转载须知
【非原创文章】本文著作权归文章作者所有,欢迎个人转发分享,未经作者的允许禁止转载,作者拥有所有法定权利,违者必究。




 个人中心
个人中心
 我是园区
我是园区




