 摘要:
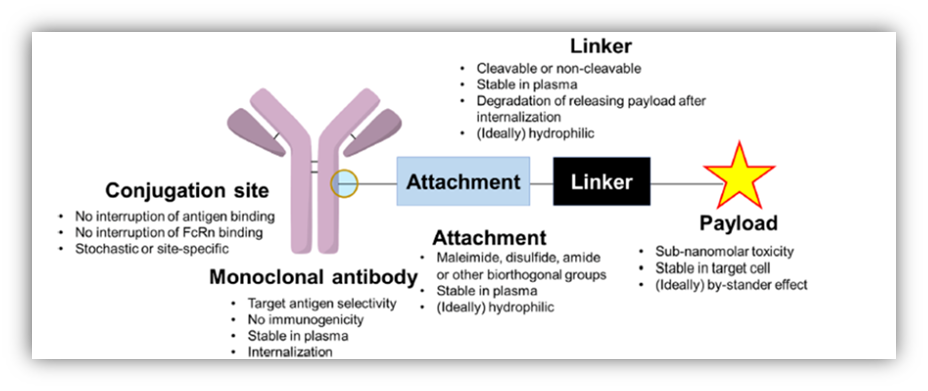
胃癌是一种难治性恶性肿瘤,发病率居世界第五,死亡率居世界第三。尽管各种治疗方案对改善晚期胃癌(AGC)的预后有很大作用,但生存期仍不理想。因此,开发新的治疗药物对改善长期疗效具有重要意义。抗体-药物偶联物(ADC)是一种创新和有效的抗肿瘤药物,由特异性靶向单克隆抗体、化学连接子和小分子细胞毒性载荷组成。
疗效强、毒性适中是其显著优势。但不可避免的是,该制剂存在耐药现象。本文系统综述了近年来
ADC药物在晚期胃癌治疗中的研究进展。
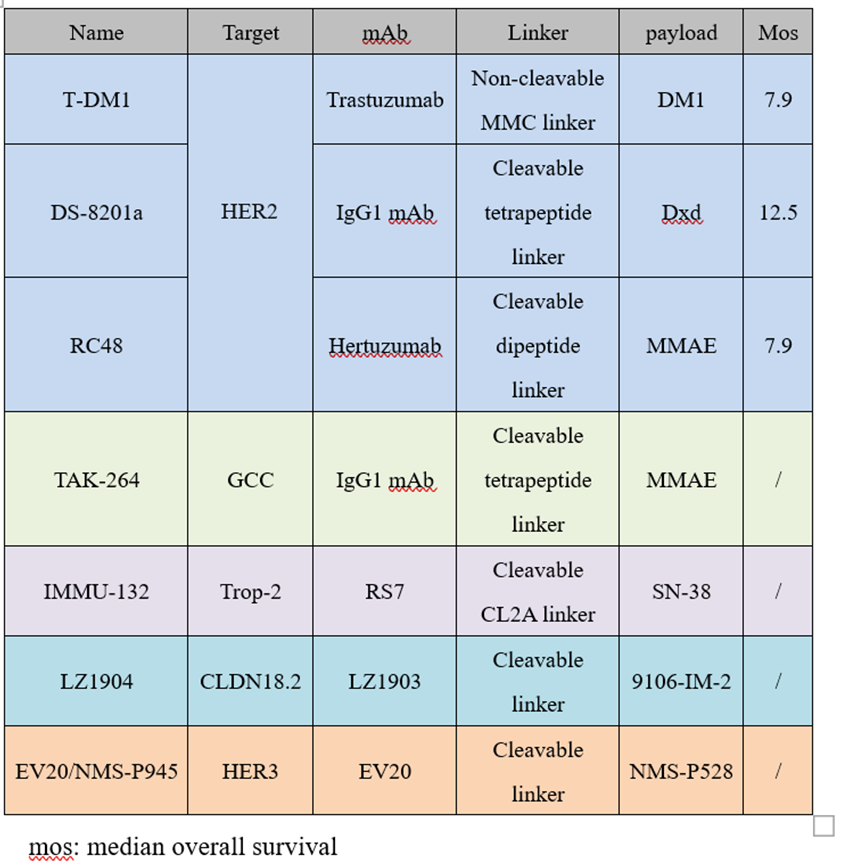
胃癌是一种常见的恶性肿瘤,一直严重威胁着人类的健康,并且大多数胃癌患者在确诊时已处于晚期,预后相对较差。与传统医学治疗相比,抗体偶联药物(ADC)具有较好的靶向性,显著的抗肿瘤能力和较低的全身毒性,近年来受到广泛关注。ADC类药物主要由人源化的单克隆抗体(包括:IgG1,IgG2以及IgG4,其中人源化的单克隆抗体可以有效降低ADC类药物的免疫原性,减小副作用)、稳定的连接子(Linker)(保证ADC药物结构的完整性,使得细胞毒性药物不会被提前释放,减少脱靶效应并且当ADC药物被内化之后,连接子能够迅速被切割,使得细胞毒性发挥作用)、高效小分子毒性药物。对于一款ADC类药物来说相应靶点的选择尤其重要,近年来基于HER2、GCC、TROP-2、CLDN18.2以及HER3五种靶点的ADC药物(表1)在胃癌晚期的治疗中展现出一定的疗效,本文你将基于此进行综述。
HER2
在胃癌以及胃管癌的过表达占到15-20%,因此有不少用于治疗胃癌晚期的ADC类药物使用HER2为目标靶点,具体包括T-DM1, DS-8201a,以及RC48。
T-DM1是由Trastuzumab(曲妥珠单抗)偶联DM1(微管抑制剂)靶向HER2的ADC类药物,DAR值为3.5,目前FDA已批准该药物用于乳腺癌晚期的治疗。结合II/III期临床数据来看,T-DM1
对HER2+的
胃癌晚期患者的中位生存期为7.9个月,临床应答率为20.6%,就安全性来看,T-DM1诱导三级不良反应率较低(26%贫血,11%血小板减少症)。总的来说,相比于其他治疗手段,T-DM1并不能使患者具有较好的获益,这可能是由于HER2+在胃癌晚期表达异质性造成的。
DS-8201a同样是靶向HER2的ADC类药物,该药物以可切割四肽Linker连接了毒性药物DXd, DAR值为7-8。该药物在低表达HER2+的胃癌患者上也展现出较好的疗效。在一项与化疗药物对照实验的结果表明,使用DS-8201a治疗的患者组(125名患者)有10名患者预后达到CR(完全缓解),而化疗组(62名患者)无达到CR级别。从患者生存期中位数来看,使用DS-8201治疗的患者的生存期(12.5个月)显著高于化疗组的8.4个月。表明DS-8201a是治疗胃癌晚期患者的有效药物,并且于2021年1月被FDA批准用于治疗HER2+的胃癌患者。
RC48是由赫妥珠单抗,通过可裂解双肽Linker连接微管抑制剂(MMAE)所组成的ADC药物,DAR值约为4。结合一项II期临床实验结果来看,RC48对低表达HER2+的胃癌患者有一定疗效,其中中位生存期达到7.9个月。从安全性的角度看,RC48主要不良反应为中性粒细胞减少症、白细胞减少症以及感觉减退症,并且不良反应率与剂量关系明显,结合该临床实验,2.5mg/kg的注入剂量具有较好的安全性。2021年6月RC48获得中国国家药监局有条件上市,用于胃癌晚期治疗。
GCC在调节肠液、离子分泌以及抑制细胞增殖方面出具有重要作用,一项相关的解破学研究表明,与正常组织相比,GCC在恶性肿瘤组织表面高度表达,因此GCC逐渐成为ADC药物的靶点。TAK-264是一种靶向GCC的ADC药物,它是由IgG单抗通过可切割四肽连接子偶联MMAE所获得的。前期动物模型表明TAK-264对高表达GCC模型具有初步杀伤结果。根据临床实验结果,TAK-264主要呈现的副作用有恶性(占41%)、食欲减退(41%)以及疲劳(32%)和腹泻(27%)。而三级不良反应中性粒细胞减少和低钾血症的发生率分别为22%以及7%,表明TAK-264具有较好耐受性。入组的41名患者中,1名患者获得部分缓解,3名患者病情稳定,所有患者中位无进展生存期(mPFS)为44天,该结果表明,TAK-264对胃癌晚期患者展现有限的疗效,但是由于GCC在胃癌中高度表达,因此该靶点对胃癌晚期治疗仍然展现出较大的潜力。
Trop-2又称肿瘤相关钙信号转导器2,具有致癌性,促进癌细胞增殖和转移的能力。目前56%Trop-2高表达的胃癌晚期患者,出现预后不良的情况。
IMMU-132是由RS7、有效载荷SN-38和可切割CL2A连接子组成,DAR为7.6,目前IMMU-132由FDA批准的第一种用于治疗转移性三阴性乳腺癌。此外,现有I/II临床实验初步结果表明IMMU-132,对晚期胃癌患者展现出一定的疗效,此外另一种靶向Trop-2的ADC药物SKB264,在胃癌晚期阳性动物模型中展现出较好的安全性以及有效性,表明Trop-2是治疗晚期胃癌的有效靶点。更多数据在进一步研究中。
CLDN18.2参与维持细胞间的紧密连接,影响细胞旁离子的通透性。其特异性亚型的特性使其成为胃癌治疗的潜在靶点。CLDN18.2的成分LZ1904在体外表现出明显的选择性抗肿瘤能力,值得在体内进一步研究。然而,CLDN18.2的临床试验还处于初级阶段。
胃癌患者中HER3过表达与预后不佳有关。以HER3为靶点的新型ADC EV20/NMS-P945由EV20;硫炔吲哚(TEI) NMS-P528,;和一个可分裂的连接剂组成。临床前研究发现EV20/NMS-P945对胃癌细胞和小鼠异种移植瘤模型具有良好的抗癌活性,这表明该制剂可能是对抗HER3表达的胃癌的有效工具。
综上所述,目前靶向HER2、GCC、TROP-2、CLDN18.2以及HER3五种靶点的ADC药物,展现出一定的疗效,是其开发是肿瘤治疗的重大突破,也是日后晚期胃癌治疗的关键。在未来,优化每个ADC组件,更好地理解潜在的修改,可以使ADC个性化和精确。ADC的研究和开发将进一步改善晚期胃癌患者的预后疗效。
摘要:
胃癌是一种难治性恶性肿瘤,发病率居世界第五,死亡率居世界第三。尽管各种治疗方案对改善晚期胃癌(AGC)的预后有很大作用,但生存期仍不理想。因此,开发新的治疗药物对改善长期疗效具有重要意义。抗体-药物偶联物(ADC)是一种创新和有效的抗肿瘤药物,由特异性靶向单克隆抗体、化学连接子和小分子细胞毒性载荷组成。
疗效强、毒性适中是其显著优势。但不可避免的是,该制剂存在耐药现象。本文系统综述了近年来
ADC药物在晚期胃癌治疗中的研究进展。
胃癌是一种常见的恶性肿瘤,一直严重威胁着人类的健康,并且大多数胃癌患者在确诊时已处于晚期,预后相对较差。与传统医学治疗相比,抗体偶联药物(ADC)具有较好的靶向性,显著的抗肿瘤能力和较低的全身毒性,近年来受到广泛关注。ADC类药物主要由人源化的单克隆抗体(包括:IgG1,IgG2以及IgG4,其中人源化的单克隆抗体可以有效降低ADC类药物的免疫原性,减小副作用)、稳定的连接子(Linker)(保证ADC药物结构的完整性,使得细胞毒性药物不会被提前释放,减少脱靶效应并且当ADC药物被内化之后,连接子能够迅速被切割,使得细胞毒性发挥作用)、高效小分子毒性药物。对于一款ADC类药物来说相应靶点的选择尤其重要,近年来基于HER2、GCC、TROP-2、CLDN18.2以及HER3五种靶点的ADC药物(表1)在胃癌晚期的治疗中展现出一定的疗效,本文你将基于此进行综述。
HER2
在胃癌以及胃管癌的过表达占到15-20%,因此有不少用于治疗胃癌晚期的ADC类药物使用HER2为目标靶点,具体包括T-DM1, DS-8201a,以及RC48。
T-DM1是由Trastuzumab(曲妥珠单抗)偶联DM1(微管抑制剂)靶向HER2的ADC类药物,DAR值为3.5,目前FDA已批准该药物用于乳腺癌晚期的治疗。结合II/III期临床数据来看,T-DM1
对HER2+的
胃癌晚期患者的中位生存期为7.9个月,临床应答率为20.6%,就安全性来看,T-DM1诱导三级不良反应率较低(26%贫血,11%血小板减少症)。总的来说,相比于其他治疗手段,T-DM1并不能使患者具有较好的获益,这可能是由于HER2+在胃癌晚期表达异质性造成的。
DS-8201a同样是靶向HER2的ADC类药物,该药物以可切割四肽Linker连接了毒性药物DXd, DAR值为7-8。该药物在低表达HER2+的胃癌患者上也展现出较好的疗效。在一项与化疗药物对照实验的结果表明,使用DS-8201a治疗的患者组(125名患者)有10名患者预后达到CR(完全缓解),而化疗组(62名患者)无达到CR级别。从患者生存期中位数来看,使用DS-8201治疗的患者的生存期(12.5个月)显著高于化疗组的8.4个月。表明DS-8201a是治疗胃癌晚期患者的有效药物,并且于2021年1月被FDA批准用于治疗HER2+的胃癌患者。
RC48是由赫妥珠单抗,通过可裂解双肽Linker连接微管抑制剂(MMAE)所组成的ADC药物,DAR值约为4。结合一项II期临床实验结果来看,RC48对低表达HER2+的胃癌患者有一定疗效,其中中位生存期达到7.9个月。从安全性的角度看,RC48主要不良反应为中性粒细胞减少症、白细胞减少症以及感觉减退症,并且不良反应率与剂量关系明显,结合该临床实验,2.5mg/kg的注入剂量具有较好的安全性。2021年6月RC48获得中国国家药监局有条件上市,用于胃癌晚期治疗。
GCC在调节肠液、离子分泌以及抑制细胞增殖方面出具有重要作用,一项相关的解破学研究表明,与正常组织相比,GCC在恶性肿瘤组织表面高度表达,因此GCC逐渐成为ADC药物的靶点。TAK-264是一种靶向GCC的ADC药物,它是由IgG单抗通过可切割四肽连接子偶联MMAE所获得的。前期动物模型表明TAK-264对高表达GCC模型具有初步杀伤结果。根据临床实验结果,TAK-264主要呈现的副作用有恶性(占41%)、食欲减退(41%)以及疲劳(32%)和腹泻(27%)。而三级不良反应中性粒细胞减少和低钾血症的发生率分别为22%以及7%,表明TAK-264具有较好耐受性。入组的41名患者中,1名患者获得部分缓解,3名患者病情稳定,所有患者中位无进展生存期(mPFS)为44天,该结果表明,TAK-264对胃癌晚期患者展现有限的疗效,但是由于GCC在胃癌中高度表达,因此该靶点对胃癌晚期治疗仍然展现出较大的潜力。
Trop-2又称肿瘤相关钙信号转导器2,具有致癌性,促进癌细胞增殖和转移的能力。目前56%Trop-2高表达的胃癌晚期患者,出现预后不良的情况。
IMMU-132是由RS7、有效载荷SN-38和可切割CL2A连接子组成,DAR为7.6,目前IMMU-132由FDA批准的第一种用于治疗转移性三阴性乳腺癌。此外,现有I/II临床实验初步结果表明IMMU-132,对晚期胃癌患者展现出一定的疗效,此外另一种靶向Trop-2的ADC药物SKB264,在胃癌晚期阳性动物模型中展现出较好的安全性以及有效性,表明Trop-2是治疗晚期胃癌的有效靶点。更多数据在进一步研究中。
CLDN18.2参与维持细胞间的紧密连接,影响细胞旁离子的通透性。其特异性亚型的特性使其成为胃癌治疗的潜在靶点。CLDN18.2的成分LZ1904在体外表现出明显的选择性抗肿瘤能力,值得在体内进一步研究。然而,CLDN18.2的临床试验还处于初级阶段。
胃癌患者中HER3过表达与预后不佳有关。以HER3为靶点的新型ADC EV20/NMS-P945由EV20;硫炔吲哚(TEI) NMS-P528,;和一个可分裂的连接剂组成。临床前研究发现EV20/NMS-P945对胃癌细胞和小鼠异种移植瘤模型具有良好的抗癌活性,这表明该制剂可能是对抗HER3表达的胃癌的有效工具。
综上所述,目前靶向HER2、GCC、TROP-2、CLDN18.2以及HER3五种靶点的ADC药物,展现出一定的疗效,是其开发是肿瘤治疗的重大突破,也是日后晚期胃癌治疗的关键。在未来,优化每个ADC组件,更好地理解潜在的修改,可以使ADC个性化和精确。ADC的研究和开发将进一步改善晚期胃癌患者的预后疗效。
参考文献
[1] Wang N, Mei Q, Wang Z, Zhao L,Zhang D, Liao D, Zuo J, Xie H, Jia Y and Kong F (2022) Research Progress of Antibody–Drug Conjugate Therapy for Advanced Gastric Cancer.Front. Oncol. 12:889017.doi: 10.3389/fonc.2022.889017
[2] Shitara K , e t a l .Trastuzumab Deruxtecan (DS-8201a) in Patients With Advanced HER2- Positive Gastric Cancer: A Dose-Expansion, Phase 1 Study. Lancet Oncol (2019) 20:827–36. doi: 10.1016/S1470-2045(19)30088-9.
 摘要:
胃癌是一种难治性恶性肿瘤,发病率居世界第五,死亡率居世界第三。尽管各种治疗方案对改善晚期胃癌(AGC)的预后有很大作用,但生存期仍不理想。因此,开发新的治疗药物对改善长期疗效具有重要意义。抗体-药物偶联物(ADC)是一种创新和有效的抗肿瘤药物,由特异性靶向单克隆抗体、化学连接子和小分子细胞毒性载荷组成。
疗效强、毒性适中是其显著优势。但不可避免的是,该制剂存在耐药现象。本文系统综述了近年来
ADC药物在晚期胃癌治疗中的研究进展。
摘要:
胃癌是一种难治性恶性肿瘤,发病率居世界第五,死亡率居世界第三。尽管各种治疗方案对改善晚期胃癌(AGC)的预后有很大作用,但生存期仍不理想。因此,开发新的治疗药物对改善长期疗效具有重要意义。抗体-药物偶联物(ADC)是一种创新和有效的抗肿瘤药物,由特异性靶向单克隆抗体、化学连接子和小分子细胞毒性载荷组成。
疗效强、毒性适中是其显著优势。但不可避免的是,该制剂存在耐药现象。本文系统综述了近年来
ADC药物在晚期胃癌治疗中的研究进展。




 个人中心
个人中心
 我是园区
我是园区




