▎药明康德内容团队报道
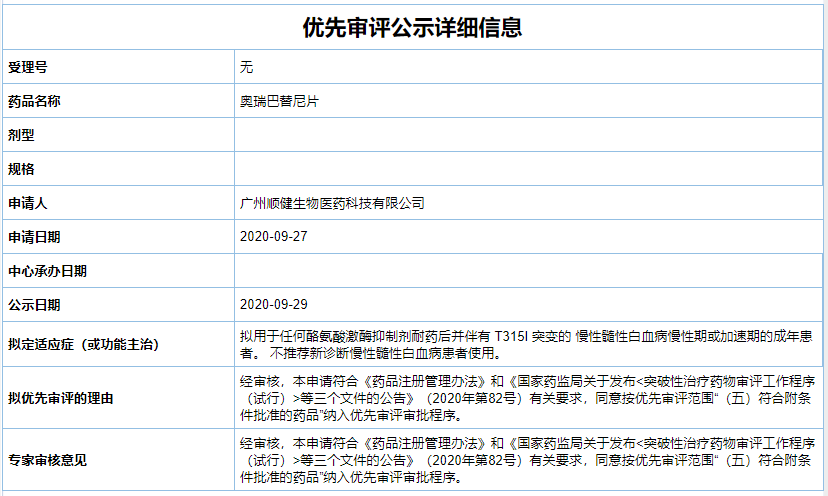
10月21日,亚盛医药宣布,该公司全资子公司顺健生物的1类新药奥瑞巴替尼片(HQP1351的拟定中文通用名)已正式被中国家药品监督管理局新药审评中心(CDE)纳入优先审评。
奥瑞巴替尼是一种第三代BCR-ABL抑制剂
,本次以“符合附条件批准的药品”被纳入优先审评,适应症为慢性髓性白血病(CML)患者。
值得一提的是,根据新闻稿,该药被纳入优先审评不仅意味着奥瑞巴替尼有望成为中国大陆地区首个上市的第三代BCR-ABL抑制剂,还意味着亚盛医药将迎来首款获批上市的新药。
CML是一种与白细胞有关的恶性肿瘤。尽管第一代BCR-ABL抑制剂及后续推出的几种二代药物对CML的治疗具有显著的临床效益,但获得性耐药一直是CML治疗的主要挑战。BCR-ABL激酶区突变是获得性耐药的重要机制之一,其中T315I突变是常见的耐药突变类型之一,在耐药CML中的发生率高达25%左右。伴有T315I突变的CML患者对目前的第一代、第二代BCR-ABL抑制剂均耐药,因此临床上急需有效的新一代治疗药物。
奥瑞巴替尼是亚盛医药开发的一款口服第三代BCR-ABL抑制剂,是亚盛医药的核心品种。该产品对BCR-ABL以及包括T315I突变在内的多种BCR-ABL突变体有突出效果,用于治疗对第一代、第二代TKI耐药的CML患者。今年6月,亚盛医药根据两项关键性2期临床研究结果向NMPA递交了奥瑞巴替尼的新药上市申请,值得一提的是,这也是亚盛医药创立以来的第一个新药上市申请。
CDE官网显示,奥瑞巴替尼以“符合附条件批准的药品”被纳入优先审评,申请的适应症为——拟用于任何酪氨酸激酶抑制剂耐药后并伴有T315I突变的慢性髓性白血病慢性期或加速期的成年患者。根据新闻稿,奥瑞巴替尼有望成为中国首个用于治疗耐药CML的后续第三代BCR-ABL靶向药。
亚盛医药首席医学官翟一帆博士表示:“奥瑞巴替尼是公司的第一个申请新药上市的品种,也将成为中国首个上市的第三代BCR-ABL抑制剂。奥瑞巴替尼正式被纳入优先审评品种,意味着其审批速度有望加快,将加速改变对现有TKI药物治疗无效的CML患者尚无药可医的局面。我们期待尽早将奥瑞巴替尼推向上市,造福更多患者。”
目前,亚盛医药正在全球范围内对奥瑞巴替尼进行开发。2019年7月,该品种获美国FDA临床试验许可,直接进入1b期临床研究。2020年5月,奥瑞巴替尼先后获得美国FDA授予的孤儿药资格和快速通道资格,用于治疗对现有TKI治疗失败的特定基因突变的CML患者。
祝贺亚盛医药第三代BCR-ABL抑制剂奥瑞巴替尼被纳入优先审评,希望该药早日获批,为CML患者带来新的治疗选择。
声明:本文由药明康德内容团队根据公开资料整理编辑,欢迎个人转发至朋友圈,谢绝媒体或机构未经授权以任何形式转发/复制至其他平台。转发授权请在「医药观澜」微信公众号留言联系我们。
欢迎扫码关注“
医药观澜
”微信公众号,了解更多中国医药创新动态。

注:本文旨在介绍医药健康研究进展,不是治疗方案推荐。如需获得治疗方案指导,请前往正规医院就诊。





 药选址
药选址


