临床试验
取得突破性进展,美国明尼苏达大学医学院神经外科Wei Zhang等人在Expert Opinion on BiologicalTherapy发表文章,文章回顾了临床前和临床数据,证明基于OV的联合疗法与FDA批准的抗癌药物的原理和潜在疗效。专家们认为,虽然OV的细胞溶解活性仍然是其抗肿瘤作用的关键驱动力,但了解病毒与宿主的相互作用可能为与FDA批准的针对这些相互作用的治疗方法的潜在协同作用提供机会。最有趣的是,OVs的免疫刺激作用使得与FDA批准的免疫疗法的结合更加有效。虽然有越来越多的临床试验采用这种联合治疗,但是需要提高对病毒-宿主相互作用的理解以利于取得更多有意义的进展。
溶瘤病毒(OVs)被设计成在癌细胞中选择性复制。虽然最初认为通过直接细胞溶解发挥其抗癌作用,但人们越来越认识到OVs在其生命周期中与多种细胞过程相互作用;FDA批准的调节这些细胞过程的药物已被证明可增强OVs的抗肿瘤作用。此外,由于肿瘤抗原的释放以及病毒固有的免疫刺激性,OVs可诱导有效的免疫反应,增强FDA批准的免疫疗法的抗肿瘤作用。在这种背景下,OV作为联合抗癌治疗平台的兴趣与日俱增。
•溶瘤病毒(OV)在其生命周期中与多种细胞途径相互作用,包括DNA修复和有丝分裂。
•FDA批准的针对OV调节细胞途径的药物制剂增强或协同OV的抗癌作用。
•除了直接溶解癌细胞外,OV还能诱导有效的免疫反应,增强FDA批准的免疫疗法的抗肿瘤效果。
•OVs作为一个合理设计多方案抗癌治疗的平台,临床上的兴趣正在上升
溶瘤病毒(OV)的发展建立在早在一个世纪前的观察基础上,当时癌症在自然获得的病毒感染后自然消退。虽然最初的努力旨在利用含有病毒的体液来传播这种治疗性感染,但随后的研究表明,天然的病毒趋化性在临床转化中造成了很大的限制。有了这一认识,基因工程的出现导致了许多对不同癌症具有明确选择性的病毒的产生。几乎所有种类的病毒,包括单纯疱疹病毒,腺病毒,痘苗病毒,麻疹病毒,细小病毒,脊髓灰质炎病毒,马拉巴病毒,呼肠孤病毒,柯萨奇病毒、水泡性口炎病毒、新城疫病毒和小核糖核酸病毒都是在这种背景下进行工程设计的,并在临床上对不同类型的肿瘤进行了测试(见表1)。该工程通常需要突变一些与病毒复制有关的关键基因,从而大大削弱了宿主细胞的杀伤能力,同时赋予病毒对肿瘤的选择性。
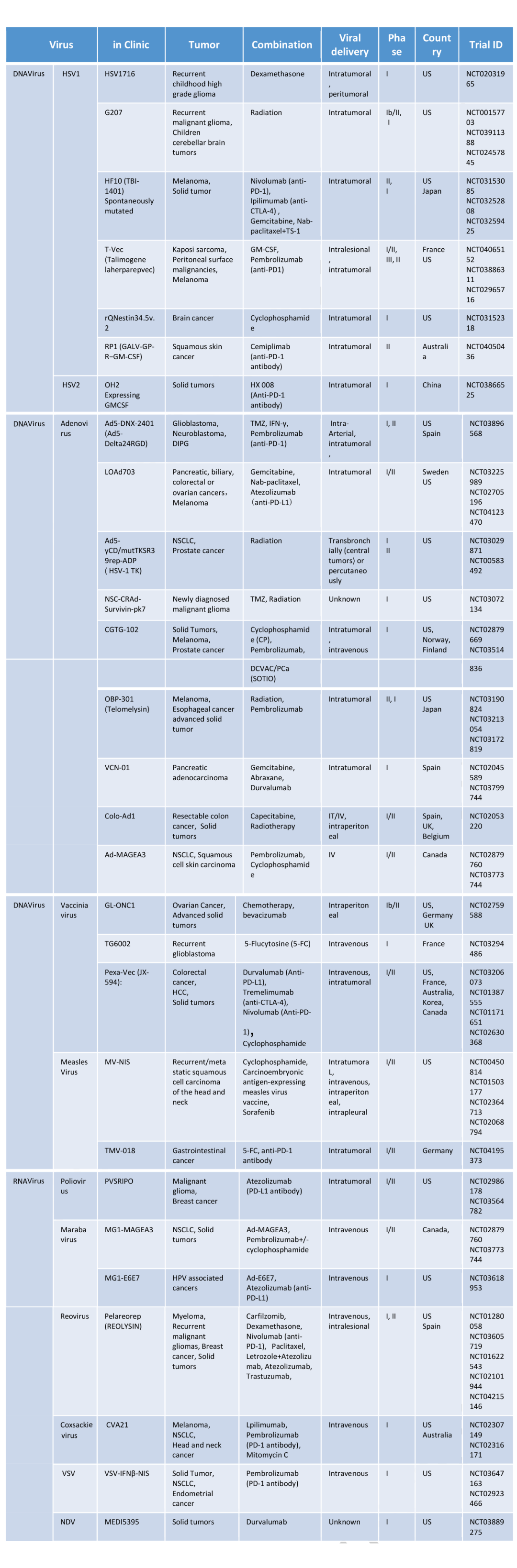
最值得注意的是,2015年获得FDA批准作为抗癌治疗的第一个OV是溶瘤疱疹病毒。这一批准激起了人们对OVs作为抗癌治疗平台的兴趣。尽管在随后具有里程碑意义的I/II期临床试验中观察到了抗肿瘤信号,但肿瘤复发几乎是普遍的。随着对大多数实体癌内在的瘤内和瘤间异质性认识的提高,已经提出了一个假说,即OV的最佳治疗效果可能需要合理的组合。新出现的数据表明,OVs在其生命周期中与多种细胞过程相结合,FDA批准的调节这些细胞过程的药物可以释放OVs真正的治疗潜力。鉴于免疫治疗在某些癌症中取得了显著的成功,并且观察到OVs能有效地刺激抗肿瘤免疫反应,OVs与FDA批准的免疫检查点抑制剂的联合已经成为中心。在这篇综述中,我们将提供一个关于OVs与FDA批准的各种药物组合的知识的当前状态的概述。
化疗是利用化学物质作为细胞内毒物,抑制DNA合成、有丝分裂和细胞分裂,引起DNA损伤的主要癌症治疗方法之一。在病毒复制过程中,这些细胞途径会受到病毒的干扰。替莫唑胺(TMZ)是一种烷基化剂,是治疗各种实体瘤,包括胶质瘤和黑色素瘤的有效抗癌药物。TMZ通过溶瘤性单纯疱疹病毒、腺病毒、新城疫病毒和粘液瘤病毒在杀死胶质母细胞瘤、肺癌、黑色素瘤和乳腺癌方面显示出更好的抗肿瘤效果。
溶瘤腺病毒(OAd)联合TMZ在体外和体内对肺癌细胞的治疗效果进行了评估。TMZ通过增加病毒在肺癌细胞而非其它正常细胞中的复制来增强OAd Adhz60的病毒疗法。这些研究表明,了解病毒与宿主的相互作用对于开发与OV等抗肿瘤药物的联合治疗药物具有重要意义。
溶瘤病毒与癌症的特定基因、蛋白质或组织环境相互作用,这些基因、蛋白质或组织环境在感染、复制和从癌细胞释放过程中有助于癌症的生长和生存。这使得OVs与靶向治疗协同工作成为可能,靶向治疗通过干扰致癌和肿瘤生长所需的特定分子来阻断肿瘤生长。索拉非尼是一种靶向抗癌药物,是一种酪氨酸激酶抑制剂,可抑制多种蛋白激酶,包括VEGFR、PDGFR和RAF激酶。Heo等人证明了溶瘤痘病毒JX-594与索拉非尼序贯联合治疗肝细胞癌(HCC)的临床前和临床疗效。JX-594,也称为Pexa-Vec(pexastimogene devacirepvec),是一种病毒胸苷激酶(TK)基因缺失、人粒细胞巨噬细胞集落刺激因子(hGM-CSF)和β-半乳糖苷酶转基因表达的武装免疫治疗性痘苗病毒。在两种小鼠肝癌模型中,JX-594与索拉非尼序贯联合治疗可提高抗肿瘤疗效。他们进一步进行了一项初步临床研究,探讨JX-594联合索拉非尼治疗3例肝癌患者的安全性和有效性。研究表明,序贯治疗具有良好的耐受性,并与肿瘤灌注显著降低相关,所有患者的客观肿瘤反应也显著降低。这是一个很好的例子,说明在设计联合疗法时,考虑药物是否会抵消OVs的疗效是很重要的,并考虑序贯联合以尽量减少抵消作用。
激素疗法以激素信号通路为靶点抑制癌细胞的生长需要荷尔蒙才能生长。早期的研究表明雌激素β-雌二醇增加了雌激素受体阳性(ER+)人乳腺中溶瘤HSV-1nv1066的复制癌症。雌激素增强了NV1066的溶瘤作用,对肿瘤细胞的杀伤率分别为95%和97%,在MOIs为0.1和0.5时,相比之下,无雌激素时分别为53%和87%。这个增强的病毒溶瘤作用与雌激素增加细胞增殖和凋亡有关减少ER+乳腺癌细胞的凋亡。到目前为止,还没有太多关于OV与经批准的激素治疗药物相结合的报道。
免疫治疗是一种以免疫检查点抑制剂为代表的激活或抑制免疫系统的免疫治疗,已成功应用于各种癌症,包括黑色素瘤、肺癌和膀胱癌。自2011年FDA批准首个检查点抑制剂ipilimumab(CTLA-4抗体)用于黑色素瘤以来,在2014年和2018年,FDA又批准了三种PD-1(Nivolumab、Pembrolizumab和Cemiplimab)和三种PD-L1(Atezolizumab,Avelumab和 Durvalumab)检查点抑制剂。OV作为免疫治疗的一种亚型,在临床前和临床研究中被广泛地与检查点抑制剂相结合。OV感染可刺激抗肿瘤免疫反应,并将对检查点阻断无反应的“冷”肿瘤微环境转变为具有激活和增加免疫细胞的检查点阻断反应的“热”环境,这增强了检查点抑制的功效。
一种编码白细胞介素7(IL-7)和IL-12的溶瘤痘苗病毒在黑色素瘤、结肠癌和肺癌模型等多种肿瘤模型中诱导了长期生存效益。将该病毒与抗PD-1或抗CTLA4抗体结合,进一步提高了抗肿瘤活性与单次治疗相比的活性。此外,单独或联合免疫检查点阻断的病毒通过免疫状态的改变在远处无创伤肿瘤中显示出抗肿瘤活性。在携带人类癌细胞的人源化小鼠中也观察到了这种现象。在许多癌症治疗中,附加的OVs和免疫检查点抑制剂包括oHSV、腺病毒和麻疹病毒。
6. OVs与FDA批准的抗肿瘤药物联合应用的临床试验
由于临床前研究证明了OVs与其他方式相结合的有效性,OVs联合治疗已广泛应用于不同类型的癌症治疗。一项1b期试验研究了溶瘤呼肠孤病毒Pelareorep联合抗PD1抗体Pembrolizumab免疫治疗和5-氟尿嘧啶、吉西他滨或伊立替康化疗的安全性和有效性。在10个疗效可评估的患者中,有3个观察到疾病控制,一个部分缓解17.4个月,另两个病情稳定超过9个月和4个月,而治疗耐受性良好。在治疗中的肿瘤活检中观察到病毒复制。通过分析外周血的T细胞受体测序,发现治疗期间出现了新的T细胞克隆,并观察了临床受益患者免疫基因表达的变化。本试验证明,Pelareorep和pembrolizumab联合化疗并没有引起明显的毒性反应,显示出令人鼓舞的疗效。除了免疫检查点抑制剂外,临床试验正在测试OVs和细胞因子(如IFN-γ)的联合免疫治疗,以增强整体抗肿瘤免疫反应或OVs与免疫抑制剂(如环磷酰胺)联合以保护OV在肿瘤中的活性。此外,临床试验报告了在晚期恶性肿瘤患者中联合使用溶瘤疫苗病毒、呼肠孤病毒、单纯疱疹病毒或腺病毒进行化疗的抗肿瘤效果令人鼓舞。
在过去的二十年中,基因工程通过产生更多的潜在致病性病毒用于癌症治疗,加速了卵母细胞的快速扩张。2015年,美国FDA批准T-VEC作为黑色素瘤免疫治疗的单剂,这是病毒治疗领域的一个转折点。随着OV的持续发展,研究者对其作用机制有了更清晰的认识。卵母细胞不仅由于病毒复制而溶解肿瘤细胞,而且改变肿瘤局部的免疫微环境。在过去几年中,检查点免疫疗法改变了癌症治疗的格局,改变了许多癌症的治疗标准,如黑色素瘤。
因此,在临床前和临床研究中,抑制剂被积极地用于癌症治疗。例如,TalimogeneLaherparepvec联合抗PD-1抗体pembrolizumab的III期试验正在进行中;用于黑色素瘤患者的试验(NCT02263508);OV与其他疗法的显著组合包括:II期试验腺病毒LOAd703加化疗吉西他滨和紫杉醇治疗胰腺癌(NCT02705196);痘苗病毒GL-ONC1加化疗和贝伐单抗,联合治疗卵巢癌患者等。
虽然许多令人兴奋的临床前和临床研究表明OV具有很强的潜力,但其疗效不理想表明了其在临床试验中的局限性。最近的研究表明,大范围小细胞肺癌患者在铂化疗后,没有受益于溶瘤的皮卡病毒NTX-010的治疗。以疫苗病毒为基础的溶瘤免疫治疗对晚期肝癌患者索拉非尼失败后作为二线治疗的整体生存率(OS)没有提高。溶瘤野生型呼肠孤病毒pelareorep与FOLFOX6/Bevacizumab的联合应用是可耐受的,客观反应率(ORR)增加,但无进展生存率(PFS)较低。这些临床局限性很可能是由于病毒的传递和传播、耐药性和抗病毒免疫反应的影响。
免疫系统是病毒治疗的双刃剑。一方面,要成功复制病毒并在肿瘤内传播,抗病毒免疫反应必须最小化。另一方面,抗肿瘤反应必须在最大限度的刺激。后者既需要调节先天免疫反应,也需要激活免疫抑制肿瘤微环境。为了提高抗肿瘤的疗效,人们一直致力于培育新的OVs,以增强宿主免疫应答的刺激或保护OV免受免疫清除。
OVs在其生命周期中靶向癌细胞或肿瘤微环境中的多个分子或信号通路,这为针对这些细胞通路抗肿瘤药物结合OVs提供了机会。OVs在癌细胞中的感染和复制直接导致细胞死亡,并引发宿主抗肿瘤免疫反应,进一步消灭癌细胞。这是OVs与FDA批准的不同免疫疗法相结合的基础,在许多癌症中显示出良好的联合疗效。OVs作为一种与其他抗癌药物联合治疗的平台,越来越受到临床的关注。随着OVs发展的步伐越来越快,我们从目前的临床试验中了解到了OVs的优点和缺点。在今后的研究中,深入了解OV与肿瘤的相互作用,包括病毒-肿瘤细胞和病毒-肿瘤微环境,以期开发出更有效的OV,在逃避免疫应答的同时激活OV,并根据特定的机制与不同的抗肿瘤试剂进行组合。
六大板块聚焦行业热点
行业大咖纵论产业前沿
千人汇聚共襄科技盛举
时间:2021年6月19-20日
地点:上海(具体地点报名后通知)
规模:800人
主办单位:四叶草会展
支持单位:生物制品圈、陆道培医疗集团
会议费用:为生物医药技术研发人员提供参会福利,5月20日之前报名FREE!(仅收取100元定金,含茶歇、会议资料等,定金概不退还),先到先得,报完即止,5月20日以后报名将收取会议费!
报名方式:扫描下方二维码或点击文章最底部“阅读原文”→ 填写表格 → 报名成功!

如需赞助,扫码登记即可!
组委会获得报名信息后,根据报名信息进行初筛,并进一步与报名者沟通确认,实现精准邀请。最终有机会进入大会微信群(严格审核通过)。

识别微信二维码,添加生物制品圈小编,符合条件者即可加入生物制品微信群!

本公众号所有转载文章系出于传递更多信息之目的,且明确注明来源和作者,不希望被转载的媒体或个人可与我们联系(cbplib@163.com),我们将立即进行删除处理。所有文章仅代表作者观点,不代表本站立场。











 药选址
药选址








