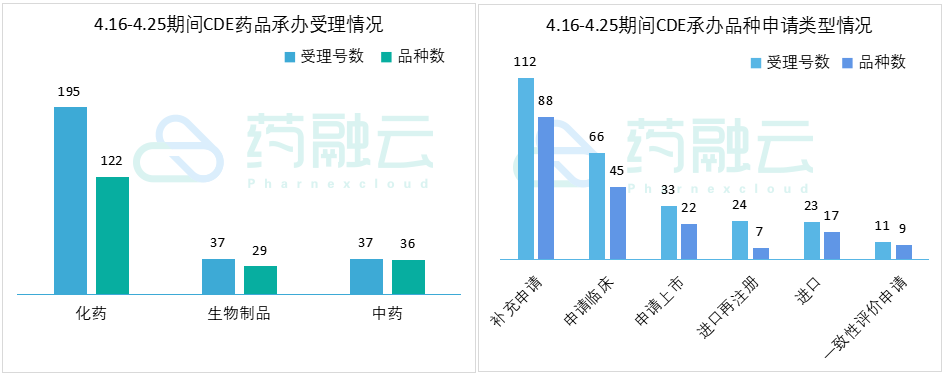
2021.04.16-2021.04.25期间药审中心受理总量为269个,涉及品种187个。
30个1类新药申请临床获CDE受理。
新增11个按仿制药质量和疗效一致性评价品种申报的受理号。
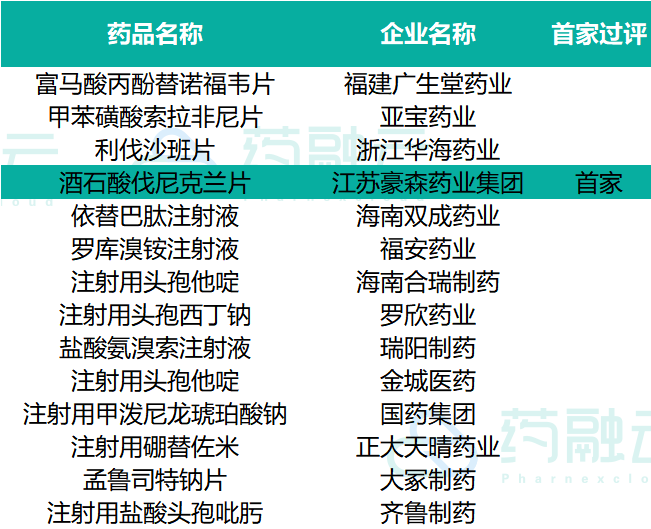
13个品种通过(含视同通过)一致性评价。
1款国产新药申请上市:复宏汉霖不限癌种PD-1申报上市

2个品种批准进口

过评品种信息
根据药融云中国药品审评数据,4月16号-4月25号期间共187个(按品种计,下同)药品获CDE承办,包括化药122个,生物制品29个,以及中药36个。
下表为2021.04.16-2021.04.25申请上市的药物情况。

近日,复宏汉霖创新型PD-1抑制剂斯鲁利单抗注射液(HLX10)上市申请获CDE受理。本品由复宏汉霖自主开发,是国内首款申请上市的MSI-H实体瘤PD-1疗法,适应症为经标准治疗失败的、不可切除或转移性高度微卫星不稳定型(Microsatellite Instability-High, MSI-H)实体瘤。该适应症依据特定的MSI-H肿瘤标志物进行筛查,不以癌种进行区分,覆盖患者群体广泛。围绕斯鲁利单抗,公司采取了“Combo+Global”(联合治疗+国际化)的差异化开发战略,在适应症选择和联合治疗上重点发力,已于全球范围内同步开展10项临床试验。

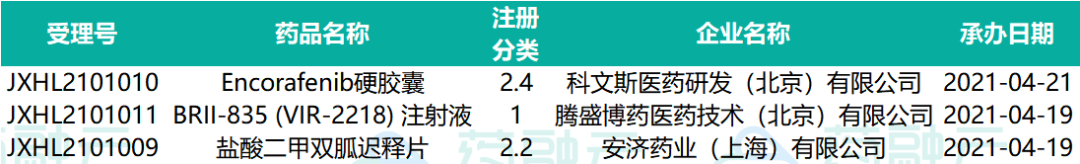
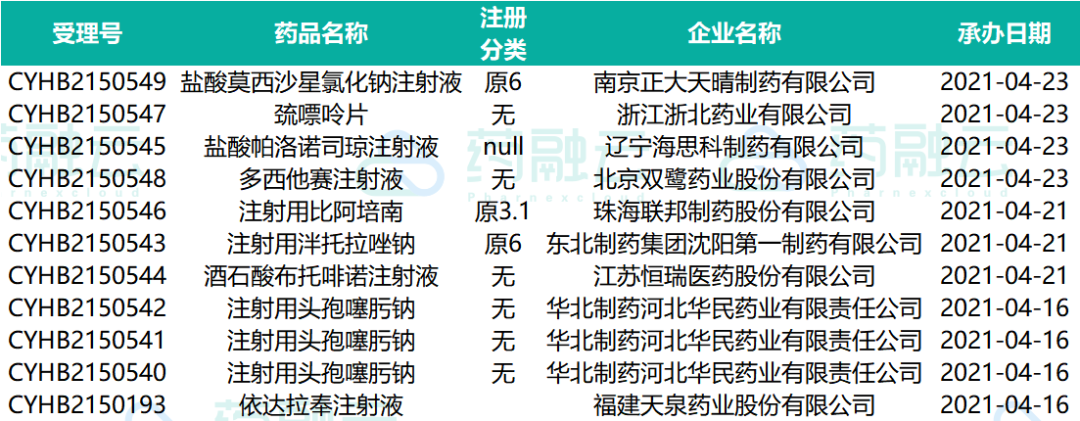
下表为2021.04.16-2021.04.25申请临床的进口药物情况。
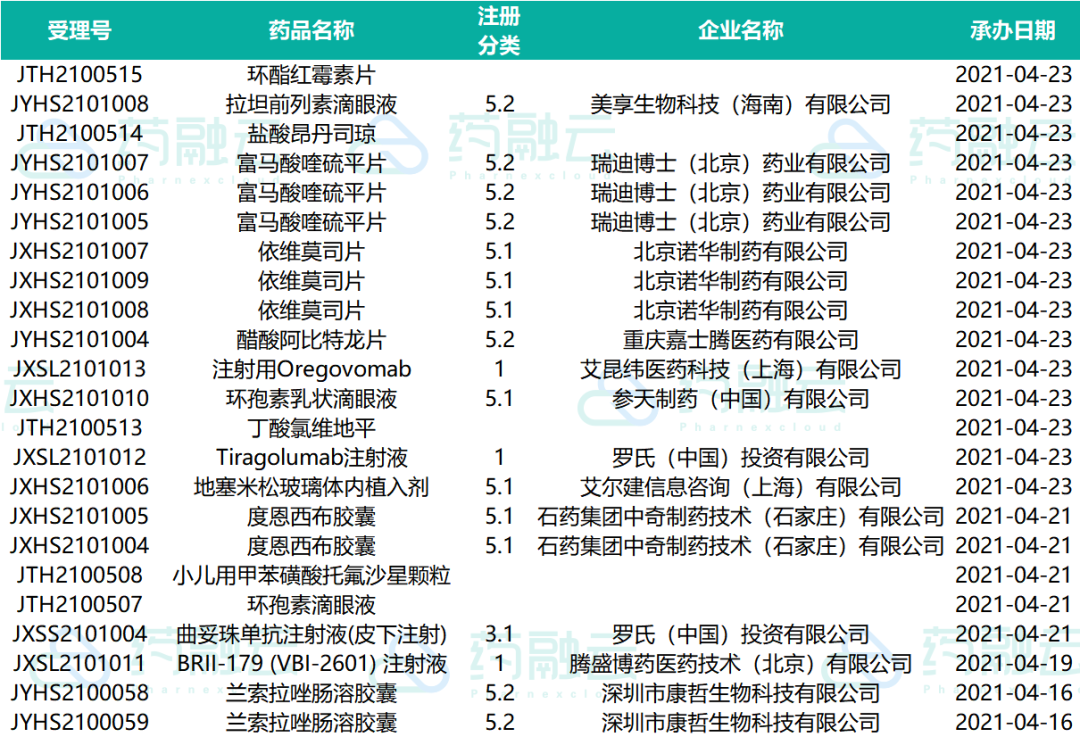
下表为2021.04.16-2021.04.25申请进口的进口药药物情况。
在审批阶段
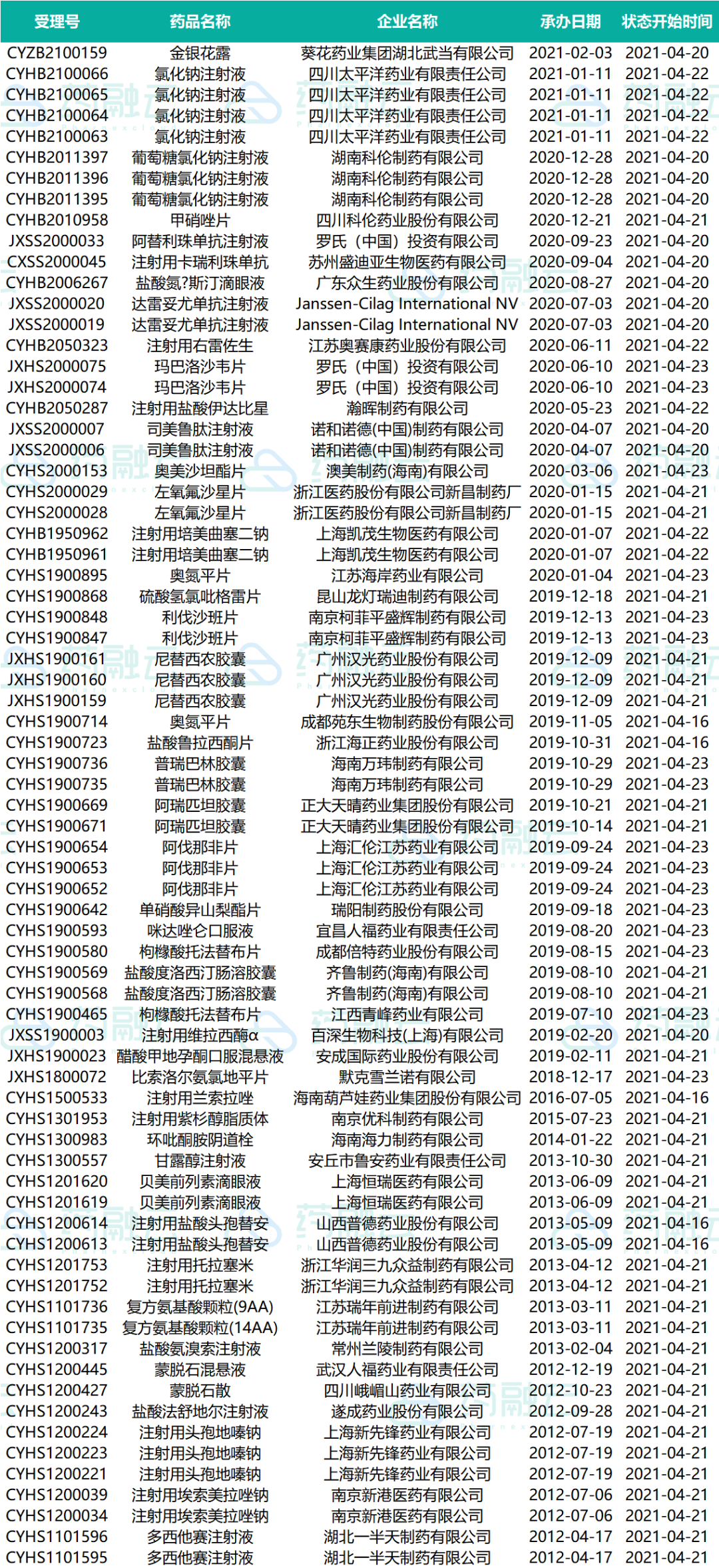
制证完毕-待发批件
近期共计62个品种(涉及受理号109个)制证完毕-待发批件,有5个品种通过一致性评价,7个品种视同通过一致性评价。下表是处于制证完毕-待发批件的过评药物情况。
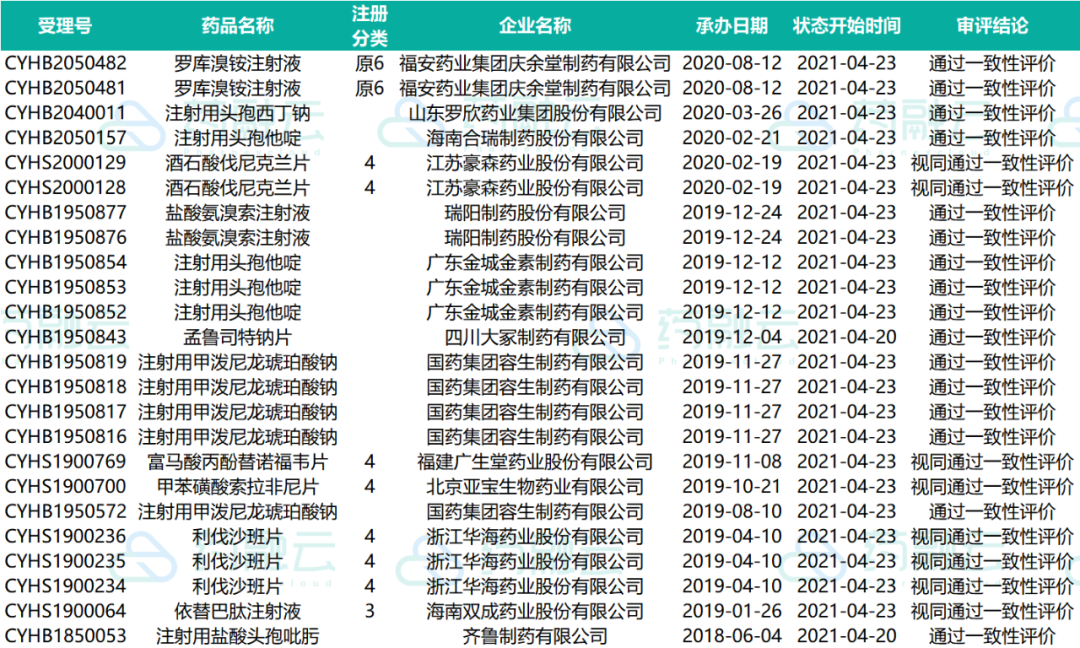
已发件药物情况
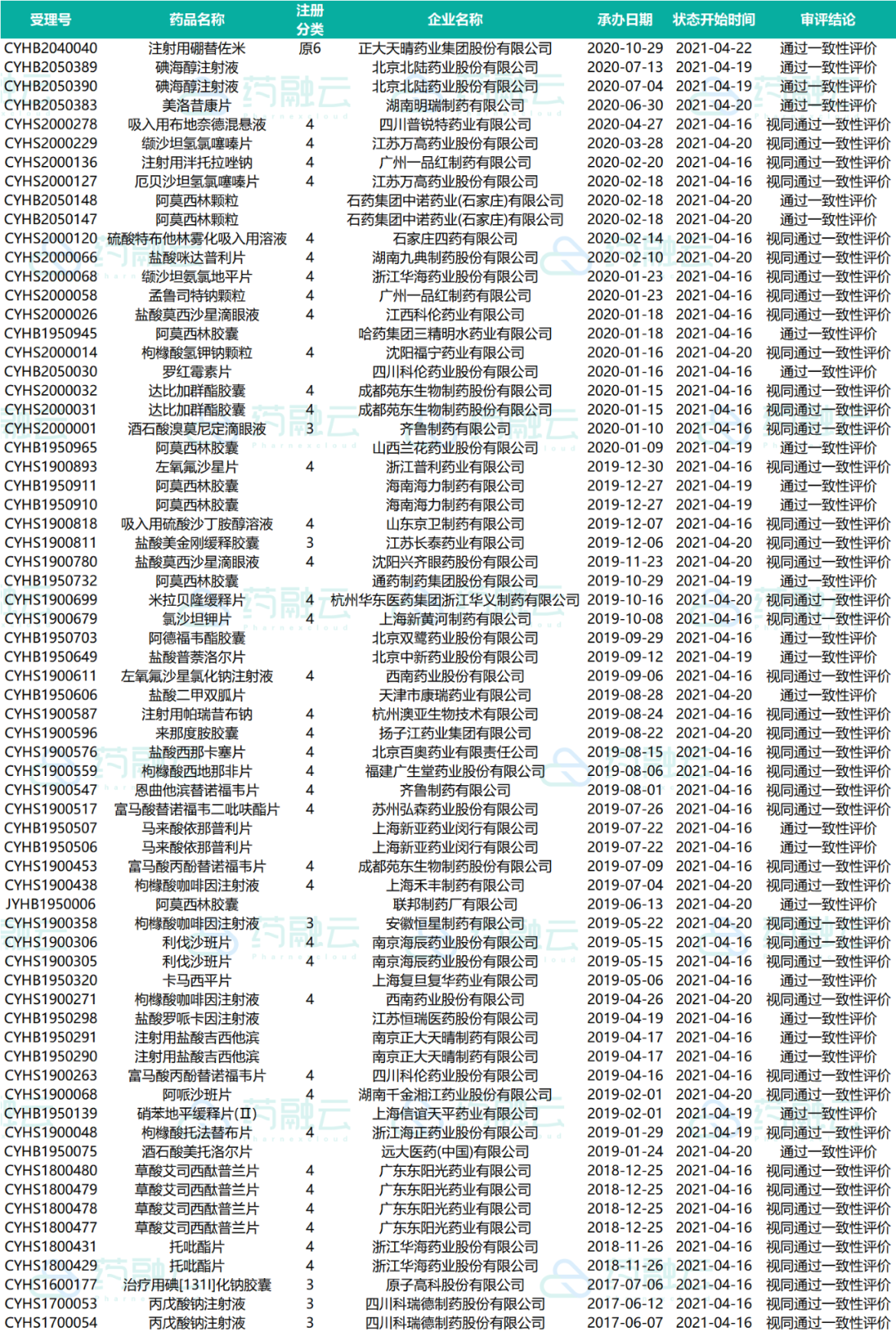
一致性评价申请
微信公众号回复CDE受理20210425
可下载2021.04.16-04.25期间CDE药品审评报告

各位朋友好,觉得本文对您有帮助,请随手点一下下方的在看,以便让你的朋友也能看到哦。



 个人中心
个人中心
 我是园区
我是园区




