孤儿药-奥曲肽微球的国内市场规模及研发概览
收藏
关键词:
孤儿药研发药
资讯来源:同写意 + 订阅账号
所属行业:化学药制剂 + 订阅行业
发布时间:
2020-09-26

10月22-24日,同写意第110期活动“第五届成都生物医药创新发展大会”,千人大会重磅来袭!本次大会共设一个主会场和六个分会场,分别就化学药品研发、生物新技术药物研发、临床研发与药政法规等话题展开交流。
肢端肥大症是一种罕见的慢性疾病,发病原因主要是垂体瘤分泌过多的生长激素
(GH)
,血浆生长激素升高直接作用于靶组织,或者间接刺激胰岛素样生长因子-1
(IGF-1)
过多分泌导致了该病的症状和病理学变化。该病好发年龄为30-50岁,男女发病概率相近,患病率约为40-70/百万人,年发病率约为3-4/百万人,预计中国肢端肥大症患者数量约7-10万人。
肢端肥大症疾病控制包括生物化学控制、缩小肿瘤体积和改善临床症状,目前治疗手段有放射治疗、手术治疗和药物治疗。通常,手术是首选治疗;对于不适宜手术的患者及术后持续性疾病的患者,可进行长期药物治疗,其中生长抑素类似物是首选。
奥曲肽
是人工改造天然生长抑素的衍生物,其生理作用与天然生长抑素相似,包括抑制生长激素功能,抑制胃酸、胰酶、胰高血糖素和胰岛素的分泌,减少内脏血流量,降低胃肠道运动等。醋酸奥曲肽注射液最初由诺华研发,并于1988年在美国上市。但肽类药物半衰期非常短,对需要短期治疗的疾病,一天内多次注射给药是可行的;而对肢端肥大症这些需要长期给药的慢性疾病患者而言,则造成极大不便。
1998年,诺华又推出注射用醋酸奥曲肽微球,将给药周期延长至4周,显著延长药物作用时间,减少用药次数,改善患者依从性。
研究数据显示,醋酸奥曲肽微球平均使用4年,68%的患者生化指标
(GH、IGF-1)
均达标。醋酸奥曲肽微球的问世为肢端肥大症治疗带来重大突破,该药物也成为全球重磅炸弹类产品。专利到期前,醋酸奥曲肽微球在2016年的全球销售额达16亿美元。
奥曲肽与奥曲肽微球适应症和临床使用方法比较
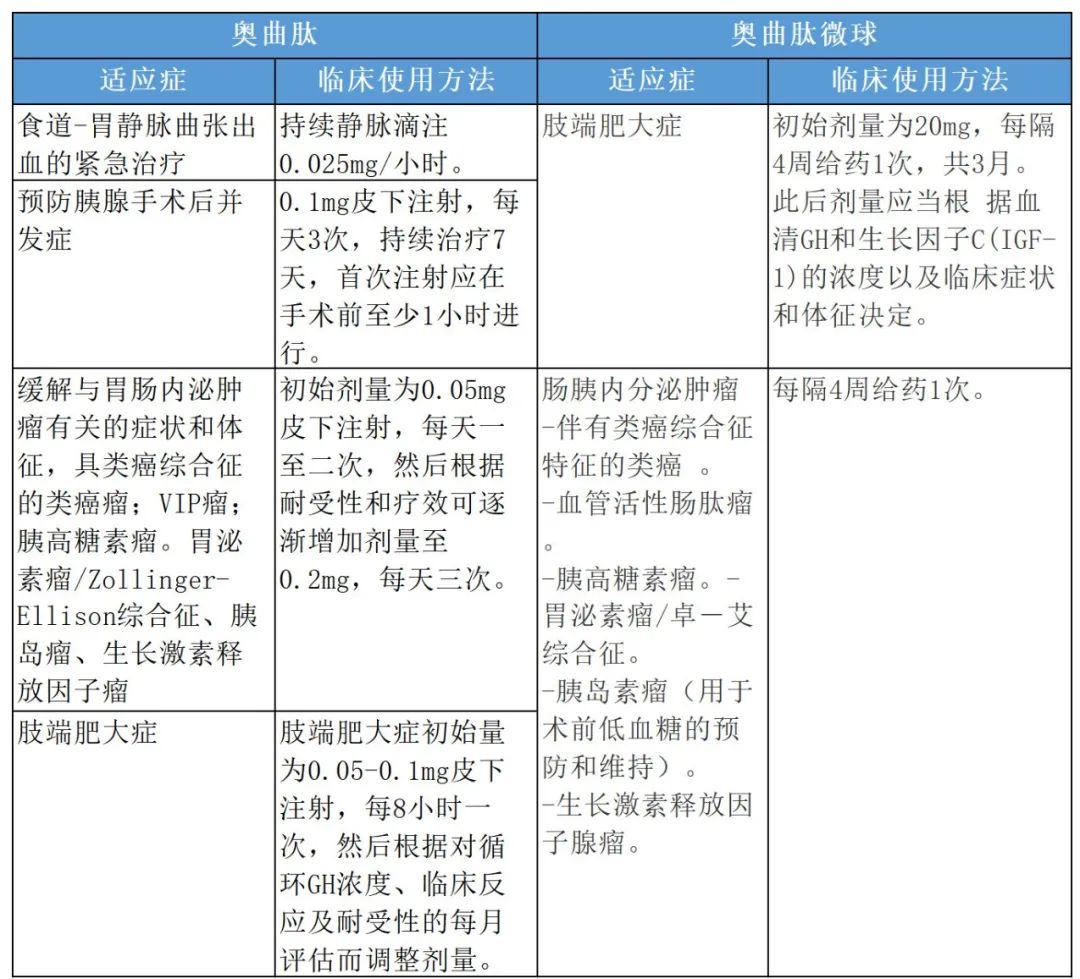
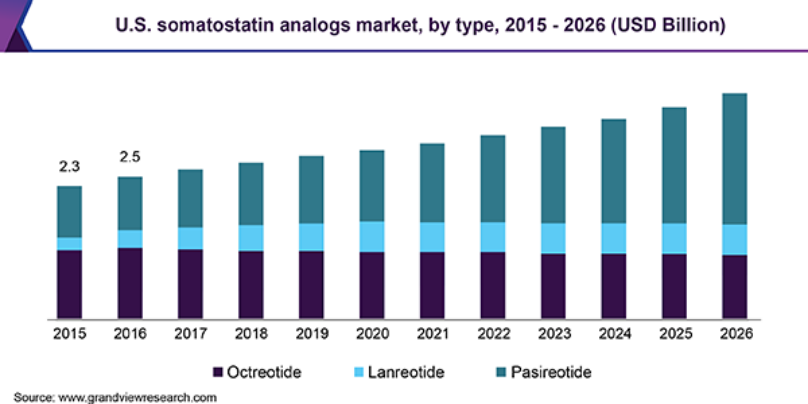
目前,全球治疗肢端肥大症的长效生长抑素类似物主要是奥曲肽微球、帕瑞肽和兰瑞肽,分属于诺华和益普生两家公司。2018年生长抑素类似物的市场为55亿美元,其中肢端肥大症的市场占45%,胃肠胰腺内分泌肿瘤适应症占比紧随其后。奥曲肽微球和兰瑞肽均于2003年在中国上市销售,帕瑞肽还未在中国上市;益普生研发的
(预充式)
醋酸兰瑞肽缓释注射液于2019年12月获批在中国上市,进一步提升了患者给药的便捷性。
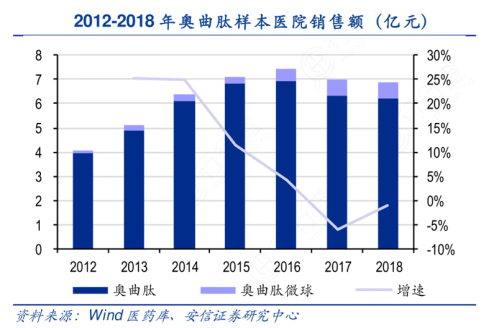
国内已有奥曲肽上市,至少50家以上国内企业可以生产、提供奥曲肽,但截止目前尚无国产奥曲肽微球上市。根据Wind医药库数据,2018年我国样本医院奥曲肽销售额约6.9亿元,同比下滑1.0%;其中奥曲肽微球销售额约0.7亿元,市场占比约10%。奥曲肽微球销售增速明显高于行业增速,市场替代效应明显,这也与诺华的奥曲肽微球在部分省市可以医保报销,以及2018年被纳入国家基本医疗保险乙类医保有关。
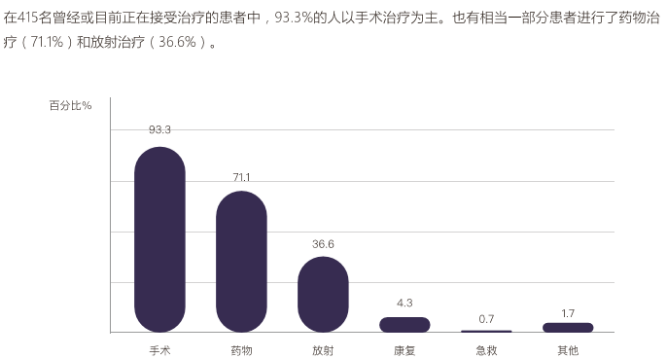
2020年6月发布的《中国肢端肥大症患者综合社会调查白皮书》,共计调研了474名受访者,93.3%的患者以手术治疗为主,71.1%的患者使用了药物治疗,36.6%的患者使用了放射治疗
(图3)
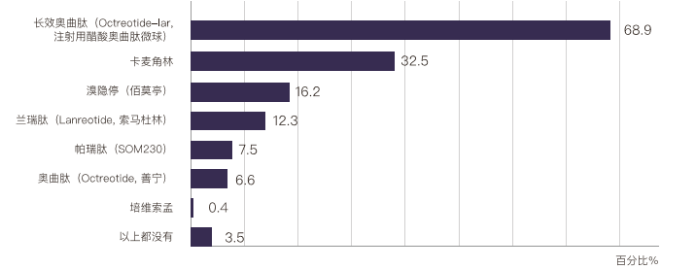
;对于正在使用药物治疗的228名患者,68.9%使用了长效奥曲肽,12.3%使用了兰瑞泰,7.5%使用了帕瑞肽
(图4)
。从以上数据可知,大部分患者曾经或正在使用生长抑素类似物治疗肢端肥大症。
虽然2018年奥曲肽微球终于进入医保报销目录乙类范围,医保支付标准分别为7911元/瓶
(30mg
)
、5800元/瓶
(20mg)
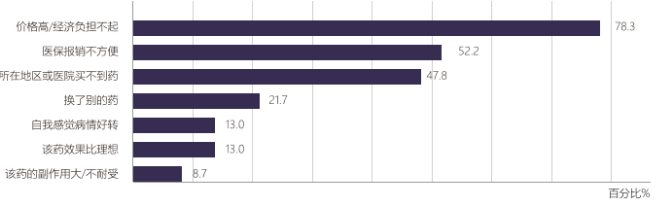
,患者自付的比例在50%左右。但根据调研结果,,价格高/经济负担不起
(78.3%)
、医保报销不便
(52.2%)
、所在地区和医院买不到药
(47.8)
,依旧是曾使用过生长抑素类似物治疗而停止使用的主要原因
(图5)
。所以,奥曲肽微球仍是一个未被满足的临床市场。
保守估计,中国现有7万肢端肥大症患者,30%患者需要长期使用生长抑素类似物治疗。如果国产奥曲肽微球
(30mg/瓶)
价格在5000元/月,患者自费支付2500元/月,那么一个患者一年的药费为6万元
(自付3万元/年)
,奥曲肽微球一年的销售额预计约为12亿元,而这只是奥曲肽微球其中一个主要适应症而已。如果再考虑胃肠胰腺内分泌肿瘤的治疗,奥曲肽微球的中国市场规模约在20亿元左右。
奥曲肽微球有如此一个规模的市场,且是国内肢端肥大症患者一个未被满足的需求,绝对是国内企业发展微球制剂的一个绝佳机会。但从诺华奥曲肽微球于2003年在中国上市后,一直无国产奥曲肽微球上市,这可能是由于微球制剂有着很高的技术壁垒造成的。
微球是指将药物溶解或分散于天然或合成高分子材料中所形成的微小球体或类球体,粒径一般在1-250μm范围内。微球将药物包埋或吸附在聚合物分子的表面,通过皮下或肌肉注射进入体内后,通过载体表面快速释放、药物扩散、聚合物的溶蚀降解等方式,实现药物的缓慢释放,可大大延长药物的半衰期。
微球制剂产业化技术壁垒较高,研发成本高昂,研发周期长:首先微球的工艺复杂,控制困难,需要定制专门的设备,并在生产过程中不断调试;其次质量控制困难,粒度分布、载药量、释药速率、突释问题、无菌度、残留溶剂都是微球质量的主要因素;最后,中试放大困难,实现产业化仍是主要瓶颈之一。由于微球制剂难以线性放大生产,需要探索合适的参数,因此技术要求较高。
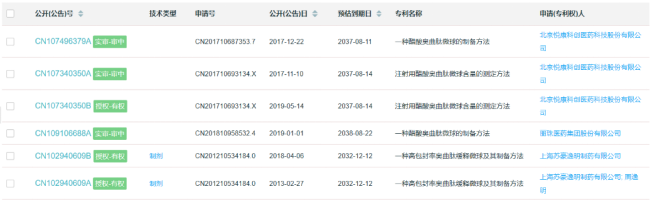
从目前国内奥曲肽微球的制备专利申请来看,主要为北京悦康科创、丽珠、上海苏豪逸明制药
(图6)
;
而目前申报奥曲肽微球临床试验申请的主要为:长春金赛药业和丽珠制药,分别于2017年6月和2020年2月获得了临床试验开展许可
(图7)
。
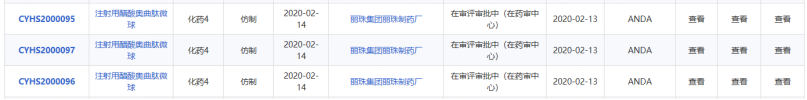
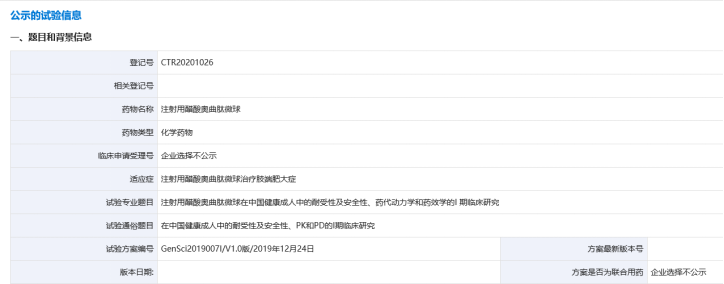
从临床试验登记网站可知,目前只有长春金赛登记了一项“健康成人中的耐受性及安全性、药代动力学和药效学的I 期临床研究”,并于2020年5月19日入组了首例健康志愿者
(图8)
。
丽珠集团于2020年9月10日发布公告称,注射用醋酸奥曲肽微球已获进行BE临床试验,预估这将加速国产奥曲肽微球的上市进程
(图9)
。
谢生荣,中国药科大学药理学硕士,临床医学学士,南京市罕见病家庭关爱中心理事长。
2
013年起触及罕见病研究,参与过3个孤儿药在中国的注册、临床策略,目前专注于罕见病疾病自然史研究、罕见病患者药物可及性的解决策略探讨、以患者为中心的立足中国数据的全球孤儿药开发模式研究。
10.17-18,西安· 高新国际会议中心
▲ 牛俊奇教授领衔,本次大会将聚焦肝脏疾病,特别是病毒性乙型肝炎和脂肪性肝病治疗的基础研究,将对治疗新靶点,和新策略进行深入研讨。
10.22-24,成都· 盛美利亚酒店
▲
千人大会重磅来袭!本次大会共设一个主会场和六个分会场,分别就化学药品研发、生物新技术药物研发、临床研发与药政法规等话题展开交流。












 个人中心
个人中心
 我是园区
我是园区




