
近日(2021年4月13日),吉利德宣布FDA加速批准了其靶向Trop-2-ADC药物Trodelvy(sacituzumab govitecan-hziy)的新适应症--局部晚期或转移性尿路上皮癌,这类患者接受铂类化疗和免疫治疗后出现了疾病进展。
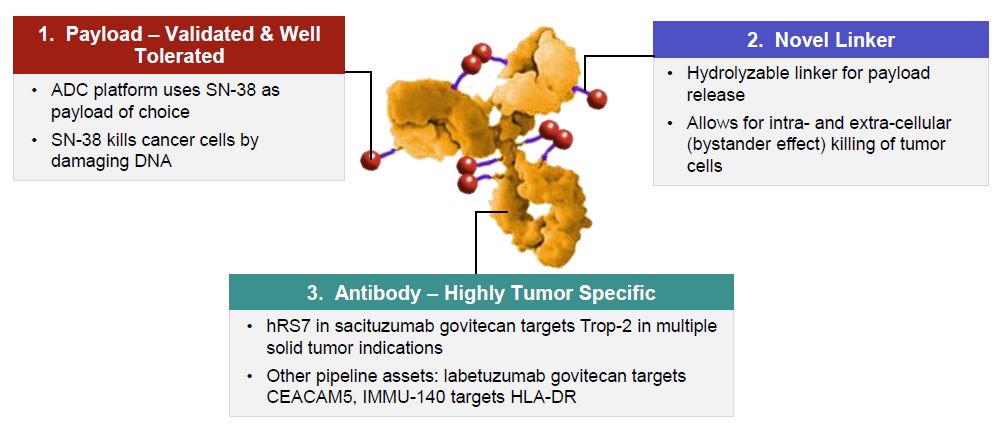
Trodelvy是一款靶向Trop-2-ADC药物,利用人源化抗体hRS7作为靶向载体与伊立替康活性代谢产物SN38偶联而成。
2020年4月23日,Trodelvy获得了FDA加速批准,用于至少接受过两种治疗的转移性三阴性乳腺癌(mTNBC)患者,这是首个专门治疗复发或难治性mTNBC的ADC药物,也是FDA批准的第一个靶向Trop-2的ADC药物。
基于其Ⅲ期ASCENT试验的惊艳临床数据,一周前(2021年4月7日),FDA已将Trodelvy的加速批准提升为完全批准,
用于
至少接受过两种或多种治疗的转移性三阴性乳腺癌(mTNBC)患者的治疗。
此次新适应症获得加速批准是基于一项名为TROPHY的Ⅱ期临床试验数据,在该项临床研究中,接受Trodelvy治疗的转移性尿路上皮癌患者中有27.7%实现了缓解,5.4%的完全缓解,22.3%的部分缓解,中位缓解持续时间为7.2个月。Trodelvy在TROPHY中的安全性与在其它肿瘤中所观察到的一致,10%的患者因治疗相关不良事件终止治疗。FDA在批准Trodelvy用于治疗mTNBC时,就在说明书上就打上一则黑框警告,提示该药服用后可能会出现严重中性粒细胞减少和腹泻。

Trop2
是一个具有多种潜在适应症的广谱靶点,在
多种肿瘤,如胰腺癌、乳腺癌、结肠癌、胃癌、口腔鳞癌、卵巢癌等上高表达。Trop2可促进肿瘤细胞增殖、侵袭、转移扩散等过程,其高表达与肿瘤患者生存期缩短及不良预后密切相关。
Trodelvy的成功上市让这个靶点走进大众视野,成为现在ADC领域的第二大热门靶点,目前已有
第一三共、
杭州多禧生/君实
、科伦、云顶新耀/Immunomedics、百奥泰等多家药企布局,国内方面,云顶新耀稍快,从Immunomedics那直接引进了Trodelvy,目前已推进到了临床II期阶段,百奥泰已经出局,其他公司Trop-2-ADC在研产品的临床进度基本上在同一水平线上。
TROP-2布局研发除了以上几家
药企,还有第二梯队的
石药集团、豪森药业及洛启生物等,此前,三家都已公开了各家候选产品的专利。
除了A
DC药物外,
复宏汉霖今年初还从Chiom那引进了TROP-2单抗。
2019年开始,全球ADC进入快速发展期。
作为首个摘得该靶点桂冠的产品,
Trodelvy的先发优势明显,
美国证券公司Cowen曾预计这款药的销售峰值有望达到40亿美元/年。
参考出处
https://www.businesswire.com/news/home/20210413006168/en
欢迎个人转发分享。其他任何媒体、网站如需转载或引用本网版权所有内容须获得授权且在醒目位置处注明“转自:生物制药小编”。







 个人中心
个人中心
 我是园区
我是园区




