▎药明康德内容团队编辑
2022年1月18日,优时比(UCB)公司宣布了抗IL-17A/F抗体Bimzelx(bimekizumab)的一项3期临床试验的积极中期分析结果。试验达到其主要终点和所有重要次要终点,表明bimekizumab能有效改善活动性非放射学中轴型脊柱关节炎(nr-axSpA)成人患者的临床症状。这项试验与该药在强直性脊柱炎患者中开展的另一项试验,共同证明了bimekizumab在整个疾病谱系中的治疗潜力。基于获得的数据,优时比计划在今年第三季度提交bimekizumab治疗中轴型脊柱关节炎(axSpA)的监管申请。

axSpA是影响骨盆关节和脊柱的一种脊柱关节炎,可表现为慢性炎症性背痛,脊柱僵硬,骨骼功能和活动能力受损。全世界约有450万成年axSpA患者。根据X光放射学检测能否发现骶髂关节的损伤,患者可分为非放射学中轴性脊柱关节炎(nr-axSpA)和r-axSpA两类。axSpA的总患病率在成人中约为0.2%~1.4%,约一半是nr-axSpA患者,10%~40%的nr-axSpA患者在2~10年内进展为强直性脊柱炎。
人源化单抗bimekizumab,能够强效并特异性地中和白细胞介素17A(IL-17A)和IL-17F。
这是驱动多种慢性炎症的两种关键细胞因子。IL-17A与IL-17F具有大于50%的结构同源性和重叠的生物学功能,在多种发炎的人体组织中均上调,并与其他促炎细胞因子,例如肿瘤坏死因子(TNF)协同作用,放大炎症反应。同时结合这两种细胞因子,阻止它们与细胞表面表达的IL-17受体相互作用,让bimekizumab能更好地发挥抗炎症的功能。去年9月,该药获欧盟批准治疗中重度斑块状银屑病患者。
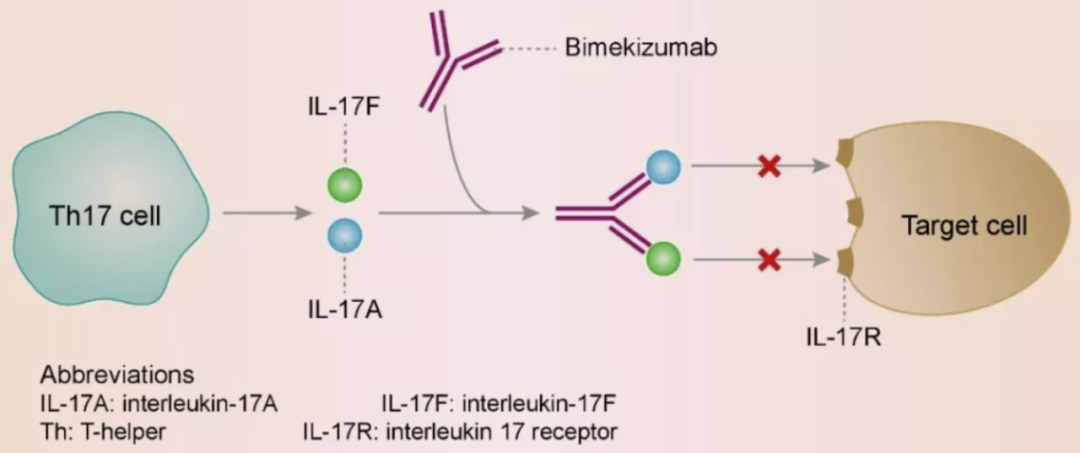
▲Bimekizumab的工作机理示意图(图片来源:参考资料[2])
第16周时,与安慰剂相比,bimekizumab组达到试验主要终点,获得国际脊柱关节炎协会评估40%(ASAS40)应答的患者比例表现出具有统计学显著性和临床意义的改善。ASAS测量了4个不同领域的疾病改善:患者对疾病活动、脊柱疼痛、身体功能和炎症的整体评估。ASAS40意味着症状较基线改善至少40%。
该研究达到了所有重要的次要终点。试验中药物表现出的安全性与既往研究一致,未观察到新的安全性信号。
免疫学解决方案执行副总裁、优时比美国负责人Emmanuel Caeymaex先生表示:“我们很高兴分享bimekizumab治疗axSpA临床项目第二项3期临床试验的顶线结果。加上之前获得的3期临床试验积极数据,支持了bimekizumab在整个axSpA谱系中改善患者预后的临床潜力。”
参考资料:
[1] Positive Top-Line Results for Bimzelx[®]▼(bimekizumab) in Phase 3 Non-Radiographic Axial Spondyloarthritis Study. Retrieved January 18, 2022, from https://www.ucb.com/stories-media/Press-Releases/article/Positive-Top-Line-Results-for-BimzelxRVbimekizumab-in-Phase-3-Non-Radiographic-Axial-Spondyloarthritis-Study
[2] Bimekizumab Overview. Retrieved December 6, 2019, from https://www.creativebiolabs.net/bimekizumab-overview.htm
免责声明:药明康德内容团队专注介绍全球生物医药健康研究进展。本文仅作信息交流之目的,文中观点不代表药明康德立场,亦不代表药明康德支持或反对文中观点。本文也不是治疗方案推荐。如需获得治疗方案指导,请前往正规医院就诊。
版权说明:本文来自药明康德内容团队,欢迎个人转发至朋友圈,谢绝媒体或机构未经授权以任何形式转载至其他平台。转载授权请在「药明康德」微信公众号回复“转载”,获取转载须知。








 个人中心
个人中心
 我是园区
我是园区




