
1
加科思CD73单抗JAB-BX102获CDE临床默示许可,用于治疗实体瘤!

2022年3月25日,CDE官网数据显示,加科思自主研发的抑制CD73酶学活性的人源化单克隆抗体JAB-BX102获临床默示许可。根据官网数据显示,开展临床适应症应为实体瘤。JAB-BX102也是加科思首个进入临床阶段的大分子研发项目,此前,已经与2021年10月15日宣布收到FDA临床试验批准通知书,目前已经在美国启动针对实体瘤患者的I/IIa期临床试验(NCT05174585)。
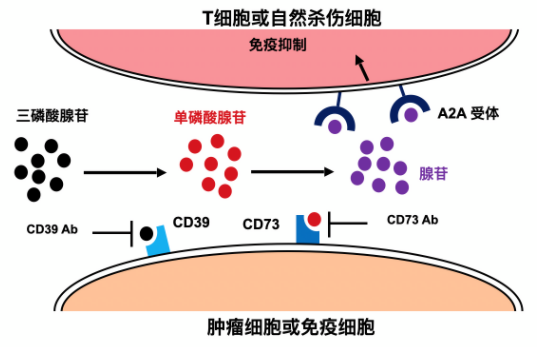
CD73(ecto-5’-nucleotidase,Ecto5’NTase)是一种膜结合/游离蛋白,能将AMP水解为腺苷,腺苷与细胞表面P1受体作用后抑制肿瘤免疫反应。CD73在很多恶性肿瘤中的表达显著升高,包括黑色素瘤、三阴乳腺癌、非小细胞肺癌、肾癌、膀胱癌、前列腺癌、胃癌、结直肠癌、卵巢癌和恶性胶质瘤等。根据目前公布的一些CD73抑制剂的初步临床研究结果,其可能对非小细胞肺癌、三阴性乳腺癌、肾癌及其他实体瘤有潜在的临床疗效。
药明巨诺瑞基奥仑赛新适应症申请获CDE拟纳入突破性疗法、优先审评!

2022年3月24日,CDE官网数据显示,药明巨诺品种瑞基奥仑赛新适应上市申请被纳入拟优先审评序列,拟增加适应症为经过二线或以上系统性治疗的成人复发或难治性滤泡淋巴瘤,包括组织学分级为1、2、3a级的滤泡性淋巴瘤。同时,以上海明聚生物科技有限公司名义申报的JWCAR029(CD19靶向嵌合抗原受体T细胞),即瑞基奥仑赛用于经过二线及以上治疗的成人复发难治性套细胞淋巴瘤被拟纳入突破性治疗药物程序。
2016年,药明康德和CAR-T制药公司Juno成立合资公司药明巨诺,共同开展CAR-T和TCR(T细胞抗原受体)疗法的研发和生产。2018年1月,新基以90亿美元的价格收购了Juno。2019年1月,BMS斥资740亿美元收购了新基。2021年9月,瑞基奥仑赛注射液获NMPA的批准,这是继复星凯特阿基仑赛注射液后,国内第2款获批的CAR-T疗法、全球第6款获批上市的CAR-T产品,批准适应症为用于治疗经过二线或以上系统性治疗后成人患者的复发或难治性大B细胞淋巴瘤(r/r LBCL)。
本次新适应症的上市申请是基于瑞基奥仑赛用于治疗复发或难治性B细胞非霍奇金淋巴瘤中国成人患者的单臂、多中心、关键性临床研究(RELIANCE研究,NCT04089215)B队列的研究结果,该研究结果已发布于2021年12月第63届美国血液学会(ASH)年会。结果显示,瑞基奥仑赛展现了治疗r/r FL极高且持续的疾病缓解率(3个月最佳完全缓解率和客观缓解率分别为92.6%及100%)、以及可控的CAR-T治疗相关毒性(任何级别的细胞因子释放综合征(CRS)及神经毒性(NT)的发生率分别为42.9%及17.9%,≥3级CRS和NT的发生率分别为0%及3.6%)。
2
医药交易
康方生物AK112单药或联合化疗新辅助/辅助治疗可切除非小细胞肺癌的II期临床完成首例患者入组

AK112是全球同类药物中率先进入III期临床研究阶段的产品。目前,AK112治疗EGFR-TKI耐药的非小细胞肺癌的注册性III期临床研究已经启动(CTR20213079),AK112一线治疗PD-L1阳性非小细胞肺癌,AK112一线治疗广泛期小细胞肺癌的III期临床试验即将启动。
参考资料
加科思官网、企业公告
https://mp.weixin.qq.com/s/dWc3v-q2jklNx-wmQ3QJOg
BI官网




 个人中心
个人中心
 我是园区
我是园区




