专访武汉大学沈吟|针对X连锁视网膜劈裂症临床结果积极,治疗视网膜色素变性的光敏蛋白计划明年开展临床试验
收藏
关键词:
专访临床治疗
资讯来源:DeepTech深科技 + 订阅账号
发布时间:
2022-10-28
眼睛是人体最为重要的感觉器官之一,人所接收的外界信息中有超 80% 都是通过眼睛获取的。
有统计数据显示,国内失明患者超过 2600 万人,每年新增失明患者 45 万人。而据《柳叶刀》发表的一项数据显示,预计到 2050 年,
全球将会有近 9 亿人将受到失明以及严重视力障碍的影响。
其中,
X 连锁视网膜劈裂症(XLRS)
是一种遗传性致盲眼科疾病,发病率最高可达五千分之一,国内大约有数十万 XLRS 患者,患者通常在学龄期便出现进行性视力损害,疾病后期可因并发玻璃体出血、视网膜脱离,最严重会导致失明。
在发病早期, XLRS 儿童患者的视力差,非常容易被误诊为弱视、屈光不正等,常辗转多处确诊才发现是视网膜劈裂导致的视力差。临床上常规方法难以治疗这种由于基因缺陷引起的视网膜疾病。
“针对 XLRS,目前的常规治疗手段主要以随访观察、保守治疗及以手术治疗网脱并发症为主,但是这些方法对于提高视力的作用非常有限,所以治疗效果并不理想。”武汉大学人民医院眼科中心沈吟教授告诉生辉。
随着基因治疗方法的发展,由腺相关病毒(AAV)介导的基因治疗或将成为治疗 XLRS 的新途径。先前研究表明,XLRS 致病基因为视网膜劈裂蛋白基因(RS1),已被定位于染色体 Xp22.13,是一种可编码包含 224 个氨基酸的蛋白质。
“由于 XLRS 疾病的基因突变原因很明确,基因疗法或许能够成为治疗该病的新方法。基于此,我们开展了一项针对 XLRS 的 IIT 临床试验(院内临床试验),目前两名患者的治疗效果较为积极。”
沈吟表示。
▲图|正常人的黄斑 OCT(左)和视网膜劈裂病人的黄斑 OCT(右)
沈吟博士期间师从中国科学院院士视网膜专家杨雄里教授,曾先后在美国爱因斯坦医学院、斯坦福大学从事博士后研究和神经眼科的临床工作,研究方向主要围绕神经眼科和视网膜遗传性疾病的基因治疗。作为武汉大学人民医院人才引进后,专注于眼科疾病的研究和临床诊疗工作。目前,沈吟是武汉大学眼科研究所所长,武汉大学人民医院眼科中心常务副主任。
全球范围内曾开展过两项针对 XLRS 基因疗法的临床试验,一项为美国国立眼科研究所(NEI)发起的 Ⅰ/Ⅱa 期前瞻性、单中心临床研究; 另一项为美国 AGTC 公司发起的 Ⅰ/Ⅱ 期非随机、单组分配临床研究。然而,两项临床试验的结果都并不理想,目前处于停止或暂停阶段。
“我们开展的这项临床试验,是在已有经验基础上设计的一项新的临床试验。
我们重新设计了新的方法,并通过大量的小动物和大动物试验以验证其安全性和有效性
,通过专业团队的商业化运营开发出基因治疗药物,经过严格的伦理审核后,推进到目前的临床试验阶段。”沈吟表示。
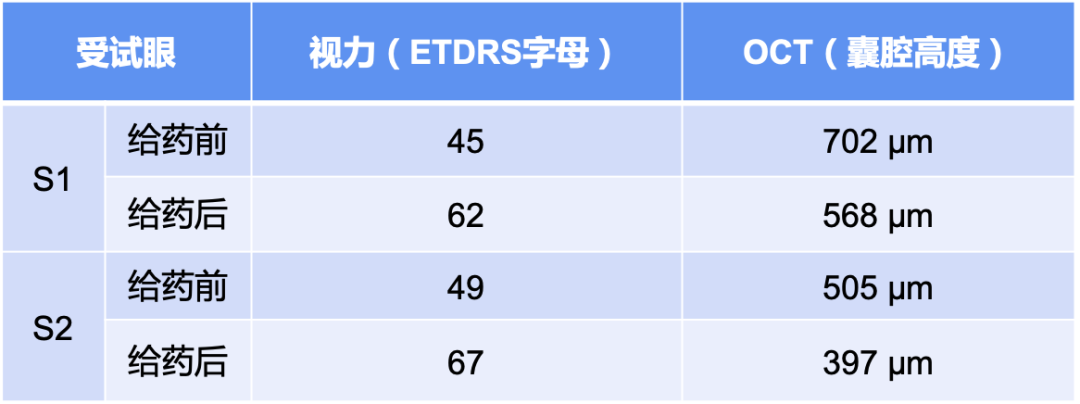
据介绍,这项临床研究已入组了
两名 XLRS 患者。
在接受基因治疗前,两名患者的视力状况较差,视网膜劈裂很严重。“经过基因治疗后,我们目前观测到的
两名患者各项指标均表现正常,没有出现视网膜出血,网脱等不良反应。
视力的改善非常明显,
目前的结果比较乐观,已经看到了初步的疗效。
现阶段,我们还在监测临床数据,
计划在未来 1-2 个月内将会正式公布临床数据结果。
”沈吟说道。
对于一款创新的基因治疗药物而言,
安全性
是第一位的。“我们更关注药物的安全性。就目前的数据可以证明,我们的安全性较好,目前没有发现因注射药物本身引起的不良反应。”沈吟指出。“我们还在整理和分析临床数据阶段,也会有更多的临床病人入组,未来将发表正式的研究结果。目前两名病人的受试眼的视力都有比较明显改善(从 0.1 到 0.3),生活质量得到有较大幅度的提升。”
创新药物研发从靶点发现,到技术研发、临床试验,再到最后上市,最后能够成功很不容易,漫长的过程中有太多因素会导致药物研发失败。在沈吟看来,“
并不是说国外的 XLRS 临床试验终止了,就代表着基因治疗 XLRS 的这条路是行不通的。
分析了先前国外开展的相关临床试验,我们基于自己的研究、分析与判断,认为这项临床试验的原始靶点没有问题,
按照我们推论的原理设想重新进行规划,再次开展的临床试验,探索和尝试其他路线。
这对于我们而言也算是“后发”优势,弯道超车。”她介绍道。
这项临床试验的开展也并非一帆风顺,沈吟坦言,研究过程中伴随着外界一些质疑的声音,国外都失败了,国内科研人员做的研究能成功么?“虽然国外的 XLRS 临床试验没有成功,但我们对于新开展的临床试验非常有信心,我们的自信是基于充分的调研、深入
思考和大量实验基础之上的自信。”她说。
除此之外,国内基因治疗仍然是一个新鲜事物。“在一项技术还没有出现的时候,不可能有与之配套的规则,所以规则总是晚于技术出现。然而,在规则尚不健全的时候开展新技术的临床研究会面临很多困难。感谢学校和医院各级领导的关怀和海内外同行朋友的帮助,我们在多方力量的协助下,最后顺利开展这项临床试验研究。”沈吟表示。
据了解,沈吟教授团队
从 2016 年开始对 XLRS 进行研究,也是国内最早进入基因治疗临床阶段的研究团队。
“我们前期研究开展的比较早。”沈吟说道,“我们一直专注于遗传性眼病和神经眼科,门诊有很多的遗传眼病患者辗转多地寻求帮助,寻医过程非常痛苦,有巨大的未被满足的临床需求。这项研究的开题起源是从临床中来,经过实验室多年研发,最后再回到临床中去。
尽快回到临床、尽快治疗患者,是我们内心最大的诉求。
”她补充说。
针对这项临床试验,沈吟表示,“接下来我们会进一步做好临床试验,会更加有针对性的进行优化方案,
扩大入组患者规模,明确药物适应人群等。
”
她坦言,“临床试验是一个非常漫长的过程,将科研团体的科研成果转化出来,我们的力量是非常单薄的,所以我们也在寻求更多合作者,政府资助和社会资金的帮助,以期更加快速和顺利地开展这项临床试验,造福广大患者。”
“创立公司进行技术和成果转化,不做跟风研究,做创新性探索”
1963 年,美国分子生物学家、诺贝尔生理学或医学奖获得者 Joshua Lederberg 首次提出了
基因交换
和
基因优化
的概念,为基因疗法的发展打下基础,同时也拉开了基因治疗时代的序幕。
作为能够编码蛋白质、负载遗传信息的基本单位,基因和遗传病的发生和发展密切相关,从理论上讲,如果能够通过基因疗法修复患者的错误基因或提供正确基因,那么
一次治疗就有可能产生长期的治疗效果。
从本质上来看,基因疗法核心构成是
目的基因、递送载体
以及
转染
后表达功能
,因此,递送载体是一项基因疗法能否成功的关键因素之一。
腺病毒相关病毒(AAV)载体具有免疫原性低、安全性高、不插入宿主基因组、感染宿主范围广并且能在组织中长期稳定表达等诸多优点。“AAV 是很多基因治疗的重要载体,在基因疗法临床管线中,
基于 AAV 的基因治疗大约占据 43%
,将近一半的比例。”沈吟指出。
如今,AAV 已在眼科研究中被用于遗传性视网膜疾病的基因治疗递送载体。2017 年,全球首款针对眼科疾病靶向 RPE65 基因突变的基因治疗药物(Luxturna)被 FDA 批准上市。该药物借助 AAV 将正常 RPE65 基因递送到患者体内,从而让患者可以产生正常功能的蛋白(RPE65)来改善视力,可以用来治疗包括莱伯氏先天性黑矇症等由 RPE65 基因突变引起遗传眼病。
“全球范围内,截至目前共有 5 款基于AAV的基因治疗药物成功上市。”沈吟介绍说,“截止到今年 6 月,
在全球已开展的 239 项 AAV 基因疗法临床试验中
,眼科疾病的临床试验占 21%。就国内而言,目前已有 14 项 AAV 基因疗法临床试验申请被国家药品监督管理局(NMPA)正式受理或获批的,其中有相当一部分也是针对眼科疾病。”她补充说。
基因疗法在眼科领域具有一些“先天”优势。“很重要的一个原因是,相较于人体的其他全身系统,眼球处在一个相对封闭的腔体里面,算是一个相对‘独立’的器官,免疫原性也相对较小,所以采用基因疗法治疗眼科疾病对全身系统的影响较小,相对较为安全。”她指出。
围绕视网膜遗传性疾病,沈吟和团队近年来已在 PNAS、STTT、Science Advances、eLife、Nature Structural and Molecular Biology 等期刊发表了大量的研究论文。“科研不能只在学术杂志上发表文章,发表文章只能证明已经具备了相应的科研能力,实际获益的受众很小,真正有意义的事情,
是把科研成果转化为到实际临床中去
,给到病人帮助,满足大量急迫等待帮助的患者的临床需求。”沈吟指出,“我们在临床方面遇到常规医学方法解决不了的问题,就把问题带到实验室进行研究和解决,问题解决以后推广到产业化,最终回归并应用到临床。而想要真正帮助到更多患者,就需要走市场化的道路,通过产业化的方式给到病人有效的治疗药物。”她补充说。
2019 年,沈吟创立了中眸医疗科技有限公司(简称中眸医疗),目前已拥有完善的专注于视网膜研究的研发部门。“我们的目的就是把实验室已经取得的研究成果进行产业转化。”沈吟表示,“基于我们的科研优势,目前公司布局的是一系列‘组合式’的产品管线,包括前期的药物设计,然后到动物实验验证,以及目前进行的临床研究等。”
据了解,现阶段中眸医疗围绕眼科疾病
共开展了 5 条在研的管线
,主要包括青少年视网膜劈裂症、无脉络膜症、全色盲、视网膜色素变性以及年龄相关性黄斑变性等疾病。
“考虑到大量临床需求,对于治疗那些不分基因类型的视网膜色素变性的光敏蛋白疗法的呼声很强,所以我们把这条产品管线进行了前置,现阶段是
开发新型光敏蛋白
的同时进行
改造升级和产品迭代。
”沈吟介绍道,“治疗视网膜色素变性的光敏蛋白,
预计明年开始进行临床试验。
”
谈及国内针对遗传性眼病基因疗法的产业现状,沈吟表达了自己的一些看法,她表示,“国内层面,眼科疾病的赛道竞争日趋激烈,很多企业会跟风开发。以目前比较热门的 RPE65 和年龄相关性视网膜黄斑变性为例,参与眼科基因治疗药物赛道的企业也开始多起来,可能是由于眼科基因治疗有一条比较安全稳妥的药物开发技术路线。但对于我们而言,我们需要
去选择做目前没有人做的、原创的、更难的、具有创新性的研究工作。
进窄门,走远路,见微光,造福广大患者。”沈吟总结道。
1.https://doi.org/10.3760/cma.j.cn511434-20210816-00439
2.http://mri.whu.edu.cn/info/1013/5281.htm
3.http://www.rmhospital.com/d/edu/170.html
4.https://mp.weixin.qq.com/s/NtuFL9vb2nuOXxfOpIjUxQ









 药选址
药选址







